
| 温度(℃) | 230 | 300 | 600 | 670 |
| 转化率(%) | 95 | 80 | 19 | 5 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
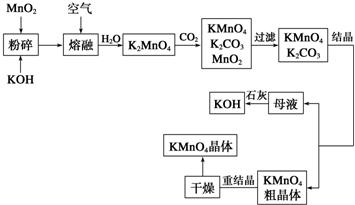
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH3:0.002 mol?L-1 |
| B、O2:0.001 mol?L-1 |
| C、NO:0.0015mol?L-1 |
| D、H2O:0.09 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操 作 步 骤 | 现 象 及 结 论 | |
| 方法一 | ||
| 方法二 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 相关实验 | 预期目的 | |
| A | 把等质量的两份同种大理石块中的一份研成粉末,在同温度下分别与等体积同浓度的盐酸反应,观察放出气体快慢. | 验证接触面积对化学反应速率的影响. |
| B | 向Na2CO3酚酞溶液中滴加BaCl2溶液后红色褪去. | 验证Na2CO3溶液中存在水解平衡 |
| C | 直接将表面积相同的铝条和镁条投入同温度滴有酚酞的热水中,观察产生气泡的速率及溶液的颜色变化. | 比较镁、铝金属性强弱 |
| D | 在装有同种浑浊的苯酚溶液的两个试管中,分别加入Na2CO3、NaHCO3固体,观察溶液是否变澄清. | 比较H2CO3、苯酚和HCO3-酸性的强弱 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 小苏打可用于治疗胃溃疡 | NaHCO3可与盐酸反应 | Ⅰ对,Ⅱ对,有 |
| B | 向Na2O2的水溶液中滴入酚酞变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
| D | Al(OH)3胶体有吸附性 | 明矾可用作净水剂 | Ⅰ对,Ⅱ对,有 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 电池 | 电解池 | |
| A | H+移向Pb电极 | H+移向Pb电极 |
| B | 每消耗3molPb | 生成1molAl2O3 |
| C | 正极:PbO2+4H++2e-=Pb2++2H2O | 阳极:2Al+3H2O-6e-=Al2O3+6H+ |
| D | Pb电极质量减少 | Pb电极质量不变 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com