
【题目】用电渗析法处理含Na2SO4废水,原理如图所示,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子不能进入中间隔室。

下列叙述正确的是( )。
A.当电路中通过2 mol电子的电量时,会有2mol的H2生成
B.负极区得到NaOH,正极区得到H2SO4
C.负极反应为2H2O-4e-=O2+4H+,负极区溶液pH增大
D.通电后中间隔室的SO42-离子向负极迁移,正极区溶液pH降低
【答案】B
【解析】
A. 根据4mole-~2H2关系式得到,转移电子2mol电子,会有1mol H2生成,故A错误;
B. 直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室,通电时,氢氧根离子在阳极区放电生成水和氧气,考虑电荷守恒,两膜中间的硫酸根离子会进入正极区,与氢离子结合成硫酸;氢离子在阴极得电子生成氢气,考虑电荷守恒,两膜中间的钠离子会进入负极区,与氢氧根离子结合成氢氧化钠,因此负极区得到NaOH,正极区得到H2SO4,故B正确;
C. 正极区为阳极,发生氧化反应,电极反应式为:2H2O4e = O2↑+4H+,生成氢离子,正极区溶液pH降低,故C错误;
D. 阴离子向阳极(即正极区)移动,正极区氢氧根离子放电pH减小,故D错误;
综上所述,答案为B。


科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
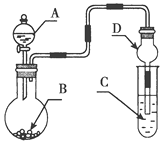
A.若A为浓盐酸,B为KMnO4晶体,C中盛有紫色石蕊溶液,则C中溶液最终呈红色
B.实验仪器D可以起到防止溶液倒吸的作用
C.若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中溶液先产生白色沉淀后沉淀又溶解
D.若A为浓H2SO4,B为Cu,C中盛有澄清石灰水,则C中溶液变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含 CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
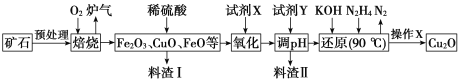
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表:
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀 | 7.5 | 2.7 | 4.8 |
完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)炉气中的有害气体成分是___________,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为___________。
(2)试剂X是H2O2溶液,当试剂X是___________时,更有利于降低生产成本。
(3)加入试剂Y调pH时,pH的调控范围是________。
(4)“还原”步骤中为提高N2H4转化率可采取的措施有_________(填序号)。
a.不断搅拌,使N2H4和溶液充分接触 b.增大通入N2H4的流速
c.减少KOH的进入量 d.减小通入N2H4的流速
(5)写出用N2H4制备Cu2O的化学方程式为_______________
(6)操作X包括烘干,其中烘干时要隔绝空气,其目的是____________。
(7)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式为________
(8)工业上用氨气生产氢氰酸(HCN的反应为:CH4(g)+NH3(g)HCN(g)+3H2(g ) △H>0。其他条件一定,达到平衡时NH3转化率随外界条件X变化的关系如图所示。则X可以是___________(填字母序号)
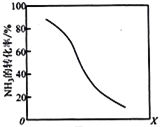
a.温度 b.压强 c.催化剂 d.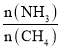
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物 K 是某药物的中间体,合成路线如图所示:
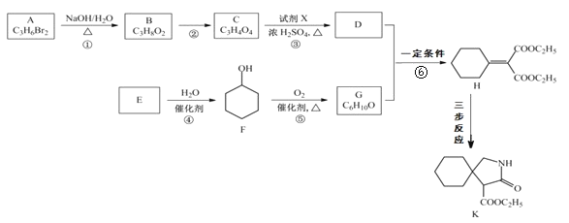
已知:i.R-CN![]() R-CH2-NH2
R-CH2-NH2
ii.R1-NH2+R2COOC2H5![]()
![]() +C2H5OH
+C2H5OH
回答下列问题
(1)A 的名称是_______。
(2)反应①的化学方程式是_____。
(3)反应②的类型是_____。
(4)反应③中的试剂 X是_____。
(5)E 属于烃,其结构简式是_____。
(6)H 中所含的官能团是_____。
(7)反应⑥的化学方程式是_____。
(8)H 经三步反应合成 K:H![]() I→J→K,写出中间产物 I和J的结构简式_____。
I→J→K,写出中间产物 I和J的结构简式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO和O2转化为NO2的反应机理如下:①2NO(g) ![]() N2O2(g)(快) △H1<0,平衡常数K1,②N2O2(g)+O2(g)
N2O2(g)(快) △H1<0,平衡常数K1,②N2O2(g)+O2(g) ![]() 2NO2(g)(慢) △H2<0,平衡常数K2,下列说法正确的是( )
2NO2(g)(慢) △H2<0,平衡常数K2,下列说法正确的是( )
A.2NO(g)+O2(g) ![]() 2NO2(g)的△H=△H1+△H2
2NO2(g)的△H=△H1+△H2
B.2NO(g)+O2(g) ![]() 2NO2(g)的平衡常数K= K1/K2
2NO2(g)的平衡常数K= K1/K2
C.反应①的速率大小决定2NO(g)+O2(g) ![]() 2NO2(g)的反应速率
2NO2(g)的反应速率
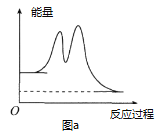
D.反应过程中的能量变化可用图a表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体A的化学式为NH5(也可写为:NH4H),它的所有原子的最外层均满足2个或8个电子的稳定结构。则下列有关说法中错误的是( )
A.它与水反应的化学方程式为NH5 + H2O ═ NH3H2O + H2↑
B.NH5中既有共价键又有离子键
C.NH5的电子式为 
D.1 mol NH5中含有5NA个N﹣H键(NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 C时,H2SO3的pKa1、pKa2(pK= -lgK)分别为1.89、7.20, NH3·H2O的pKb为4.72。常温时,下列指定溶液中粒子物质的量浓度关系正确的是
A.pH=3的H2SO3溶液中,c(HSO3 -) +2c(SO3-)=1 ×10-3 mol·L-1
B.0.1 mol·L-1H2SO3溶液用NaOH溶液滴定至pH =7.20, c( HSO3 ) =2c(SO3- )
C.0.1 mol.L-1H2SO3溶液用氨水滴定至pH=7.0, c(NH4+) =c(HSO3-) +c(SO32- )
D.0.1 mol·L-1NH4HSO3溶液中: c(NH4+ ) >c(H+) >c( NH3·H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制物质的量浓度为0.1 mol·L-1的Na2CO3溶液100 mL时,下列操作正确的是( )
A. 用托盘天平称取1.06 g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 定容时,若仰视,则所配溶液的浓度将偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是
A.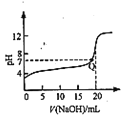 是常温下用0.1000 mol/LNaOH溶液滴定20.000mL 0.l000 mol/L CH3COOH的滴定曲线,说明Q点表示酸碱中和滴定终点
是常温下用0.1000 mol/LNaOH溶液滴定20.000mL 0.l000 mol/L CH3COOH的滴定曲线,说明Q点表示酸碱中和滴定终点
B.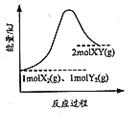 是1mol X2(g)、Imol Y2(g)反应生成2mol XY(g)的能量变化曲线,说明反应物所含化学键的键能总和大于生成物所含化学键的键能总和
是1mol X2(g)、Imol Y2(g)反应生成2mol XY(g)的能量变化曲线,说明反应物所含化学键的键能总和大于生成物所含化学键的键能总和
C.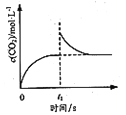 是恒温密闭容器中发生CaCO3(s) = CaO(s)+CO2(g)反应时C(CO2)随反应时间变化的曲线,说明t1时刻改变的条件可能是缩小容器的体积
是恒温密闭容器中发生CaCO3(s) = CaO(s)+CO2(g)反应时C(CO2)随反应时间变化的曲线,说明t1时刻改变的条件可能是缩小容器的体积
D.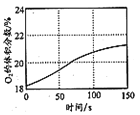 是光照盛有少量氯水的恒容密闭容器时容器内O2的体积分数变化曲线,说明光照氯水有O2生成
是光照盛有少量氯水的恒容密闭容器时容器内O2的体积分数变化曲线,说明光照氯水有O2生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com