
【题目】标准状况下VL氨气溶解在1L水中,所得溶液的密度为ρ g·mL-1,质量分数为ω,物质浓度为c mol·L1,则下列关系中正确的是( )
A. c=![]() B. ω=
B. ω=![]() C. ω=
C. ω=![]() D. ρ=
D. ρ=![]()
科目:高中化学 来源: 题型:
【题目】1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况),它在光照条件下与氯气反应能生成3种不同的一氯代物。则该烃的结构简式是
A. 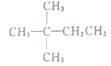 B. CH3CH2CH2CH2CH3
B. CH3CH2CH2CH2CH3
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示。据图判断正确的是
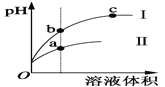
A. Ⅱ为盐酸稀释时pH变化曲线
B. b点溶液的导电性比c点溶液的导电性弱
C. a点KW的值比c点KW的值大
D. 与相同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积,a点比b点大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组在实验室使用软锰矿(主要成分为MnO2)和浓盐酸通过加热制备氧气,并对氯气的性质进行探究。
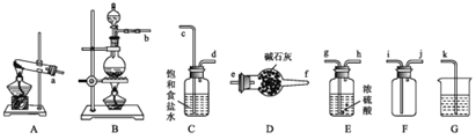
(1)写出实验室制氯气的化学方程式________。欲制取并收集一瓶干燥的氯气,则“制取→收集”的实验装置连接顺序为:____→c→d→_____→i→j→k
(2)装置C中饱和食盐水的作用是______________。
(3)该小组同学对氯气性质进行如下探究:
实验步骤 | 实验结论 |
①将氯气通入到NaCl溶液中,再加入1mL CCl4振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序: 氯、溴、碘 |
②将氯气通入到KBr溶液中,再加入1mL CCl4振荡,静置,观察四氯化碳层颜色 | |
③将氯气通入到KI溶液中,再加入1mL CCl4振荡,静置,观察四氧化碳层颜色 |
该小组的实验设计缺陷是___________,改进的办法是________________。
(4)常温下,高锰酸钾固体和浓盐酸反应也可制得氯气,该反应的离子方程式为______________。
(5)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的质量之比为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.液氨可用作制冷剂B.SO2使湿润的蓝色石蕊试纸变红
C.常温下可以用铁或铝制容器盛装浓硝酸或浓硫酸D.测定某雨水的pH值小于7.0可判断雨水为酸雨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ka 为平衡常数,pKa=﹣lgKa,25℃时,H2A的 pKa1 =1.85,pKa2=7.19。用 0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如下图所示(曲线上的数字为 pH)。下列说法不正确的是

A.a 点所得溶液中;2c(H2A)+c(A2-)=0.002mol
B.b 点所得溶液中:c(H2 A)+c(H+)=c(A2-)+C(OH-)
C.C 点所得溶液中:c(Na+)<3c(HA-)
D.d 点所得溶液中:c(Na+)>c(A2-)>c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾是配制波尔多液的主要原料,常用在树木,花卉的保护上。
(1)基态铜原子的电子排布式为___________。
(2)乙烯氨氧化可以得到丙烯腈(CH2=CH-CN),丙烯腈中各元素的电负性由大到小顺序为____________,1mol丙烯腈分子中含有π键数目为_________。
(3)CN-与N2互为等电子体,写出CN-的电子式______________。
(4)通过X射线衍射发现,胆矾中存在SO42-离子,SO42-离子的VSEPR构型名称为___________,CO32-中心原子的杂化形式为________。
(5)硫酸铜灼烧可以生成一种红色晶体,其结构如图所示为体心立方晶胞,则该化合物的化学式是______;若该晶体中距离最近的铜原子与氧原子直接距离为acm,则晶体密度表达式为_____g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式的叙述正确的是
A. 已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol,则氢气的燃烧热为241.8 kJ/mol
B. 已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C. 已知2C(s)+2O2(g)=2CO2(g) △H1; 2C(s)+O2(g)=2CO(g) △H2;,则△H1>△H2
D. 含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则该反应中和热的热方程式为NaOH(aq)+ HCl(aq)=NaCl(aq)+H2O(l) △H=一57.4kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前世界上新建的金矿中约有80%都采用氧化法提金。某工厂利用锌冶炼渣回收金、银等贵金属的流程如下图所示:

已知:HCN有剧毒,其Ka(HCN)=5×10-10,
Au++2CN-=[Au(CN)2]-平衡常数KB=1×1038
(1)磨矿细度对浸出率的影响如图所示,依据浸出率应选择磨矿细度_____为宜。

(2)生产中用生石灰调节矿泥pH>11.5,其目的之一是阻止溶液中的氰化物转化为HCN而挥发,其作用原理是________________(用离子方程式表示)。
(3)“氰化”环节,是以NaCN溶液浸取调节pH的矿泥,敞口放置,将Au转换为Na[Au(CN)2]。
①其化学方程式为________________。
② “氰化”环节中,金的溶解速率在80℃时达到最大值,但生产中控制反应液的温度在10-20℃,原因是:___________________________(答一点即可)。
③已知2H++[Au(CN)2]-![]() Au++2HCN,该反应的K=____________。
Au++2HCN,该反应的K=____________。
(4)用锌还原NaAu(CN)2生成金,消耗的锌与生成的金的物质的量之比为____________。
(5)氰化物有剧毒,经合理处理就可以基本消除对环境的负面影响。H2O2可消除水中的氰化物(如NaCN),经以下反应实现:NaCN+H2O2+H2O=A+NH3↑。
①生成物A的化学式为______________。
②某废水用H2O2处理40min后,测得剩余总氰为0.16mg/L,除氰率达80%,计算0-40min时间段反应速率v(CN-)=____mg/(L·min)(结果保留两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com