
【题目】已知NaNO2是色泽和味道与NaCl相似的盐,是导致某些建筑工地食物中毒的主要物质,它可与酸性KMnO4溶液发生反应2MnO![]() +5NO
+5NO![]() +a===b+5
+a===b+5![]() +3H2O。下列叙述正确的是( )
+3H2O。下列叙述正确的是( )
A. a是6H+,b是2MnO2
B. 反应过程中溶液的pH减小
C. 还原产物是Mn2+
D. 当有0.1 mol b生成时转移电子数为NA
【答案】C
【解析】
NO![]() 可与酸性KMnO4溶液发生反应2MnO
可与酸性KMnO4溶液发生反应2MnO![]() +5NO
+5NO![]() +a=b+5
+a=b+5![]() +3H2O,依据锰元素守恒及得失电子相等可确定b是2Mn2+,依据电荷守恒,结合酸性条件,故a是6H+,由此可写出对应的离子方程式:2MnO
+3H2O,依据锰元素守恒及得失电子相等可确定b是2Mn2+,依据电荷守恒,结合酸性条件,故a是6H+,由此可写出对应的离子方程式:2MnO![]() +5NO
+5NO![]() +6H+=2Mn2++5NO
+6H+=2Mn2++5NO![]() +3H2O。
+3H2O。
A、因有酸性KMnO4溶液参与反应,故a是6H+,依据锰元素守恒及得失电子相等可确定b是2Mn2+,由此可写出对应的离子方程式:2MnO![]() +5NO
+5NO![]() +6H+=2Mn2++5NO
+6H+=2Mn2++5NO![]() +3H2O,故A错误;
+3H2O,故A错误;
B、根据方程式,反应消耗氢离子,反应过程中溶液的pH增大,故B错误;
C、+7价的Mn得电子,化合价降低为+2价,还原产物为Mn2+,故C正确;
D、由化合价变化情况知,生成0.1 mol Mn2+时转移电子数为0.5NA,故D错误。
故选C。


科目:高中化学 来源: 题型:
【题目】如图是一种表示集合的图案,该图案中由左到右分别写了H2O、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分由左到右A、B、C、D为其相应的分类依据代号。请回答下列问题:
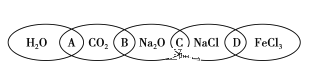
(1)请将分类依据代号填入相应的括号内:
(_____)两种物质都是非金属氧化物
(_____)两种物质都是钠的化合物
(_____)两种物质中一种是酸性氧化物,一种是碱性氧化物
(_____)两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入上图中某种物质M的水溶液,继续煮沸可制得一种红褐色胶体。
①物质M的化学式为____。
②证明有红褐色胶体生成的最常用的实验操作是____。
③生成该胶体的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PbO2、KMnO4、Cl2、FeCl3、CuCl2的氧化性依次减弱。下列反应不可能发生的是
A. Cu+2Fe3+==Cu2++2Fe2+ B. 10Cl-+2MnO![]() +16H+=2Mn2++5Cl2↑+8H2O
+16H+=2Mn2++5Cl2↑+8H2O
C. Cu+Cl2![]() CuCl2 D. 5Pb2++2MnO
CuCl2 D. 5Pb2++2MnO![]() +2H2O=5PbO2↓+2Mn2++4H+
+2H2O=5PbO2↓+2Mn2++4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如图:
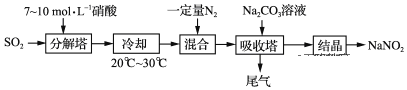
已知:Na2CO3+NO+NO2=2NaNO2+CO2
(1)“分解塔”中SO2从塔底进入,硝酸从塔顶喷淋,其目的是____。
(2)“分解塔”中的温度不宜过高,其原因是____。
(3)按一定计量比在“分解塔”中通SO2和喷入硝酸,若反应后生成的NO与NO2物质的量之比恰好1:1,则“分解塔”中发生反应的化学方程式为____。
(4)为提高氮氧化物的转化率,可向“尾气”中通入一定量的____气体,再通入“吸收塔”中,实现循环吸收。
(5)“吸收塔”所得溶液中除含有NaNO2、NaNO3和少量Na2CO3外,还含有的溶质为___(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验、现象、所对应的离子方程式不正确的是( )
选项 | 实验 | 现象 | 离子方程式 |
A | 将稀硫酸滴加到淀粉-KI溶液中 | 在空气中放置一段时间后溶液呈蓝色 | 4H++4I-+O2===2I2+2H2O |
B | 向FeBr2溶液中通入少量Cl2 | 溶液由浅绿色变棕黄色 | 2Fe2++Cl2===2Fe3++2Cl- |
C | 向氯水中加入适量NaOH溶液 | 溶液由黄绿色变为无色 | Cl2+2OH-===Cl-+ClO-+H2O |
D | 将Na2S加入到滴有酚酞的KCl溶液中 | 溶液由无色变为红色 | S2-+2H2O===H2S+2OH- |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某含有SO![]() 、SiO
、SiO![]() 、CO
、CO![]() 、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断不正确的是( )
、Br-、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断不正确的是( )
A. 整个过程共发生2个氧化还原反应
B. 所有阴离子的浓度都发生了变化
C. 溶液的颜色发生了变化
D. 反应过程中既有气体产生,也有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种具有咸味、有毒,且价格比食盐(NaCl)便宜的工业用盐,常被误作食盐使用,导致多起中毒事故发生。它的部分性质见下图,下列说法错误的是
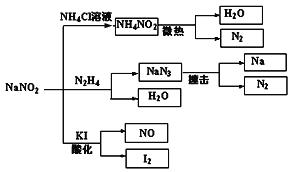
A. 上图所涉及到的化学反应都是氧化还原反应
B. N2H4极易溶于水,因为它是极性分子且与水分子之间易形成氢键
C. NaNO2与N2H4生成NaN3的反应方程式为:NaNO2 + N2H4 = NaN3 + 2H2O
D. 可用淀粉碘化钾试纸和食醋鉴别食盐(NaCl)与亚硝酸钠(NaNO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向1L 0.1 mol·L-1一元弱酸HR溶液中缓慢加入一元碱MOH(加入MOH过程中溶液的温度和溶液的体积变化忽略不计),lg![]() 随溶液pH变化的部分图像如下图所示[已知:Kb(MOH)>Ka(HR)],下列叙述中正确的是( )
随溶液pH变化的部分图像如下图所示[已知:Kb(MOH)>Ka(HR)],下列叙述中正确的是( )
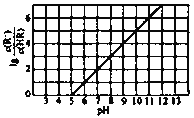
A. 常温下,Ka(HR)=1×10-6
B. 常温下,0.1 mol·L-1的HR溶液的pH约为3
C. 当HR与MOH恰好完全反应时,溶液中c(R-)>c(M+)
D. 当溶液呈中性时,c(HR)=c(R-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】火法炼铜是目前世界上最主要的冶炼铜的方法,其产量可占到铜总产量的85%以上,火法炼铜相关的方程式有
Cu2S(s)+O2(g)=2Cu(s)+SO2(g) △H1=-271.4kJ/mol 反应①
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g) △H2=+123.2kJ/mol 反应②
(1)Cu2S(s)在空气中煅烧生成Cu2O(s)和SO2(g)的热化学方程式是___。
(2)火法炼铜所得吹炼烟气中SO2含量较高,该烟气在工业上可直接用于生产硫酸,从绿色化学角度考虑其优点有____(任写一条)。
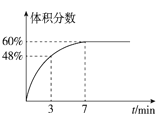
(3)在2L的恒温密闭容器中通入5mol氧气并加入足量Cu2S发生反应①(不考虑其它反应),容器中的起始压强为akPa,反应过程中某气体的体积分数随时间变化如图所示,反应前3min平均反应速率v(SO2)=___mol/(L·min),该温度下反应的平衡常数KP=___(KP为以分压表示的平衡常数)。若保持温度不变向平衡体系中再通入1mol氧气,达到新平衡后氧气的体积分数___(填“大于”“小于”或“等于”)原平衡时氧气的体积分数。
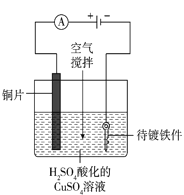
(4)工业上电镀铜的装置如图所示,阳极产物除Cu2+外还有部分Cu+,部分Cu+经过一系列变化会以Cu2O的形式沉积在镀件表面,导致镀层不够致密、光亮。电镀过程中用空气搅拌而不是氮气搅拌的原因是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com