
【题目】下列各组物质中,互为同位素的是
A.O2和O3B.H和D
C.H2O和D2OD.金刚石和石墨
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增多。其中A、B、C都是能层数为2的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。E的核外电子排布中有6个未成对电子,是同周期中最多的,ECl3能与B、C的氢化物形成六配体的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界。试用相应的元素符号或式子填空:
(1)写出元素的名称 A ___________ E ____________;
(2)A、B、C的第一电离能由小到大的顺序为 __________;B的氢化物分子的空间构型为 _________ 。
(3)化合物AC2与一种由B、C组成的化合物X互为等电子体,则X的化学式为 ____________;完全由B的原子组成的某粒子与AC2也属于等电子体,该粒子的化学式为 _____ ,其空间构型为 __________ 。
(4)ECl3形成的配合物的化学式为 ____________________________ ;
(5)D的单质在AC2中可以燃烧并一种白色固体和一种黑色固体,该反应的化学方程式为 ________ 。
(6)与E同周期,且最外层电子排布相同的元素有___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】COCl2(g)![]() CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0,当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高COCl2转化率的是( )
A. ①②④ B. ①④⑥ C. ②③⑤ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2的燃烧热为ΔH=-285.8 kJ·mol-1,CO的燃烧热为ΔH=-282.8 kJ·mol-1;现有H2和CO组成的混合气体5.6 L(标准状况),经充分燃烧后,放出总热量为71.15 kJ,并生成液态水。下列说法正确的是
A. CO燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-282.8 kJ·mol-1
B. H2燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(g) ΔH=-571.6 kJ·mol-1
C. 燃烧前混合气体中CO的体积分数为60%
D. 燃烧后的产物全部与足量的过氧化钠作用可产生0.125 mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已经298K、101kPa时,下列说法不正确的是
反应1:4Fe(s)+3O2(g) = 2Fe2O3 (s) ΔH1 =-1648 kJ/mol
反应2:C(s) + O2 (g) = CO2 (g) ΔH2 = -393 kJ/mol
反应3:2Fe(s)+2C(s) +3O2(g) = 2FeCO3(s) ΔH3 =-1480 kJ/mol
反应4:2FeCO3(s) +1/2O2(g) =2CO2(g) +Fe2O3(s) ΔH4
A. 上述反应1.2.3.4在热力学上自发趋势都很大
B. 反应1和3在较低温度下能自发反应,反应4是熵增反应
C. 自发反应代表反应一定能发生,可以判断过程的方向,但不能确定过程发生的速率
D. 反应1表示铁在氧气中燃烧的热化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是( )

A. (CH3)3COH (气)B. NH3C. CH3CH2CH2OH(气)D. CO和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.同种元素的质子数必定相同
B.不同元素原子的质量数必定不同
C.原子核都是由质子和中子构成的
D.凡是核外电子数相同的微粒必定属于同一元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基法提纯粗镍涉及的两步反应依次为:
(1)Ni(s)+4CO(g)![]() Ni(CO)4(g) ΔH < 0 (2)Ni(CO)4(g)
Ni(CO)4(g) ΔH < 0 (2)Ni(CO)4(g) ![]() Ni(s)+4CO(g),下列说法正确的是
Ni(s)+4CO(g),下列说法正确的是
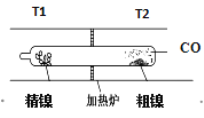
A. T1<T2
B. 可通过高压的方式提高反应(1)中Ni(CO4)的产率
C. 反应(2)平衡后,降低温度,CO浓度减小
D. 升温,反应(1)的气体平均相对分子质量增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,把0.5mol N2O4气体通入体积为5L的恒容密闭容器中,立即出现红棕色。反应进行到2秒时,NO2的浓度为0.02 mol/L。在60秒时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是( )
A. 前2秒,以N2O4的浓度变化表示的平均反应速率为0.01mol/(L·s)
B. 在2秒时体系内的压强为开始时的1.2倍
C. 在平衡时体系内含N2O40.20mol
D. 平衡时,如果再充入一定量N2O4, 则可提高N2O4的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com