
【题目】已经298K、101kPa时,下列说法不正确的是
反应1:4Fe(s)+3O2(g) = 2Fe2O3 (s) ΔH1 =-1648 kJ/mol
反应2:C(s) + O2 (g) = CO2 (g) ΔH2 = -393 kJ/mol
反应3:2Fe(s)+2C(s) +3O2(g) = 2FeCO3(s) ΔH3 =-1480 kJ/mol
反应4:2FeCO3(s) +1/2O2(g) =2CO2(g) +Fe2O3(s) ΔH4
A. 上述反应1.2.3.4在热力学上自发趋势都很大
B. 反应1和3在较低温度下能自发反应,反应4是熵增反应
C. 自发反应代表反应一定能发生,可以判断过程的方向,但不能确定过程发生的速率
D. 反应1表示铁在氧气中燃烧的热化学方程式
【答案】CD
【解析】
根据盖斯定律知,反应4=反应1×![]() +反应2×2-反应3=(-1 648×
+反应2×2-反应3=(-1 648×![]() -393×2+1480) kJ·mol-1=-130 kJ·mol-1,反应1、2、3、4均为放热反应,以此分析解答。
-393×2+1480) kJ·mol-1=-130 kJ·mol-1,反应1、2、3、4均为放热反应,以此分析解答。
A.题述反应1、2、3、4都是放热反应且放出的热量较多,在热力学上自发趋势很大,故A项正确;
B.反应1和3都是放热的熵减反应,根据复合判据ΔH-T·ΔS<0知,在较低温度下能自发进行,反应4是气体分子数增大的反应,它是熵增反应,B项正确;
C. 化学反应的自发性只能判断过程的方向,不能确定反应是否一定会发生和过程发生的速率,故C项错误;
D.铁在氧气中燃烧只生成四氧化三铁,不是氧化铁,故D项错误。
故选CD。


科目:高中化学 来源: 题型:
【题目】化学是以实验为基础的科学,以下实验是高一学生必须掌握的基本实验,请根据实验内容完成下列问题;
(1)下图是从海带中提取碘单质的过程:
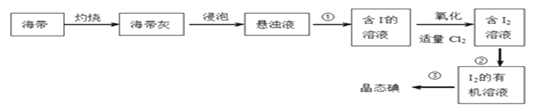
①进行实验①的操作名称是:_________________。
②在进行实验②的过程中,可以选择的有机溶剂是____________。
A.乙醇 B.四氯化碳 C.苯 D. 乙酸
③从I2的有机溶液中提取碘的装置如图所示,仪器a的名称为:_______。
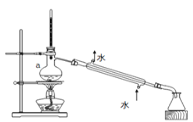
④向含I-的溶液中加入适量氯气发生反应的离子方程式为:__________________________。
(2)下图是实验室制取乙酸乙酯的实验装置,回答下列问题:
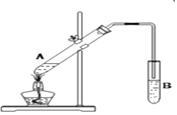
①在A试管中加入试剂的顺序是___________ (填以下字母序号)。
a.先浓硫酸再乙醇后乙酸 b.先浓硫酸再乙酸后乙醇 c.先乙醇再浓硫酸后乙酸
②在试管B中常加入_______________ 来接收乙酸乙酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的实验操作中所用仪器合理的是
A.用25 mL的碱式滴定管量取14.80 mL NaOH溶液
B.用100 mL量筒量取5.2 mL盐酸
C.用托盘天平称取25.20 g氯化钠
D.用150 mL容量瓶配制50 mL 0.1 mol/L盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NA代表阿伏加德罗常数的数值,则关于热化学方程式C2H2(g)+![]() O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法中,正确的是( )
O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ·mol-1的说法中,正确的是( )
A. 转移10NA个电子时,该反应放出1300 kJ的能量
B. 生成NA个液态水分子时,吸收1300 kJ的能量
C. 有2NA个碳氧共用电子对生成时,放出1300 kJ的能量
D. 有10NA个碳氧共用电子对生成时,放出1300 kJ的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在冰醋酸加水稀释的过程中,溶液的导电能力(I)随着加入水的体积V变化的曲线如图所示。下列说法正确的是( )
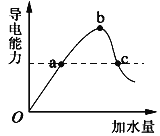
A.a、c两点pH不同
B.向c溶液中加水,溶液中所有离子浓度都减小
C.误用湿润的pH试纸测b点pH结果偏大
D.![]() b点大于c点
b点大于c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应 2SO2(g) + O2(g)![]() 2SO3(g)(正反应放热),相关数据如下,下列说法正确的是( )
2SO3(g)(正反应放热),相关数据如下,下列说法正确的是( )
容器 1 | 容器 2 | 容器 3 | |
反应温度 T/K | 700 | 700 | 800 |
反应物投入量 | 2molSO2、 1molO2 | 4molSO3 | 2molSO2、 1molO2 |
平衡ν正(SO2 )/mol·L-1·s-1 | ν1 | ν2 | ν3 |
平衡 c(SO3 )/ mol·L-1 | c1 | c2 | c3 |
平衡体系总压强 p/Pa | p1 | p2 | p3 |
物质的平衡转化率ɑ | α1(SO2) | α2(SO3) | α3(SO2) |
平衡常数 K | K1 | K2 | K3 |
A. ν1<ν2,c2<2c1 B. K1>K3,p2>2p3
C. ν1< ν3,α1(SO2) > α3(SO2) D. c2>2c3,α2(SO3) +α3(SO2)<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)真空碳热还原-氧化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g) △H=akJ·mol-1
3AlCl(g)═2Al(l)+AlCl3(g) △H=bkJ·mol-1
反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=________kJ·mol-1(用含a、b的代数式表示);
(2)已知 2SO2(g)+O2(g)=2SO3(g)△H反应过程的能量变化如图所示,已知1mol SO2(g)氧化为1mol SO3放出99kJ的热量,请回答下列问题:
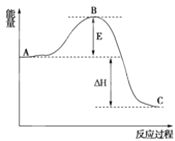
①图中A分别表示______________;
②E的大小对该反应的反应热_________(填“有”或“无”)影响;
③该反应通常用V2O5作催化剂,加V2O5会使图中B点 __________(填“升高”“降低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于平衡体系mA(g)+nB(g)![]() pC(g)+qD(g) ΔH<0。下列结论中错误( )
pC(g)+qD(g) ΔH<0。下列结论中错误( )
A. 若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n<p+q
B. 若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n
C. 若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a
D. 若A为固体,则增大压强,平衡向逆向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com