
【题目】一定温度下,在一容积固定的密闭容器中,加入1molCO2、2molH2进行反应CO(g)+H2O(g)![]() CO2(g)+H2(g),下列情况能说明反应一定达到平衡状态的是( )
CO2(g)+H2(g),下列情况能说明反应一定达到平衡状态的是( )
A.容器内混合物的相对分子质量不再随时间改变
B.生成1molH—H键的同时消耗1molCO2
C.容器内的气体总压强不再随时间改变
D.容器内CO2与H2的浓度相等
【答案】B
【解析】
根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态。
A.混合气体的平均相对分子质量是混合气体的质量和混合气体的总物质的量的比值,混合气体的质量和总物质的量均始终不变,所以容器内混合气体的相对分子质量始终不变,A项错误;
B.生成1molH—H键的同时消耗![]() 说明正逆反应速率相等,反应达到平衡状态,B项正确;
说明正逆反应速率相等,反应达到平衡状态,B项正确;
C.反应前后气体体积不变,容器内的气体总压强不再随时间改变不能说明反应达到平衡状态,C项错误;
D.根据方程式可知,二氧化碳和氢气均是生成物,容器内![]() 与
与![]() 的浓度始终相等,不能说明反应达到平衡状态,D项错误;
的浓度始终相等,不能说明反应达到平衡状态,D项错误;
故答案选:B。


科目:高中化学 来源: 题型:
【题目】用H2O2和H2SO4的混合溶液可溶出印刷电路板中的铜,其热化学方程式为Cu(s)+H2O2(l)+2H+(aq)===Cu2+(aq)+2H2O(l) ΔH已知①Cu(s)+2H+(aq)===Cu2+(aq)+H2(g) ΔH1=+64 kJ·mol-1②2H2O2(l)===2H2O(l)+O2(g) ΔH2=-196 kJ·mol-1③H2(g)+1/2O2(g)===H2O(l) ΔH3=-286kJ·mol-1。下列说法不正确的是
A. 反应①可通过铜作电极电解稀H2SO4的方法实现
B. 反应②在任何条件下都能自发进行
C. 若H2(g)+1/2O2(g)===H2O(g) ΔH4,则ΔH4<ΔH3
D. ΔH=-320 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)单质钠是一种______色的金属,密度比水______![]() 大
大![]() 小
小![]() ,钠在自然界中以______
,钠在自然界中以______![]() 化合
化合![]() 游离
游离![]() 态存在;金属钠与水反应的化学方程式:______,金属钠在空气中燃烧生成______色的______
态存在;金属钠与水反应的化学方程式:______,金属钠在空气中燃烧生成______色的______![]() 化学式
化学式![]() ,其生成物与水反应的化学方程式:______。
,其生成物与水反应的化学方程式:______。
(2)氯气是一种______色的气体,密度比空气______,______溶于水,并可以和水发生反应,写出其反应的化学方程式:______,实验室中用______溶液![]() 化学式
化学式![]() 吸收多余的氯气。
吸收多余的氯气。
铁丝在氯气中燃烧的化学方程式:______。漂白粉是______和______![]() 化学式
化学式![]() 的混合物,是利用氯气与氢氧化钙反应制成的,写出其反应的方程式:______。
的混合物,是利用氯气与氢氧化钙反应制成的,写出其反应的方程式:______。
(3)现有物质:①氧化镁②硫酸铜③碳酸钙④金属钠⑤氯气⑥氢气⑦硫酸⑧氯水⑨二氧化硫⑩氧化钠![]() 二氧化硅
二氧化硅![]() 次氯酸
次氯酸![]() 漂白粉
漂白粉
按下列标准进行归类![]() 填序号
填序号![]() 混合物______酸______盐______单质______碱性氧化物______酸性氧化物______。
混合物______酸______盐______单质______碱性氧化物______酸性氧化物______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾可用作除草剂、净水剂或抗贫血药等。某研究小组同学采用硫铁矿焙烧后的烧渣(主要成分为Fe2O3、Al2O3和SiO2,不考虑其他杂质)制备绿矾,流程如下:
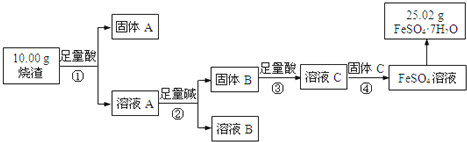
已知:固体B为红褐色固体,固体C为用途最广泛的金属,请回答:
(1)①~③所涉及的实验操作方法中,用到过滤的是__________(填序号);
(2)③中所发生反应的离子方程式是____;
(3)下列说法正确的是__________;
a①中可选用盐酸,③中应选择硫酸
b溶液B中含有OH-、SiO32-、AlO2-等阴离子
c④中发生了氧化还原反应
(4)如何检验溶液C中的阴离子?___________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mol固体A置于体积不变的真空密闭容器中(固体试样体积忽略不计),在恒定温度下使其分解:A(s)![]() 2B(g)+C(g),下列可以判断该反应已达到化学平衡状态的是( )
2B(g)+C(g),下列可以判断该反应已达到化学平衡状态的是( )
A.反应速率:vB(正)=vC(逆)
B.B的体积分数不变
C.气体的密度保持不变
D.混合气体的平均摩尔质量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是一种治疗艾滋病的新药(结构简式见图),已知M的分子中-NH-COO-基团(除H外)与苯环在同一个平面内,关于M的以下说法正确的是
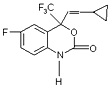
A.该物质易溶于水
B.M能发生缩聚反应
C.M分子内至少有15个原子在同一个平面上
D.M的分子式为C13H22O2NF4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关滴定的说法正确的是( )
A. 用25mL滴定管进行中和滴定时,用去标准液的体积为21.7mL
B. 用标准的KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体KOH中有NaOH杂质,则结果偏低
C. 用C1mol/L酸性高锰酸钾溶液滴定V2mL未知浓度的H2C2O4溶液,至滴定终点用去酸性高猛酸钾溶液体积为V1mL,则H2C2O4溶液的浓度为![]() mol/L
mol/L
D. 用未知浓度的盐酸滴定已知浓度的NaOH溶液时,若读取读数时,滴定前仰视,滴定到终点后俯视,会导致测定结果偏低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 表示阿伏加德罗常数的值,下列叙述中正确的是( )
表示阿伏加德罗常数的值,下列叙述中正确的是( )
A.常温常压下,20g![]() 和足量的金属钠反应产生气体的分子数为
和足量的金属钠反应产生气体的分子数为![]()
B.1mol![]() 与足量的水反应,转移的电子数为
与足量的水反应,转移的电子数为![]()
C.![]() 个
个![]() 分子在标准状况下的体积为
分子在标准状况下的体积为![]() L
L
D.![]() 时,
时,![]() 的
的![]() L
L![]() 溶液中含有的
溶液中含有的![]() 数目为
数目为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明代《天工开物》记载了“火法”冶炼锌的方法:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷淀,毁罐取出,…,即倭铅也”,现代工业开发了用NH3—NH4Cl水溶液浸出氧化锌烟灰(主要成分为ZnO 、少量Pb、CuO和As2O3)制取高纯锌的工艺流程如图所示。
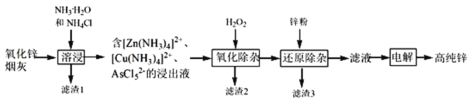
请回答下列问题:
(1)《天工开物》中炼锌的方法中“泥封”的目的是____________。
(2)滤渣1的主要成份分别是_______(填化学式),“过滤”用到的玻璃仪器是__________。
(3) “溶浸”时,氧化铜参与反应的相关离子方程式是________;“溶浸”时可以适当升高温度,但不宜过高,其原因是________________。
(4) “氧化除杂”的目的是将AsCl52-转化为As2O5胶体,再经吸附聚沉除去,溶液始终接近中性,该反应的离子方程式是_____________________。
(5) “电解”含 [Zn(NH3)4]2+的溶液,阴极放电的电极反应式是_________。阳极区产生一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是_______(写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com