
【题目】下列描述,其因果关系成立的是
A.因为NH3的水溶液可以导电,所以NH3是电解质
B.因为SO2可以使溴水褪色,所以SO2具有漂白性
C.因为某碱性溶液的焰色呈黄色,所以其溶质为NaOH
D.因为电解质溶于水后电离为离子,所以电解质在溶液中的反应实质是离子反应
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】根据下图A、B、D、E的转化关系,回答下列问题:
(1)写出A、D的名称:A , D。
(2)写出B→A的化学方程式:。
(3)写出下列反应的离子方程式:A→E:;E→D:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验题
(1)分别取Wg钠、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是。
(2)分别取0.1mol钠、铁、铝与足量的盐酸反应,在相同条件下产生氢气的体积比是。
(3)若产生相同物质的量的氢气,所需钠、铁、铝的质量比是。
(4)若产生相同体积(同温同压)的氢气,所需钠、铁、铝三种金属的物质的量之比是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 1 mol氧原子的质量是16 g· mol-1
B. 钠离子的摩尔质量是22 g· mol-1
C. 二氧化碳的摩尔质量是44 g· mol-1
D. 氢的摩尔质量是2 g· mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液有Cl-、![]() 、
、![]() , 要求依次检验出这三种离子,请完成下列实验设计:
, 要求依次检验出这三种离子,请完成下列实验设计:
检验离子 | 所加试剂 | 实验现象 | 离子方程式 |
① | 稀硝酸 | ||
② | 产生白色沉淀 | ||
③ Cl- | 产生白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,可以加快反应速率的是( )
A. 锌与稀硫酸反应时,加入少量CuSO4固体
B. 钠与水反应时,增加水的量
C. 用18mol/L的硫酸溶液代替2mol/L硫酸溶液常温下与铝反应
D. 锌与稀硫酸反应时,加入少量醋酸钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫COS的结构与CO2相似,广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。羰基硫的氢解反应和水解反应是两种常用的脱硫方法,其反应式分别为:
①氢解反应:COS(g)+H2(g) ![]() H2S(g)+ CO(g) △H=+7 kJ/mol
H2S(g)+ CO(g) △H=+7 kJ/mol
②水解反应: COS(g)+H2O(g) ![]() H2S(g)+ CO2(g) △H = ?
H2S(g)+ CO2(g) △H = ?
已知反应中相关的化学键键能数据如下:

回答下列问题:
(1)羰基硫的结构式为:___________,
(2)已知热化学方程式CO(g)+H2O(g) ![]() H2(g)+ CO2(g) △H3 则△H3 =__________kJ/mol。
H2(g)+ CO2(g) △H3 则△H3 =__________kJ/mol。
(3)COS的氢解反应的平衡常数K与温度T具有如下的关系式 ![]() ,式中a和b均为常数。
,式中a和b均为常数。
①如图中,表示COS氢解反应的直线为__________;


②一定条件下,催化剂A和B对COS的氢解反应均具有催化作用,相关数据如表所示:
则a1____a2 (填“>”或“<”或“=”)。
③某温度下,在体积不变的容器中,若COS和H2的起始体积比为1:V,平衡后COS和H2的体积比为1:10V,则此温度下该反应的化学平衡常数K=_________。(关于V的表达式)
(1)COS完全燃烧会生成大气污染物SO2。目前,科学家正在研究一种以乙烯作为还原剂的脱硫(SO2)方法,其脱硫机理如图2,脱硫率与温度、负载率(分子筛中催化剂的质量分数)的关系如图3。

①该脱硫原理总反应的化学方程式为_________________________________________;
②据图3,为达到最佳脱硫效果,应采取的具体反应条件是________________________;
③根据a曲线在450℃以上的变化趋势,分析可能的原因是:______________________。
(5)为测定某工厂烟道气中SO2的含量,现将16.00 L烟道气缓慢通过1.00 L水,设SO2完全被吸收,且溶液体积不变。取出20.00 mL溶液,用1.18×10-3mol·L-1的饱和碘水与之反应,若恰好完全反应时消耗碘水19.07 mL,则该厂烟道气中SO2的含量为________________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对于下列反应:2SO2+O2 2SO3,如果 2min 内 SO2 的浓度由 6mol/L 下降为 2mol/L,那么,用 SO2 浓度变化来表示的化学反应速率为______,用 O2 浓度变化来表示的反应速率为______。如果开始时 SO2 浓度为 4mol/L,2min 后反应达平衡,若这段时间内v(O2)为 0.5mol/(Lmin),那么 2min 时 SO2 的浓度为______。
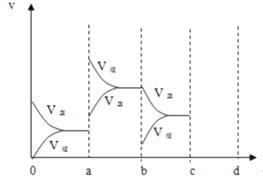
(2)下图表示在密闭容器中反应:2SO2+O2![]() 2SO3 ΔH<0 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab 过程中改变的条件可能是___________;bc 过程中改变的条件可能是____________;若在 c 时刻增大压强,画出 c~d 时刻反应速率变化情况____________。
2SO3 ΔH<0 达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab 过程中改变的条件可能是___________;bc 过程中改变的条件可能是____________;若在 c 时刻增大压强,画出 c~d 时刻反应速率变化情况____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com