
����Ŀ����ǰ��ԴΣ����һ��ȫ�������⣬��Դ������Ӧ����ԴΣ������Ҫ�ٴ롣
��1������������������Դ����Դ����������________(����ĸ)��
A������̫���ܡ�ˮ�ܡ����ܵ�����Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ��
B���о���ú�������¼�������߲��������㹤ҵ�����Ŀ��ٷ�չ
C��������չũ���������������Ľո�ת��Ϊ����Ч����Դ
D��������Դ���ġ�������Դ���ظ�ʹ�ú���Դ��ѭ������

��2�����ʯ��ʯī��Ϊ̼��ͬ�������壬��������������ʱȼ������һ����̼������������ʱ���ȼ�����ɶ�����̼����Ӧ�зų���������ͼ��ʾ������ͨ��״���£����ʯ��ʯī��Ƚϣ�_________(�� �����ʯ������ʯī��)���ȶ���ʯī��ȼ������H��______________��
��3��N2��O2�����л�ѧ���ļ��ֱܷ���946 kJ/mol��497kJ/mol����֪��N2(g)��O2(g)��2NO(g) ��H����180.0 kJ/mol��NO�����л�ѧ���ļ���Ϊ_____��
��4���ۺ������й���Ϣ����д����CO��ȥNO��������Ⱦ������Ȼ�ѧ����ʽ��_______________��
���𰸡�Bʯī��393.5 kJ��mol��1631.5 kJ/mol2NO(g)��2CO(g)��N2(g)��2CO2(g) ��H����746.0 kJ��mol��1
��������
��1��ֻҪ�ܼ��ٻ�ʯȼ�ϵ���Դ�����ö���������Դ��������B����������ú��ʯ�ͺ���Ȼ�������ܼ��ٻ�ʯȼ�ϵ����ã��ʴ���A��C��D�ܼ��ٻ�ʯȼ�ϵ����ã���ȷ����ѡACD��
��2��ͼ��������ʯ��������ʯī������Խ��Խ�ȶ�������˵��ʯī�ȶ���ͼ�����1molʯī��ȫȼ������1mol������̼�ų�������Ϊ393.5kJ����ʯī��ȼ����Ϊ��H=-393.5kJmol-1��
��3��![]() ��Ӧ����ܺ�-��������ܺ�������N2(g)��O2(g)==2NO(g)����H����180.0 kJ/mol����946 kJ/mol+ 497kJ/mol-2Q(N-O)= 180.0 kJ/mol���Q(N-O)= 631.5kJ/mol��
��Ӧ����ܺ�-��������ܺ�������N2(g)��O2(g)==2NO(g)����H����180.0 kJ/mol����946 kJ/mol+ 497kJ/mol-2Q(N-O)= 180.0 kJ/mol���Q(N-O)= 631.5kJ/mol��
��4����֪��C(ʯī,![]() ��C(ʯī,
��C(ʯī,![]() ��
��![]() ���ɸ�˹����:����ʽ�١�2-�ڡ�2-�۵�
���ɸ�˹����:����ʽ�١�2-�ڡ�2-�۵�![]()
![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о�С���Լױ�Ϊ��Ҫԭ�ϣ���������·�ߺϳ�ҽҩ�м���F��Y�� 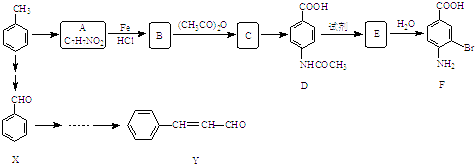
��֪�� ![]()
![]()
![]() ��2CH3CHO
��2CH3CHO ![]()
![]()
��ش��������⣺
��1�������й�F��˵����ȷ���� ��
A.����ʽ��C7H7NO2Br
B.�������
C.�ܷ���ȡ����Ӧ�����۷�Ӧ
D.1mol��F�����Ժ�2mol NaOH��Ӧ
��2��C��D�ķ�Ӧ������ ��
��3��B��C�Ļ�ѧ����ʽ�� �� �ںϳ�F�Ĺ����У�B��C���費��ʡ�ԣ������� ��
��4��д��ͬʱ��������������A��ͬ���칹��Ľṹ��ʽ �� ��Ҫ��д��3�֣� �ٱ�����ֻ�����ֲ�ͬ��ѧ��������ԭ�ӣ� �ڷ����к��� ![]() ��
��
��5����X����ϩΪԭ�Ͽɺϳ�Y������ƺϳ�·�ߣ����Լ����ܼ���ѡ���� ע���ϳ�·�ߵ���д��ʽ��������ʾ������ͼ��
CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3 �� ��
CH3COOCH2CH3 �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ͨ���绯ѧԭ�����������γ�����Ĥ������俹��ʴ����������ԭ����ͼ��ʾ������˵������ȷ����

A. ̼������ͭ�����棬�������Ǵ��ݵ���
B. ͨ��һ��ʱ�����Һ��pH��С
C. ͨ�����ӱ�ǿ�ƴ�̼��������Ƭʹ�������γ�����Ĥ
D. ��ͨ�����ڻ�������������������Ĥ���γ��ٶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������NH4I�����ܱ������У���һ���¶��·������з�Ӧ����NH4I(s)![]() NH3(g)��HI(g)����2HI(g)
NH3(g)��HI(g)����2HI(g) ![]() H2(g)��I2(g)�ﵽƽ��ʱ��c(H2)��1 mol��L��1��c(HI)��4 mol��L��1������¶��·�Ӧ�ٵ�ƽ�ⳣ��Ϊ( )
H2(g)��I2(g)�ﵽƽ��ʱ��c(H2)��1 mol��L��1��c(HI)��4 mol��L��1������¶��·�Ӧ�ٵ�ƽ�ⳣ��Ϊ( )
A. 36 B. 24 C. 16 D. 9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����Ȼ�ѧ����ʽ�У���ѧ��Ӧ�ġ�Hǰ�ߴ��ں��ߵ��ǣ�������
��C��s��+O2��g���TCO2��g������H1 C��s��+ ![]() O2��g���TCO��g������H2
O2��g���TCO��g������H2
��S��s��+O2��g���TSO2��g������H3 S��g��+O2��g���TSO2��g������H4
��H2��g��+ ![]() O2��g���TH2O��l������H5 2H2��g��+O2��g���T2H2O��l������H6
O2��g���TH2O��l������H5 2H2��g��+O2��g���T2H2O��l������H6
��CaCO3��s���TCaO��s��+CO2��g������H7 CaO��s��+H2O��l���TCa��OH��2��s������H8 ��
A.��
B.��
C.�ڢۢ�
D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�ƻ�1mol H��H����1mol I��I����1mol H��I���ֱ���Ҫ���յ�����Ϊ436kJ��151kJ��299kJ�����������͵ⵥ�ʷ�Ӧ����2mol HI��Ҫ�ų�kJ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��˵����ȷ����(����)
A. �����ȼ����Ϊ��H����890 kJ��mol��1 �������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)��2O2(g)=CO2(g)��2H2O(g)����H����890 kJ�� mol��1
B. 500 �桢30 MPa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3 kJ�����Ȼ�ѧ����ʽΪ��N2(g)��3H2(g)![]() 2NH3(g)����H����38.6 kJ��mol��1
2NH3(g)����H����38.6 kJ��mol��1
C. ��֪��H2(g)��F2(g)=2HF(g)����H����270 kJ��mol��1 ����1 mol������1 mol������Ӧ����2 molҺ̬������ų�������С��270 kJ
D. ��C����ͬ�����£�2 mol HF���������С��1 mol������1 mol�����������ܺ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л���AΪԭ�Ͽ��Ժϳ�ҩ��SERMs���м���E����ϳ�·��������

�ش�����������
��1��A�Ļ�ѧ����Ϊ_________��E�й����ŵ�����Ϊ________________��
��2��A��B�ķ�Ӧ����Ϊ________��B��C�ķ�Ӧ����Ϊ________________��
��3��B�Ľṹ��ʽΪ_________________��
��4����D����E�Ļ�ѧ����ʽΪ__________________��
��5����ȡ�������廯����W��E��ͬ���칹������������������W����___��(���������칹)��
��1molW��������������Һ����������Ӧ����4molAg
������FeCl3��Һ������ɫ��Ӧ
���к˴Ź�������Ϊ�����Ľṹ��ʽΪ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�ص�ԭ�ӽṹ���������ʺ����ڱ��е�λ�ã�����˵����ȷ���ǣ� ��
A.Ԫ��ԭ�ӵ���������������Ԫ�ص�����ϼ�
B.�����ԭ���У�����˽Ͻ����������˶��ĵ��ӵ������ϸ�
C.P,S,Cl�õ�������������������Ӧˮ��������Ծ�������ǿ
D.Ԫ�����ڱ���λ�ڽ����ͷǽ����ֽ��߸�����Ԫ�����ڹ���Ԫ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com