
����Ŀ�����л���AΪԭ�Ͽ��Ժϳ�ҩ��SERMs���м���E����ϳ�·��������

�ش�����������
��1��A�Ļ�ѧ����Ϊ_________��E�й����ŵ�����Ϊ________________��
��2��A��B�ķ�Ӧ����Ϊ________��B��C�ķ�Ӧ����Ϊ________________��
��3��B�Ľṹ��ʽΪ_________________��
��4����D����E�Ļ�ѧ����ʽΪ__________________��
��5����ȡ�������廯����W��E��ͬ���칹������������������W����___��(���������칹)��
��1molW��������������Һ����������Ӧ����4molAg
������FeCl3��Һ������ɫ��Ӧ
���к˴Ź�������Ϊ�����Ľṹ��ʽΪ_________________��
���𰸡� �䱽����(��1��3-������) �Ѽ����ʻ� ȡ����Ӧ �ӳɷ�Ӧ ![]()
 9
9 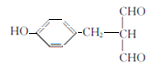
����������1�������л���C�Ľṹ�������A�ķ���ʽ��֪��AΪ�䱽���ӣ�����л���E�Ľṹ��ʽ��֪��E�й�����Ϊ�Ѽ����ʻ�����ȷ�𰸣��䱽����(��1��3-������)���Ѽ����ʻ���
��2��AΪ�䱽���ӣ����B�ķ���ʽ���л���C�Ľṹ��֪��BΪ![]() ������A��B�ķ�ӦΪȡ����Ӧ���л���B��CH2=CHCN�����ӳɷ�Ӧ����
������A��B�ķ�ӦΪȡ����Ӧ���л���B��CH2=CHCN�����ӳɷ�Ӧ����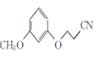 ����ȷ����ȡ����Ӧ���ӳɷ�Ӧ��
����ȷ����ȡ����Ӧ���ӳɷ�Ӧ��
��3��AΪ�䱽���ӣ����B�ķ���ʽ���л���C�Ľṹ��֪��BΪ![]() ����ȷ�𰸣�
����ȷ�𰸣�![]() ��
��
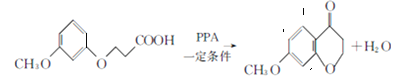
��4�����л���D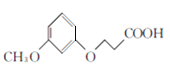 ����ȡ����Ӧ�����л���E
����ȡ����Ӧ�����л���E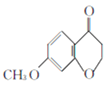 ����ѧ����ʽΪ��
����ѧ����ʽΪ�� ����ȷ����
����ȷ���� ��
��
��5���л���EΪ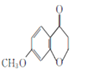 ����ȡ�������廯����W��E��ͬ���칹������1molW��������������Һ����������Ӧ����4molAg������2��ȩ����������FeCl3��Һ������ɫ��Ӧ�����з��ǻ����������ڱ����ϣ������������л����У�1��-OH ��1�� -CH2-CH(CHO)2 �ֱ����ڱ����������ڼ��������1��-OH ��1��-CH(CHO)-CH2-CHO�ֱ����ڱ����������ڼ��������1��-OH ��1�� -C(CH3)(CHO)2�ֱ����ڱ����������ڼ�����֣�������9�֣����к˴Ź�������Ϊ�����Ľṹ��ʽΪ
����ȡ�������廯����W��E��ͬ���칹������1molW��������������Һ����������Ӧ����4molAg������2��ȩ����������FeCl3��Һ������ɫ��Ӧ�����з��ǻ����������ڱ����ϣ������������л����У�1��-OH ��1�� -CH2-CH(CHO)2 �ֱ����ڱ����������ڼ��������1��-OH ��1��-CH(CHO)-CH2-CHO�ֱ����ڱ����������ڼ��������1��-OH ��1�� -C(CH3)(CHO)2�ֱ����ڱ����������ڼ�����֣�������9�֣����к˴Ź�������Ϊ�����Ľṹ��ʽΪ ����ȷ����9��
����ȷ����9�� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС����̽���������ʵ����ʼ��Ʊ���
��̽��һ��ѡ�������װ�ú�ҩƷ̽��������������������ǿ����
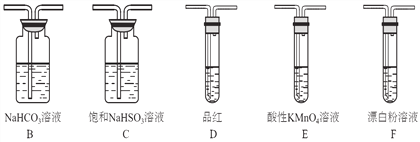
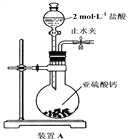
��1��װ��A��ʢҺ��IJ�������������____________��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ________________________________��
��2��װ������˳��ΪA��C��_______��_______��D��F������װ��C��������_________��ͨ������_________________________________������֤�������������ǿ�ڴ����ᡣ
��̽�����������������ƣ�Na2S2O4���׳Ʊ��շۣ��㷺���ڷ�֯��ҵ�Ļ�ԭ��Ⱦɫ����ϴ��ӡ������ɫ�Լ�֯���Ư�ȡ���ȡ���շ�ͨ����Ҫ��������
��3����ȡNa2S2O4���ü����Ʒ��������¶�70-80�棬�ڼ״���Һ���ܼ������ܽ�����ƣ�HCOONa�����ٵμ�Na2CO3��ҺͬʱͨSO2ά����Һ���ԣ���������Na2S2O4���÷�Ӧ�����ӷ���ʽ_________________________________��
��4���ⶨ���շ۴��ȡ�Na2S2O4����ǿ��ԭ������¶�ڿ������ױ�����������Na2S2O4��KMnO4������Һ������Ӧ��5Na2S2O4+6KMnO4+4H2SO4�T5Na2SO4+3K2SO4+6MnSO4+4H2O����ȡ5.0gNa2S2O4��Ʒ������ˮ�У����100mL��Һ��ȡ��10mL����Һ����ƿ�У���0.10molL��1��KMnO4��Һ�ζ����ظ���������2�Σ�ƽ������KMnO4��Һ21.00mL�������Ʒ��Na2S2O4����������Ϊ_______________�����ʲ����뷴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǰ��ԴΣ����һ��ȫ�������⣬��Դ������Ӧ����ԴΣ������Ҫ�ٴ롣
��1������������������Դ����Դ����������________(����ĸ)��
A������̫���ܡ�ˮ�ܡ����ܵ�����Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ��
B���о���ú�������¼�������߲��������㹤ҵ�����Ŀ��ٷ�չ
C��������չũ���������������Ľո�ת��Ϊ����Ч����Դ
D��������Դ���ġ�������Դ���ظ�ʹ�ú���Դ��ѭ������

��2�����ʯ��ʯī��Ϊ̼��ͬ�������壬��������������ʱȼ������һ����̼������������ʱ���ȼ�����ɶ�����̼����Ӧ�зų���������ͼ��ʾ������ͨ��״���£����ʯ��ʯī��Ƚϣ�_________(�� �����ʯ������ʯī��)���ȶ���ʯī��ȼ������H��______________��
��3��N2��O2�����л�ѧ���ļ��ֱܷ���946 kJ/mol��497kJ/mol����֪��N2(g)��O2(g)��2NO(g) ��H����180.0 kJ/mol��NO�����л�ѧ���ļ���Ϊ_____��
��4���ۺ������й���Ϣ����д����CO��ȥNO��������Ⱦ������Ȼ�ѧ����ʽ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤������������˵����ȷ���У�������
A.1molNa2O2���������4NA������
B.0.1mol AlCl3��ȫˮ��ת��Ϊ�����������壬����0.1NA������
C.���³�ѹ��16gO2��O3������庬��NA����ԭ��
D.1mol/LNa2CO3��Һ�к���NA��CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˼���úȼ�նԴ�����ɵ���Ⱦ��ú��������Һ���Ǹ�Ч���������ú̿����Ҫ;����������CO2������ŷ�Ҳ���������ٵ��ش���⣮
��1������֪C��s��+H2O��g���TCO��g��+H2��g����H1=+131.3kJmol��1
C��s��+2H2O��g���TCO2��g��+2H2��g����H2=+90kJmol��1
��һ����̼��ˮ������Ӧ���ɶ�����̼���������Ȼ�ѧ����ʽ�� ��
��2����ȼ�շ����е�CO2ת��Ϊ�����ѵķ�Ӧԭ��Ϊ��
2CO2��g��+6H2��g�� ![]() CH3OCH3��g��+3H2O��g��
CH3OCH3��g��+3H2O��g��
�ٸ÷�Ӧƽ�ⳣ������ʽΪK= ��
�����¶Ȳ��䣬��С��ӦͶ�ϱ�[ ![]() ]����K�����������С�����䡱����
]����K�����������С�����䡱����
��3��ͨ��ˮú���ϳɶ����ѵ��Ȼ�ѧ����ʽ���£�
3H2��g��+3CO��g���TCH3OCH3��g��+CO2��g����H=��aKJ/mol
�÷�Ӧ��һ�������µ��ܱ������пɴﵽƽ��״̬������1��������t0ʱ�̸ı�һ������������I��Ϊ���ߢı�������� �� ������ĸ��ţ�
A.�����¶�
B.�������
C.���������
D.����H2��Ũ��
E.����������ѣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ڼ����������ܹ��ֽ��һ���������������÷�Ӧ���е�45sʱ���ﵽƽ�⣨NO2Ũ��ԼΪ0.0125mol/L����ͼ�е����߱�ʾ���������ֽⷴӦ��ǰ25s�ڵķ�Ӧ���̣�
��1��ǰ20����O2��ƽ���������ʣ�mol/��Ls��
��2����ij�¶��´ﵽƽ����ı���������������������ټ���������NO2 �� ƽ���ƶ��ķ����� �� NO2��ƽ��ת���� 68.75%�����������������=������NO������ٷֺ��� �����������С�����䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2+3H2![]() 2NH3���ǹ�ҵ�����쵪�ʵ���Ҫ��Ӧ�����й��ڸ÷�Ӧ��˵����ȷ����
2NH3���ǹ�ҵ�����쵪�ʵ���Ҫ��Ӧ�����й��ڸ÷�Ӧ��˵����ȷ����
A. �ﵽƽ��ʱ����Ӧ���ʣ�v(��)=v(��)=0
B. ���º�ѹ�£���������He����Ӧ���ʼ���
C. ��������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
D. ���ڷ�Ӧ���ܱ���������1 mol N2������H2�����������2 mol NH3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǹ�ˮ���� {[(CH3COO)2Cr]2��2H2O����Է�������Ϊ376}��һ�����ɫ���壬��������ˮ���dz��õ��������ռ���ʵ��������п�������Ȼ�����Һ����������Һ������Ϊ��Ҫԭ���Ʊ������Ǹ�ˮ�����װ����ͼ��ʾ��������2��Ԥ�ȼ���п������֪���۸����ȶ������ױ���������������п��Ӧ���Ʊ������з�������ط�Ӧ����:
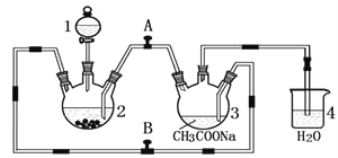
Zn��s��+ 2HCl��aq��=ZnCl2��aq��+ H2��g����
2CrCl3��aq��+Zn��s��= 2CrCl2��aq��+ ZnCl2��aq��
2Cr2+��aq��+ 4CH3COO����aq��+ 2H2O��l��=[(CH3COO)2Cr]2��2H2O��s��
��ش���������:
��1������1��������______________________________________��
��2��������2�м���������Ȼ�����Һ��˳�������____________(�����)��Ŀ����_________________________��
A.��������Ȼ�����Һͬʱ����
B.�ȼ����Ȼ�����Һ��һ��ʱ����ټ�����
C.�ȼ����ᣬһ��ʱ����ټ����Ȼ�����Һ
��3��Ϊʹ���ɵ�CrCl2��Һ���������Һ˳����ϣ�Ӧ�رշ���_____(����A������B"����ͬ)������____��
��4����ʵ����п��Ҫ��������ԭ������ò�����H2��CrCl2��Һѹ��װ��3���������Һ��Ӧ�⣬��һ��������_____________________________________________��
��5����֪������Ӧ��������ʵ��ʱȡ�õ�CrCl3��Һ�к�����9.51g��ȡ�õĴ�������ҺΪ1.5L0.1mol/L��ʵ���ø��﴿����[(CH3COO)2Cr]2��2H2O 9.4g�����ʵ�����ò�Ʒ�IJ���Ϊ____________(�������ܽ�Ĵ����Ǹ�ˮ����)��
��6���������ӻ���Ⱦˮ��������Ҫ��ȥ����ʵ���ж����Cr2+���������Һ��ͨ��������_______���ټ����Һ������pH����Ϊ_______�����Ǹ������ӳ�����ȫ(��������Ũ��ӦС��10-5mol/L)������֪Cr(OH)3���ܶȻ�Ϊ6.3��10-31��![]() ��4��lg2��0.3��
��4��lg2��0.3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������ԭ��Ӧ��ϵ�з�Ӧ������ﹲ�������ӣ�Fe3+��NO![]() ��Fe2+��NH
��Fe2+��NH![]() ��H+��H2O������������ȷ����( )
��H+��H2O������������ȷ����( )
A���÷�Ӧ˵��Fe(NO3)2��Һ���˼����ữ
B���÷�Ӧ���������뻹ԭ�����ʵ���֮��Ϊ8��1
C������1 mol NO![]() ����������Ӧ����ת�Ƶ���5 mol
����������Ӧ����ת�Ƶ���5 mol
D�������÷�Ӧ��Ƴ�ԭ��أ�����ӦΪFe3++e��===Fe2+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com