
【题目】某同学通过实验研究钠及其化合物的有关性质,请回答相关问题。
(1)实验室中少量的钠通常保存在__________中,在实验室中取用钠的仪器是_______________。
(2)若将钠在空气中加热,钠会燃烧发出黄色火焰,同时生成________________色的固体,写出该产物与H2O反应的化学方程式:___________________。
(3)将金属钠投入水中,发生反应的离子方程式为______________________。
(4)该同学在实验室欲配制500 ml.0.1 mol/L NaOH溶液。
①配制溶液时肯定不需要如图所示仪器中的______________(填字母),配制上述溶液还需要用到的玻璃仪器是_______________(填仪器名称)。

②根据计算,该同学应用托盘天平称取NaOH的质量为________。
③该同学将所配制的NaOH溶液进行测定,发现浓度大于0.1 mol/L。下列操作会引起所配浓度偏大的是___________。
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
D.往容量瓶转移时,有少量液体溅出
E.在容量瓶中定容时俯视容量瓶刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
【答案】(1)煤油或石蜡油;镊子(各1分)
(2)淡黄(1分);2Na2O2+2H2O=4NaOH+O2↑(2分)
(3)2Na+2H2O=2Na++2OH-+H2↑(2分)
(4)①AC;烧杯、玻璃棒②2.0 g(2分)③CE(2分)
【解析】
试题分析:(1)钠能够与空气中氧气、水等物质反应,实验室中少量的通常保存在煤油中,在实验室中取用钠的仪器镊子。
(2)钠燃生成黄色的固体过氧化钠,过氧化钠与H2O反应的化学方程式:2Na2O2+2H2O=4NaOH+O2↑。
(3)钠投入水中生成氢氧化钠和氢气,2Na+2H2O=2Na++2OH-+H2↑;
(4)配置溶液一定不用烧瓶和分液漏斗,需要的仪器:量筒、玻璃棒、胶头滴管、容量瓶、烧杯等;②配制500 ml.0.1 mol/L NaOH溶液需要NaOH固体质量0.1×0.5×40=2.0 g ;③A.烧杯未进行洗涤,溶质减少,偏低;B.配制前,容量瓶中有少量蒸馏水,溶质不变,无影响;C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容,冷却到室温时,体积减少,浓度偏大;D.往容量瓶转移时,有少量液体溅出,溶质减少,浓度偏低;E.在容量瓶中定容时俯视容量瓶刻度线,造成溶液体积较少,浓度偏大;F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,溶液体积增大,浓度偏小;


科目:高中化学 来源: 题型:
【题目】RFC是一种将水电解技术与氢氧燃料电池技术向结合的可充电电池。下图为RFC工作原理示意图,下列有关说法正确的是
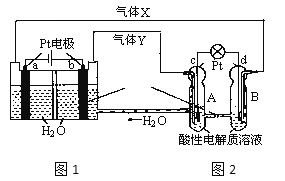
A.图1把化学能转化为电能,图2把电能转化为化学能,水得到了循环使用
B.当有0.1mol电子转移时,a极产生0.56LO2(标准状况下)
C.c极上发生的电极反应是:O2+4H++4e-=2H2O
D.图2中电子从c极流向d极,提供电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2、CO、CH4的燃烧热分别为ΔH1=-285.8 kJ/mol、ΔH2=-283 kJ/mol、ΔH3=-890 kJ/mol。H2O(g)=H2O(l) ΔH4=-44 kJ/mol。回答下列问题:
(1)用CH4替代水煤气作家用燃气的优点是____________________。将煤气灶改为天然气灶时,应适当调_________(填“大”或“小”)空气进气阀门。
(2)合成氨厂一般采用烃(以CH4为例)和水蒸气反应制取原料气H2,发生如下反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。
CO(g)+3H2(g)。
①该反应的ΔH=________________。
②当该反应达到平衡状态时,下列说法一定正确的是__________(填字母)。
A.v(CH4)=v(CO) B.加入催化剂,ΔH不变
C.升高温度,平衡常数K增大 D.CH4与H2O的转化率相等
③T℃时,该反应的初始浓度与起始速率的部分数据如下:
初始浓度/mol·L-1 | 起始速率/mol3·L-3·s-1 | |
c(CH4) | c(H2O) | v |
0.10 | 0.10 | 1.0×10-4 |
0.10 | 0.20 | 4.0×10-4 |
0.30 | 0.20 | 1.2×10-3 |
写出起始速率与初始浓度的关系式[用c(CH4)、c(H2O)及适当的速率常数表示]v=________。
④T℃时,在一个体积可变的恒压密闭容器中,充入0.1 mol CH4、0.1 mol H2O(g)发生反应,起始时容器的体积为1 L。CH4的转化率与反应时间的关系如图中曲线A所示。则T℃时该反应的平衡常数K=____________。若温度与投料方式相同,该反应在容积为1 L的恒容密闭容器中进行,刚达平衡状态的点是__________(选填B、C、D、E)。
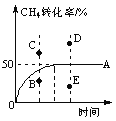
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成。甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子。A元素原子核内质子数比E的少l,D、E同主族。某同学为探究甲的组成而进行如下实验:

①取mg甲的晶体溶于蒸馏水,配成500 mL溶液;
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20 mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224 mL。
回答下列问题:
(1)D在元素周期表中的位置为_ 。
(2)经测定晶体甲的摩尔质量为453 g·mol-1,其中阳离子和阴离子物质的量之比为1:1。 则晶体甲的化学式为 。
(3)图像中V(Oa):V(ab):V(bc)= 。
(4)写出ab段发生反应的离子方程式: 。
(5)配成的甲溶液物质的量浓度是_ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
方法Ⅰ | 用炭粉在高温条件下还原CuO |
方法Ⅱ | 用肼(N2H4)还原新制Cu(OH)2 |
方法Ⅲ | 电解法:2Cu+H2O |
已知:2Cu(s)+1/2O2(g)=Cu2O(s);△H=-akJ·mol-1
C(s)+1/2O2(g)=CO(g);△H=-bkJ·mol-1
Cu(s)+1/2O2(g)=CuO(s);△H=-ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g) △H = kJ·mol-1
(1)工业上很少用方法Ⅰ制取Cu2O是由于方法Ⅰ反应条件不易控制,若控温不当,会降低Cu2O产率,请分析原因: 。
(2)方法Ⅱ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为 。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,写出电极反应式:阴极 ;阳极 。

(4)在相同的密闭容器中,用方法Ⅱ和方法Ⅲ制得的Cu2O分别进行催化分解水的实验:2H2O(g) ![]() 2H2(g)+ O2(g) ⊿H >0,水蒸气的浓度(mol·L-1)随时间t (min)变化如下表所示:
2H2(g)+ O2(g) ⊿H >0,水蒸气的浓度(mol·L-1)随时间t (min)变化如下表所示:
序号 | Cu2Oa克 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
① | 方法Ⅱ | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
② | 方法Ⅱ | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
③ | 方法Ⅲ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
下列叙述正确的是 (填字母代号)。
a.实验的温度T2小于T1
b.实验①前20 min的平均反应速率v(O2)=7×10-5 mol·L-1 min-1
c.实验②比实验①所用的催化剂催化效率高
d.实验①、②、③的化学平衡常数的关系:K1=K2<K3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,在一定条件下既能起加成反应,也能起取代反应,但不能使KMnO4酸性溶液褪色的是 ( )
A. 甲烷 B. 苯 C. 乙烯 D. 乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人设想用SO2制取少量硫酸,其装置如图所示:

①H+移向 极(填“a”或“b”),c极的电极名称是 ,
②a极发生的电极反应式为 。
③c极发生的电极反应式为 。
④标准状况下,A装置吸收3.36LSO2时,B装置中溶液最多减重 g。(装置中气体的溶解性忽)不计)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com