
【题目】下列反应中属于加成反应的是( )
A.乙炔通入酸性高锰酸钾溶液中,溶液褪色
B.苯滴入溴水中,振荡后溴水层接近无色
C.油脂的皂化反应
D.将裂化获得的汽油滴入溴水中,溴水褪色
科目:高中化学 来源: 题型:
【题目】NaCN超标的电镀废水可用两段氧化法处理:
(1)NaCN与NaClO反应,生成NaOCN和NaCl
(2)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
已知HCN(Ki=6.3×10-10)有剧毒;HCN、HOCN中N元素的化合价相同。
完成下列填空:
(5)上述反应涉及到的元素中,氯原子核外电子能量最高的电子亚层是___________;H、C、N、O、Na的原子半径从小到大的顺序为_______。
(6)HCN是直线型分子,HCN是___________分子(选填“极性”或“非极性”)。HClO的电子式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为含有少量Zn杂质的粗银电解精炼银的示意图

(1) (填a或b)极为含有杂质的粗银。
(2)电解一段时间后电解液中c(Ag+)浓度________(填偏大,偏小或不变)。
(3)若b极有少量红棕色气体生成,则生成该气体的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
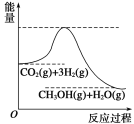
(1)你认为该反应为____________(填放热或吸热)反应.
(2)恒容容器中,对于以上反应,能加快反应速率的是 。
a.升高温度 b.充入He c.加入催化剂 d.降低压强
(3)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
从反应开始到5min末,用H2浓度变化表示的平均反应速率v(H2)= ;反应达到平衡状态,此时H2的转化率为 。
(4)在相同温度、容积不变的条件下,能说明该反应已达平衡状态的是 (填序号)。
a.CO2、H2、CH3OH、H2O的浓度均不再变化
b.v生成(CH3OH)=v消耗(CO2)
c.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶1∶1∶1
d.容器中混合气体的密度保持不变
e. H2的消耗速率与CH3OH的消耗速率之比为3∶1
f.体系压强不变
(5)以CH3OH、空气、氢氧化钾溶液为原料,石墨为电极可构成然料电池,该电池中负极上的电极反应式是:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是:4Ag+2H2S+O2===2X+2H2O。下列说法正确的是
A.X的化学式为AgS
B.银针验毒时,空气中氧气失去电子
C.反应中Ag和H2S均是还原剂
D.每生成1 mol X,反应转移2 mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2的离子化合物。
(1)写出Y2O2的电子式:____ _,其中含有的化学键是___ _。
(2)用电子式表示Y2O的形成过程________ _______。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶浓氧化性最强的是_____(填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是__________(填化学式)。
(5)由X、Y组成的化合物分子中.X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式_______________ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN﹣![]() Fe(SCN)3↓
Fe(SCN)3↓
B.向海带灰浸出液中加入稀硫酸、双氧水:2I﹣+2H++H2O2![]() I2+2H2O
I2+2H2O
C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH﹣![]() Na2SiO3↓+H2O
Na2SiO3↓+H2O
D.NaHCO3溶液和少量Ba(OH)2溶液混合:+OH﹣+Ba2+![]() H2O+BaCO3↓
H2O+BaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电-Fenton法是用于水体里有机污染物降解的高级氧化技术。其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2![]() Fe3++OH- +·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法不正确的是
Fe3++OH- +·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法不正确的是
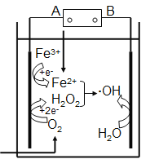
A.电源的A极是负极
B.电解池中只有O2、Fe3+发生还原反应
C.阳极上发生电极反应:H2O-e-![]() ·OH + H+
·OH + H+
D.消耗1molO2,可以产生4mol ·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多沙唑嗪盐酸盐是一种用于治疗高血压的药物。多沙唑嗪的合成路线如下:
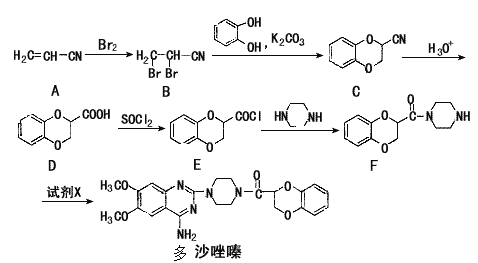
(1)写出D中两种含氧官能团的名称:______和_____。
(2)写出满足下列条件的D的两种同分异构体的结构简式_______________________。
①苯的衍生物,且苯环上的一取代产物只有两种;②与Na2CO3溶液反应放出气体;
③水解后的产物才能与FeCl3溶液发生显色反应。
(3)E→F的反应中还可能生成一种有机副产物,该副产物的结构简式为____________。
(4)由F制备多沙唑嗪的反应中要加入试剂X(C10H10N3O2Cl),X的结构简式为_______。
(5)苯乙酸乙酯是一种常见的合成香料。请设计合理的方案以苯甲醛和乙醇为原料合成
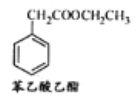
苯乙酸乙酯(用合成路线流程图表示,并注明反应条件)。
提示:①R-Br+Na→R-CN+NaBr;
②合成过程中无机试剂任选;
③合成路线流程图示例如下:
CH3CH2OH ![]() H2C=CH2
H2C=CH2![]() BrH2C-CH2Br
BrH2C-CH2Br
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com