
【题目】将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c(NH4+)=c(Cl-) ⑤c(NH4+)<c(Cl-)正确的是( )
A. ①⑤ B. ③④ C. ②⑤ D. ②④
科目:高中化学 来源: 题型:
【题目】化学小组设计以下实验方案,测定某部分变质为碳酸钠的小苏打样品中NaHCO3的质量分数。
(1)方案一:称取一定质量样品,置于仪器a中用酒精灯加热至恒重,冷却,用托盘天平称量剩余固体质量。重复操作,计算。
仪器a的名称是____________;其中发生反应的化学方程式为_______________。实验中为保证NaHCO3分解完全需加热至恒重,判断方法是________________。
⑵方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,待沉淀后,过滤,洗涤,干燥,称量固体质量,计算。
写出NaHCO3与足量Ba(OH)2溶液反应的离子方程式_______________;实验中判断沉淀是否完全的方法是______________。过滤操作中,除烧杯、漏斗外,还要用到的玻璃仪器为____________。
(3)方案三:称取一定质量样品,按如图装置进行实验:

B装置内所盛试剂是;D装置的作用是______________。实验前称取17.9g样品,实验后测得C装置增重8.8g,则样品中NaHCO3的质量分数为________。某同学认为上述测定结果__________(填“偏高”或“偏低”),因为实验装置还存在一个明显的缺陷是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学变化一定存在:①状态和颜色的变化 ②发光放热 ③生成新物质 ④气体的放出 ⑤能量的变化( )
A. ③ B. ③⑤ C. ②④⑤ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A.Fe、Fe2O3都能与稀盐酸反应,都属于置换反应
B.CaO、NaOH固体都能与水反应,都能作干燥剂
C.浓盐酸、浓硫酸都有挥发性,敞口放置浓度都会变小
D.NH4Cl、(NH4)2SO4都含有NH4+,都能与熟石灰反应生成NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将250mL含BaCl2和KCl的混合溶液分成5等份,取一份加入含amol硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀。则原混合溶液中钾离子物质的量浓度为
A.4(b-2a)mol/L
B.20(2a-b)mol/L
C.20(b-2a)mol/L
D.10(b-a)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( )
A. B.
B.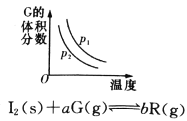
C. D.
D.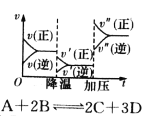
A.t0时改变某一条件有如图所示,则改变的条件一定是加入催化剂
B.反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应
C.从加入反应物开始,物质的百分含量与温度关系如图所示,则该反应的正反应为吸热反应
D.反应速率和反应条件变化如图所示,则该反应正反应为放热反应,A、B、C是气体、D为固体或液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2.0L的密闭容器内,物质D在T℃时发生反应。其反应物和生成物的物质的量随时间t的变化关系如下图,据图回答下列问题:
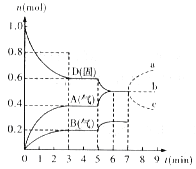
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为___________mol/(Lmin)。(结果保留两位有效数字)
(2)根据右图写出该反应的化学方程式___________。
(3)第5分钟时,升高温度,A、B、D的物质的量变化如图,则该反应是___________(填“放热”或“吸热”)反应,若在第7分钟时增加D的物质的量,A的物质的量变化正确的是___________(用图中a~c的编号回答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“组成不同生物的元素含量有不同”。对此现象的合理解释是( )
A. 组成细胞的化学元素在含量上具有差异性
B. 生物界与非生物界在元素含量上具有差异性
C. 生物根据自身生命活动的需要,有选择地从环境中吸收的元素
D. 生物体内元素的存在形式各不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com