
【题目】把0.6molX气体和0.4molY气体混合于2L容器中,发生反应:3X(g)+Y(g)= nZ(g) +2W(g).5min末已生成0.2molW,若测知以Z浓度的变化来表示平均速率为0.01mol/(L·min),则
(1)上述反应Z气体的计量系数n的值是______;
(2)上述反应在5min末时,已用去的Y占原来物质的质分数是__________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下图所示装置的叙述,正确的是( )
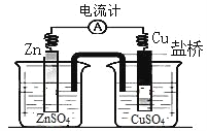
A.铜做正极,铜片上有气泡产生
B.盐桥中的阴离子会移向 CuSO4 溶液
C.正极附近的 SO![]() 浓度逐渐增大
浓度逐渐增大
D.锌片表面被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中各微粒浓度关系正确的是( )
A.向氨水中滴加稀硫酸至溶液呈中性:c(NH4+)=c(SO![]() )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
B.向 l00mL 3 mol/L 的 NaOH 溶液中通入标准状况下体积为 4.48L 的 CO2:3c(Na+)=2[c(CO3 2-)+c(HCO3-)+c(H2CO3)]
C.CH3COONa 溶液中加入少量 KNO3 后溶液一定有:c(Na+)+c(H+)=(CH3COO 一)+c(OH 一)
D.等物质的量浓度的①NH4HSO4、②NH4HCO3、③NH4Cl 溶液中,c(NH4+)的大小关系:①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究NO与铜粉的反应并检验NO,实验装置如图所示(夹持装置略)。实验开始前,向装置中通入一段时间的N2,排尽装置内的空气。

已知:在溶液中.FeSO4+NO![]() [Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法不正确的是
[Fe(NO)]SO4(棕色),该反应可用于检验NO。下列说法不正确的是
A. 装置F、I中的试剂依次为水、硫酸亚铁溶液
B. 若观察到装置H中红色粉末变黑色,则NO与Cu发生了反应
C. 实验结束后,先熄灭酒精灯,再关闭分液漏斗的活塞
D. 装置J收集的气体中一定不含NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2在工业上常作为重要的化工原料,其混合气称为合成气。工业上CH4—H2O 催化重整是目前大规模制取合成气的重要方法,其原理为:
反应Ⅰ:CH4(g)+H2O(g)![]() CO(g)+3H2(g) H1 = +210kJ/mol
CO(g)+3H2(g) H1 = +210kJ/mol
反应Ⅱ:CO(g)+ H2O(g)![]() CO2(g)+H2(g) H2 =﹣41kJ/mol
CO2(g)+H2(g) H2 =﹣41kJ/mol
(1)CH4(g)、H2O(g)反应生成 CO2(g)、H2(g)的热化学方程式是 ___________________________。
(2)反应Ⅰ达到平衡的标志是(____________)
a.恒温恒容情况下,压强不再改变 b. v(CO):v(H2)=1:3
c.平均相对分子质量不再改变 d.恒温恒容情况下,气体密度不再改变
(3)若容器容积不变,不考虑反应Ⅰ,对反应Ⅱ下列措施可增加 CO 转化率的是(____________)
a.升高温度 b.将 CO2 从体系分离 c.充入 He,使体系总压强增大 d.按原投料比加倍投料
(4)某温度下,对于反应Ⅰ,将 n(H2O)∶n(CH4) = 1∶1 的原料气充入恒容密闭容器中,初始压强为 P0,反应达 平衡时总压强为 P1,则平衡时甲烷的转化率为 ____________________________ (忽略副反应)。
(5)将 1molCH4(g) 和 1molH2O(g)加入恒温恒压的密闭容器中(温度 298K、压强 100kPa),发生反应Ⅰ,不考虑 反应Ⅱ的发生,该反应中,正反应速率 v 正=k 正×p(CH4)×p(H2O) , 逆反应速率 v 逆=k 逆×p(CO)×p3(H2),其中 k 正、k 逆 为速率常数,p 为分压(分压=总压×物质的量分数),则该反应的压强平衡常数 Kp= ____________________________ (以 k 正、k 逆表示)。若 该条件下 k 正=4.4×104kPa-1·s-1,当 CH4 分解 20%时,v 正= ___________________________kPa·s-1(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:Zn(s) +![]() O2(g) =ZnO(s) ΔH1=-351.1kJ/mol
O2(g) =ZnO(s) ΔH1=-351.1kJ/mol
Hg(l) +![]() O2(g) = HgO(s) ΔH2=-90.7kJ/mol
O2(g) = HgO(s) ΔH2=-90.7kJ/mol
由此可知Zn(s) + HgO(s) = ZnO(s) + Hg(l)的ΔH3,其中ΔH3的值是
A.-260.4 kJ/molB.-254.6 kJ/molC.-438.9 kJ/molD.-441.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.用坩埚灼烧![]() 的反应式
的反应式 ![]()
![]()
![]()
B.根据表中提供的数据,等物质的量浓度的NaClO、![]() 混合溶液中,有
混合溶液中,有![]()
化学式 | 电离常数 |
HClO |
|
|
|
|
C.常温下,将![]() 的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一
的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一
D.某温度时,![]() 在水中的沉淀溶解平衡曲线如图所示,溶度积常数
在水中的沉淀溶解平衡曲线如图所示,溶度积常数![]() 则加入
则加入![]() 可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点
可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点
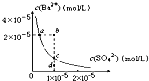
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.可通过加成反应实现![]() 的转化
的转化
B.组成元素的质量分数相同,相对分子质量也相同的不同化合物,一定互为同分异构体
C.核磁共振氢谱、红外光谱都能够快速精确地测定有机物的相对分子质量
D.烯烃只能发生加成反应,不能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是
A. 0.1 mol·L1 Na2S溶液与0.1 mol·L1 NaHS溶液等体积混合:3c(Na+)2c(HS)=2c(S2)+2c(H2S)
B. 向20 mL 0.1 mol·L1 NH4HSO4溶液中滴入0.1 mol·L1 NaOH溶液 20 mL:2c(![]() )=c(NH3·H2O)+c(
)=c(NH3·H2O)+c(![]() )
)
C. 10 mL 0.1 mol·L1 CH3COONa溶液与6 mL 0.2 mol·L1盐酸混合:c(Cl)>c(Na+)>c(OH)>c(H+)
D. 0.2 mol·L1 NaHCO3溶液和0.1 mol·L1 NaOH溶液等体积混合:3c(![]() )+6c(H2CO3)c(Na+)=3c(OH)3c(H+)
)+6c(H2CO3)c(Na+)=3c(OH)3c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com