
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸的反应,记录以下实验数据:
实验编号 | 实验温度 | 试管中所加试剂及其用量 / mL | 溶液褪至无色所需时间/ min | |||
0.6mol/L H2C2O4 溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4溶液 | |||
① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式_________,当该反应以表中数据反应完全时转移电子数为_______NA;
(2)V1=________ mL;
(3)根据上表中的实验①、②数据,可以得到的结论是________。
(4)探究温度对化学反应速率的影响,应选择________(填实验编号);
(5)该小组同学根据经验绘制了n(Mn 2+)随时间变化的趋势如图所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn 2+)随时间变化的实际趋势如图所示。

该小组同学根据如图所示信息提出了新的假设,并设计以下实验方案继续进行实验探究。
实验编号 | 实验温度/℃ | 试管中所加试剂及其用量 | 再加入某种固体 | 溶液褪至无色所需时间 / min | |||
④ | 25 | 0.6mol/L H2C2O4 | H2O | 3mol/L H2SO4 | 0.05mol/L KMnO4溶液 | ||
2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t | ||
①小组同学提出的假设是_________。
②若该小组同学提出的假设成立,应观察到_______________________现象。
【答案】2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 0.00075 2.0 其他条件相同时,反应物浓度减小,反应速率减慢 ②、③ Mn2+对该反应有催化作用 褪色时间变短
【解析】
(1)酸性高锰酸钾与草酸的反应生成CO2、Mn2+和H2O,结合电荷守恒、原子守恒和电子守恒配平书写离子方程式,分析图表数据n(KMnO4)=0.05mol/L×0.003L=0.00015mol,n(H2C2O4)=0.6mol/L×0.003L=0.0018mol,结合化学方程式定量关系分析判断,高锰酸钾完全反应,据此计算电子转移总数;
(2)探究H2C2O4溶液浓度对反应速率的影响,则必须保证其他影响反应速率的因素是相同的;
(3)实验①和②除H2C2O4溶液浓度不同,其它均相同;
(4)实验②和③除温度不同,其它均相同;
(5)①由图乙可知反应开始后锰离子浓度增大,反应速率增加的比较快,所以探究的是硫酸锰在反应中的作用;
②若反应加快,说明Mn2+是催化剂,反应过程中溶液褪色时间减少。
(1)酸性高锰酸钾与H2C2O4的反应生成CO2、Mn2+和H2O,结合电子守恒、电荷守恒、原子守恒,可得配平的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,分析图表数据n(KMnO4)=0.05mol/L×0.003L=0.00015mol,n(H2C2O4)=0.6mol/L×0.003L=0.0018mol,结合化学方程式定量关系分析判断,高锰酸钾完全反应,据此计算电子转移总数=0.00015mol×(7-2)×NA=7.5×10-4NA;
(2)探究H2C2O4溶液浓度对反应速率的影响,必须保证其他影响反应速率的因素是相同的,而由实验②可知,H2C2O4溶液、H2O、KMnO4溶液和稀硫酸的体积和为10.0mL,由于须保证KMnO4 溶液的浓度相同,故V1=2.0mL;
(3)由实验①和②数据可知,H2C2O4溶液浓度不同,说明探究浓度对反应速率的影响,可知其他条件不变,增大反应物的浓度,加快反应速率;
(4)由实验②和③数据可知,除温度不同,其它均相同,说明探究温度对反应速率的影响,故应该选择②③;
(5)①由图乙可知反应开始后速率增大较快,说明Mn2+对该反应起催化剂的作用;
②若该小组同学提出的假设成立,则反应速率加快,溶液褪色的时间小于1.5min,从而说明Mn2+是催化剂。


科目:高中化学 来源: 题型:
【题目】织物漂白剂亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO![]() 、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。25 ℃时,各组分含量随pH变化情况如图所示(Cl-没有画出)。下列说法错误的是
、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。25 ℃时,各组分含量随pH变化情况如图所示(Cl-没有画出)。下列说法错误的是

A. 25 ℃时,HClO2的电离平衡常数的数值Ka=10-6
B. 使用该漂白剂的最佳pH为3.0
C. 25 ℃时,等浓度的HClO2溶液和NaClO2溶液等体积混合后,混合溶液中:c(HClO2)+2c(H+)=c(ClO![]() )+2c(OH-)
)+2c(OH-)
D. 该温度下的NaClO2溶液中c(Na+)>c(ClO![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有Fe2+、Mg2+、Cu2+、NH4+、Al3+中的一种或几种。当加入一种淡黄色固体并加热溶液时,有刺激性气体放出和白色沉淀生成,加入淡黄色固体的物质的量(横坐标)与析出沉淀和产生气体的物质的量(纵坐标)的关系,如下图所示。请填写下列空白:

(1)在该溶液中含有的离子是_____________,物质的量浓度之比为_______________。
(2)所加的淡黄色固体是________________(化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制备气体和验证气体性质的装置图。
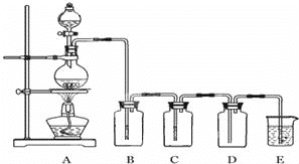
若利用如图装置实现碳和浓硫酸的反应,并进行如下验证:
①装置B、C、D、E中分别装有品红溶液、酸性KMnO4溶液、品红溶液、澄清石灰水,则D装置中品红溶液的作用是______,证明气体中有CO2的现象是______。
②若证明SO2具有氧化性,同时证明碳酸的酸性比硅酸的强,B、C、D中分别装有Na2S溶液、足量酸性KMnO4溶液、品红溶液。
则:B中的现象______,E中应加入______溶液,E中发生反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气的化学方程式为:4HCl(浓)+MnO2![]() Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
(1)反应物HCl中氯元素的化合价为___。
(2)在该氧化还原反应中,MnO2做___剂,锰元素被___,而HCl在反应中表现的性质包括___和___。
(3)若有6molCl2生成时,反应中转移___mol电子。
(4)写出该反应的离子方程式___,用双线桥法标出电子转移的方向和数目:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol·L-1的MgCl2溶液中各加入10滴2 mol·L-1NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
实验序号 | 加入试剂 | 实验现象 |
Ⅰ | 4 mL 2 mol·L-1HCl 溶液 | 沉淀溶解 |
Ⅱ | 4 mL 2 mol·L-1NH4Cl 溶液 | 沉淀溶解 |
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程_____________。
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因___________。
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是_________。
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是____________。
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是___________。
③乙同学这样配制混合溶液的理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】8gCH4共有___mol氢原子,0.1molNH3共有约___个原子,同温同压下,同体积的NH3和H2S气体的质量比为___;同温同压下,同质量的NH3和H2S气体的体积比为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)甲苯苯环上的氢原子被相对分子质量为43的烃基取代,所得一元取代物有_________ 种。
(2)已知二氯苯有3种同分异构体,则四氯苯的同分异构体数目有________种。
(3)某芳香烃的分子式为C8H10,它不能使溴水褪色,但能使酸性KMnO4溶液褪色,该有机物苯环上的一氯代物只有一种,则该烃的结构简式是_____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上烟气脱氮的原理![]()
(1)该反应化学平衡常数K的表达式为____________。温度升高,K值___________(选填“增大”、“减小”、“不变”)。如果平衡常数K值增大,对_______(填“正反应”或“逆反应”)的速率影响更大。
(2)若反应在恒容条件下进行,能说明反应已经达到平衡状态的是______(填序号)
a.容器内混合物的质量不变 b.容器内气体的压强不变
c.反应消耗0.5mol NO的同时生成1mol N2 d.![]() 的浓度不变
的浓度不变
(3)向2 L密闭容器中加入反应物,10 min后达到平衡,测得平衡时气体的物质的量增加了0.2mol,则用![]() 表示的平均反应速率为__________。
表示的平均反应速率为__________。
(4)如图是P1压强下NO的转化率随反应时间(t)的变化图,请在图中画出其他条件不变情况下,压强为![]() 下NO的转化率随反应时间变化的示意图。
下NO的转化率随反应时间变化的示意图。
 ______
______
(5)工业合成氨的反应温度选择500℃左右的原因是_______________。
(6)写出反应物中的氨气的电子式______;其空间构型为______;它常用来生产化肥![]() 。
。![]() 溶液显__________性;常温下将等体积等浓度的氨水和
溶液显__________性;常温下将等体积等浓度的氨水和![]() 溶液混合,pH>7,溶液中
溶液混合,pH>7,溶液中![]() 浓度由大到小的关系是_______________。
浓度由大到小的关系是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com