
| A、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| B、含有大量Fe2+的溶液中:H+、Mg2+、ClO-、NO3- |
| C、c(H+)=10-12mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、能使Al溶解产生H2的溶液中:NH4+、Na+、SiO32-、HCO3- |


科目:高中化学 来源: 题型:
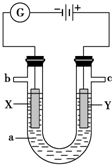 如图表示一个电解池,装有电解液a;X、Y是两块电极板通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 联合国气候变化大会于2010年12月召开,焦点议题之一是发展“低碳经济,节能减排”,减少温室气体排放.你认为下列做法中,不能有效减少空气中CO2含量的是( )
联合国气候变化大会于2010年12月召开,焦点议题之一是发展“低碳经济,节能减排”,减少温室气体排放.你认为下列做法中,不能有效减少空气中CO2含量的是( )| A、开发利用太阳能、风能、生物能、海洋能等清洁能源 |
| B、使用节能产品,推广节能环保汽车 |
| C、植树造林,增加森林植被面积 |
| D、用脱硫处理的煤代替原煤作燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-CH3 |
| B、-CHO |
| C、-COOH |
| D、-OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的醋酸和pH=11氢氧化钠溶液 |
| B、pH=2的硫酸和pH=12的氢氧化钠溶液 |
| C、pH=3的盐酸和pH=11的氨水 |
| D、pH=2的硝酸和pH=12的氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有酸性 |
| B、只有氧化性 |
| C、只有还原性 |
| D、以上三种均具有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com