
【题目】化学与生活、环境密切相关,下列说法错误的是
A. 补铁剂与维生素C共同服用可提高补铁效果
B. 铁粉和碳粉的混合物可作食品抗氧化剂
C. 生活中钢铁制品生锈主要是析氢腐蚀所致
D. 新能源汽车的推广使用有助于减少光化学烟雾
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定溶液中能大量共存的是
A. 无色溶液中:K+、Na+、MnO4—、SO42—
B. 在酸性溶液中:Ba2+、Na+、SO42—、Cl—
C. 加入Al能放出H2的溶液中:Cl—、HCO3—、SO42—、NH4+
D. 含大量Fe2+溶液中:K+、Cl—、SO42-、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2、CO是处理方法对环境保护用重要意义。
(1)已知:①CO2(g)+H2(g)![]() CO(g)+H2O(g) △H=+41kJ·mol-1
CO(g)+H2O(g) △H=+41kJ·mol-1
②C(g)+2H2(g)![]() CH4(g) △H=-73kJ·mol-1
CH4(g) △H=-73kJ·mol-1
③2CO(g)![]() C(g)+CO2(g) △H=-171kJ·mol-1
C(g)+CO2(g) △H=-171kJ·mol-1
则CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=__________。
CH4(g)+2H2O(g) △H=__________。
(2)CO2与H2反应可合成甲醇:CO2(g)+3H2(g)![]() CH4(g)+H2O(g)
CH4(g)+H2O(g)
某温度下,将1molCO2和3molH2充入探究不变的2L密闭容器中,发生上述反应。测得不同时刻的反应前后压强关系如下:
时间(h) | 1 | 2 | 3 | 4 | 5 | 6 |
P后/p前 | 0.90 | 0.85 | 0.82 | 0.81 | 0.80 | 0.80 |
①用CO2表示第1小时反应的平均速率v(CO2)=_______mol·L-1·h-1。
②该温度下的H2平衡转化率为______________。
(3)CO2与NH3反应可合成尿素:CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g)
CO(NH2)2(s)+H2O(g)
在T1℃时,将1molCO2和2molNH3置于1L密闭容器中,发生上述反应,在t时刻,测得容器中CO2转化率约为73%。保护其他初始实验条件不变,分别在温度为T2℃、T3℃、T4℃、T5℃时,重复上述实验,经过相同时间测得CO2转化率并绘制变化曲线如图所示:

①该反应的△H______0(填“>”或“<”)
②T4℃时该反应的平衡常数K=___________。
③在T1℃~T3℃之间,CO2转化率逐渐增大,其原因是____________________。
(4)工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图所示
img src="http://thumb.zyjl.cn/questionBank/Upload/2018/01/02/09/ce4caee6/SYS201801020935301407189654_ST/SYS201801020935301407189654_ST.003.png" width="212" height="154" style="-aw-left-pos:0pt; -aw-rel-hpos:column; -aw-rel-vpos:paragraph; -aw-top-pos:0pt; -aw-wrap-type:inline" />
①阳极区产生CO2的原因是______________(用离子方程式表示)。
②利用平衡移动原理,简述CO32-在阴极区再生的原因_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂的操作方法正确的是 ( )
A. N2中有少量的O2:通过灼热的木炭。
B. 食盐中有少量的NH4Cl:加过量的烧碱溶液后加热蒸干。
C. NO中有少量的NO2:用水洗涤后再干燥。
D. CO2中混有少量的SO2气体:通过饱和NaHSO3溶液洗气。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,N5是破坏力极强的炸药之一,18O2是比黄金还贵的物质。下列说法正确的是( )
A. N5和N2互为同位素 B. 2N5==5N2是化学变化
C. 原子半径:N<18O D. 18O2的摩尔质量为36
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒温密闭容器发生可逆反应Z(?)+W(?)![]() X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
X(g)+Y(?)ΔH,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后未再改变条件。下列有关说法中正确的是
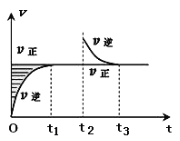
A.Z和W在该条件下至少有一个是为气态
B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C.若该反应只在某温度T0以上自发进行,则该反应的平衡常数K随温度升高而增大
D.若在该温度下此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废催化剂含58.2%的SiO2、21.0%的ZnO、4.50%的ZnS和12.8%的CuS及少量的Fe3O4。某同学用15.0 g该废催化剂为原料,回收锌和铜。采用的实验方案如下,回答下列问题:

已知:ZnS与稀硫酸反应,且化合价不变; CuS既不溶解于稀硫酸,也不与稀硫酸反应
(1)在下列装置中,第一次浸出反应装置最合理的_______(填标号)。

(2)滤液1中含有Fe2+,选用提供的试剂进行检验,检验方法如下:____________。
(提供的试剂:稀盐酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水)
(3)本实验要用到抽滤,设所用的洗涤剂为X,抽滤洗涤沉淀的操作__________。
(4)写出第二次浸出的化学反应方程式__________________________,
向盛有滤渣1的反应器中加H2SO4和H2O2溶液,应先加_________________。
(5)滤渣2的主要成分是____________________________________。
浓缩、结晶得到硫酸锌晶体的主要仪器名称是______________________。
(6)某同学在实验完成之后,得到1.50 g CuSO4·5H2O,则铜的回收率为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知,在木炭还原氧化铜的实验中发生的主要反应是C+2CuO![]() 2Cu+CO2↑。某化学实验小组对该实
2Cu+CO2↑。某化学实验小组对该实
验产物(假设已完全反应)进行了如下探究:
探究一:检验产物的成分
【提出问题】实验产物是暗红色固体,很难观察到紫红色固体,那么该暗红色固体物质是什么?
【查阅资料】氧化亚铜(Cu2O)为红色固体,可以和硫酸反应:Cu2O+H2SO4═CuSO4+Cu+H2O。
【猜想假设】暗红色固体除铜外还可能含有Cu2O。
【设计实验】取少量暗红色固体,加入稀硫酸,如果观察到_______________,说明猜想正确。
探究二:测定产物中Cu2O的含量

【查阅资料】草酸在浓硫酸的作用下会分解为CO和CO2
【设计实验】称取固体样品6.0g,置于上右图装置D中进行实验(固定装置略去,碱石灰为氧化钙和氢氧化钠的混合物),通过测定反应前后装置E的质量达到实验目的。
(1)证明草酸的分解产物中有CO2存在的是_______________。
(2)装置C的作用是__________________。
(3)写出装置D中反应的化学方程式___________________________。
(4)下列为加热装置前所涉及的部分操作,正确的顺序是_________(填序号)。
①检查装置的气密性 ②关闭K2,打开K1,使装置A中的反应先进行一段时间
③连接仪器 ④关闭K1,打开K2
(5)若装置E在反应前后的质量分别为30.1g和31.2g,则该固体样品中Cu2O的质量分数为__________。
指出该装置的不足之处,说明不足的理由并绐出改进方案__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com