
【题目】叠氮酸(HN3)与醋酸的酸性相似,0.2 mol HN3与0.2 mol NaOH反应后将溶液稀释至500 mL,测得溶液pH=a,下列说法一定错误的是( )
A.HN3水溶液中微粒浓度大小顺序为c(HN3)>c(H+)>c(N3—)>c(OH-)
B.题示500 mL溶液中离子浓度大小顺序为c(Na+)>c(N3—)>c(OH-)>c(H+)
C.题示500 mL溶液中由水电离产生的c(OH-)=1×10-amol·L-1
D.根据题给数据可以计算该温度下叠氮酸的电离平衡常数Ka
【答案】C
【解析】
A. 叠氮酸与醋酸的酸性相似,则叠氮酸是弱酸,其电离程度很小,水溶液中叠氮酸和水都电离生成氢离子,只有HN3电离生成N3,所以离子浓度大小顺序是c(HN3)>c(H+)>c(N3—)>c(OH-),故A正确;
B. 强碱弱酸盐NaN3水解导致溶液显碱性,离子浓度大小顺序为c(Na+)>c(N3-)>c(OH)>c(H+),故B正确;
C. 强碱弱酸盐NaN3水解,溶液pH=α,c(H+)=1×10αmolL1,由水电离产生的c(OH)=1×10(14a)molL1,故C错误;
D. 据溶液pH和水的离子积常数可以求得氢离子和氢氧根离子浓度,因为叠氮酸根离子的水解,叠氮酸分子浓度为氢氧根离子浓度与氢离子浓度差,钠离子浓度不变,为![]() =0.4mol/L,据电荷守恒,c(Na+)+c(H+)=c(N3)+c(OH)可以求得叠氮酸根离子浓度,进而求得Ka,故D正确;
=0.4mol/L,据电荷守恒,c(Na+)+c(H+)=c(N3)+c(OH)可以求得叠氮酸根离子浓度,进而求得Ka,故D正确;
故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知:H2(g)+I2(g) ![]() 2HI(g) H=-149kJ/mol。在甲、乙两个体积相同的密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。
2HI(g) H=-149kJ/mol。在甲、乙两个体积相同的密闭容器中充入反应物,保持恒温恒容,其起始浓度如下表所示。
起始 浓度 | c(H2)(mol/L) | c(I2)(mol/L) | c(HI)/(mol/L) |
甲 | 0.01 | 0.01 | 0 |
乙 | 0.02 | 0.02 | 0 |
甲中反应达到平衡时,测得c(H2)=0.008 mol/L下列判断正确的是( )
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) ![]() 2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
温度/体积分数/压强 | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | B |
915 | c | 75.0 | D |
1000 | E | f | 83.0 |
①b<f ②915 ℃、2.0 MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1 000 ℃)>K(810 ℃) 上述①~④中正确的 ( )
A.①②B.②③C.②③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】800°C时,在2L密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g) H<0,测得n(NO)随时间的变化如下表:
2NO2(g) H<0,测得n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)NO的平衡浓度c(NO)=____________________。
(2)下图中表示NO2的变化的曲线______________。(填字母)
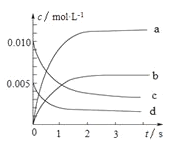
(3)能说明该反应已经达到化学平衡状态的是______________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=v正(O2) D.容器内NO、O2、NO2同时存在
(4)下列操作中,能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
A.及时分离出NO2气体B.适当升高温度
C.增大O2的浓度D.选择高效的催化剂
(5)下图中的曲线表示的是其它条件一定时,体系中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示v(正)<v(逆)的点是____________。(填选项)
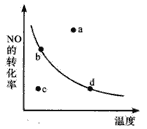
A.a B.b C.c D.d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表格中的各种情况,可以用对应选项中的图像表示的是
选项 | 反应 | 甲 | 乙 |
A | 外形、大小相近的金属和水反应 | Na | K |
B | 4mL0.01mol·L-1 KMnO4溶液分别和不同浓度的2mLH2C2O4(草酸)溶液反应 | 0.1mol·L-1的H2C2O4溶液 | 0.2mol·L-1的H2C2O4溶液 |
C | 5mL0.1mol·L-1Na2S2O3溶液和5mL0.1mol·L-1H2SO4溶液反应 | 热水 | 冷水 |
D | 5mL4%的过氧化氢溶液分解放出O2 | 无MnO2粉末 | 加MnO2粉末 |
A.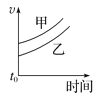 B.
B.
C. D.
D.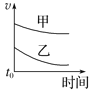
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】炼铁的还原剂CO是由焦炭和CO2反应而得。现将焦炭和CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)![]() 2CO(g) △H=Q kJ/mol。图为CO2、CO的物质的量n随时间t的变化关系图。下列说法正确的是
2CO(g) △H=Q kJ/mol。图为CO2、CO的物质的量n随时间t的变化关系图。下列说法正确的是
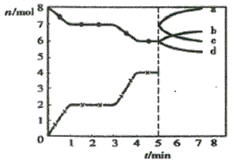
A.0~1min,v(CO)=1 mol/(L·min);1~3min时,v(CO)=v(CO2)
B.当容器内的压强不变时,反应一定达到平衡状态,且![]()
C.3min时温度由T1升高到T2,则Q>0,再达平衡时![]()
D.5min时再充入一定量的CO,a、d曲线分别表示n(CO)、n(CO2)的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性。将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、9.6、3.7。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
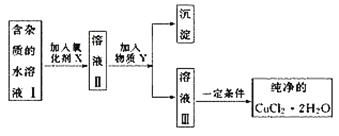
请回答下列问题:
(1)本实验最适合的氧化剂X是___(填序号)。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)物质Y是____。
(3)本实验用加碱沉淀法能不能达到目的?___,原因是___。
(4)除去Fe3+的有关离子方程式是____。
(5)加氧化剂的目的是____。
(6)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体___,应如何操作___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在400℃时,将一定量的SO2和14molO2压入一个盛有催化剂的10L密闭容器中进行反应:2SO2+O2![]() 2SO3,已知2min后,容器中剩余2molSO2和12molO2,则:
2SO3,已知2min后,容器中剩余2molSO2和12molO2,则:
①生成了__molSO3,SO2的起始物质的量浓度是__。
②2min内平均反应速率:v(O2)=__。
(2)某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
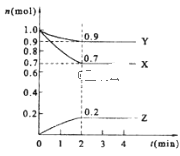
①X的转化率是__;
②由图中所给数据进行分析,该反应的化学方程式为___;
③若三种物质都是气体,则平衡时Y所占体积的百分比为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图示的说法正确的是

A. 图甲表示CH4 (g)+2O2 (g)=CO2 (g)+2H2O(1)的能量变化
B. 图乙表示压强对2A(g)+2B(g)![]() 3C(g)+D(g)的影响,且压强:P甲>P乙
3C(g)+D(g)的影响,且压强:P甲>P乙
C. 图丙表示温度对N2 (g)+3H2(g)![]() NH3 (g) △H<0的影响
NH3 (g) △H<0的影响
D. 图丁表示N2 (g)+3H2(g)![]() 2NH3 (g)平衡时NH3体积分数随起始n(N2)/n(H2)的变化,则转化率:αA(H2)=αB(H2)
2NH3 (g)平衡时NH3体积分数随起始n(N2)/n(H2)的变化,则转化率:αA(H2)=αB(H2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com