
【题目】硫代硫酸钠又名大苏打、海波,可以用于治疗氰化物中毒等,某化学兴趣小组通过查阅资料,设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体并探究其性质。

已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l) ;S(s)+Na2SO3(aq) ![]() Na2S2O3(aq)
Na2S2O3(aq)
(1)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有_________________________(写一条)
(2)常温下,用pH试纸测定0.1 mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是_______________________________。
(3)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子方程式_____________________。
【答案】 调节硫酸的滴加速度 用洁净的玻璃棒蘸取待测液点在pH试纸上,与标准比色卡对照,读出溶液的pH值 S2O32-+4Cl2+5H2O=2SO42-+10H++8Cl-
【解析】A中的Na2SO3中加入浓硫酸生成SO2,装置B的作用之一是观察SO2的生成速率,为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,烧瓶C中发生反应如下:Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq);2H2S(aq)+SO2(g)=3S(s)+2H2O(l);S(s)+Na2SO3(aq)![]() Na2S2O3(aq),反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O35H2O,E中盛放NaOH溶液进行尾气处理,防止含硫化合物排放在环境中。
Na2S2O3(aq),反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O35H2O,E中盛放NaOH溶液进行尾气处理,防止含硫化合物排放在环境中。
(1)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以通过调节硫酸的滴加速度控制SO2生成速率,故答案为:调节硫酸的滴加速度;
(2)常温下,用pH试纸测定0.1 mol·L-1 Na2S2O3溶液pH值约为8,测定的具体操作为:用洁净的玻璃棒蘸取待测溶液点在pH试纸中段,与标准比色卡对照,读出溶液的pH值,故答案为:用洁净的玻璃棒蘸取待测溶液点在pH试纸中段,与标准比色卡对照,读出溶液的pH值;
(3)氯气具有强氧化性,可氧化S2O32-生成硫酸根离子,反应的离子方程式为S2O32-+4Cl2+5H2O=2SO42-+10H++8Cl-,故答案为:S2O32-+4Cl2+5H2O=2SO42-+10H++8Cl-。


科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)为紫黑色粉末,是一种新型高效消毒剂。K2FeO4易溶于水,微溶于浓KOH溶液,在0 ℃~5 ℃的强碱性溶液中较稳定。一般制备方法是先用Cl2与KOH溶液在20 ℃以下反应生成KClO(在较高温度下则生成KClO3),KClO再与KOH、Fe(NO3)3溶液反应即可制得K2FeO4。实验装置如图所示:
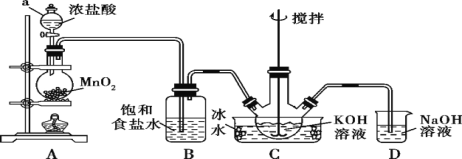
回答下列问题:
(1)制备KClO。
①仪器a的名称是________________;装置B吸收的气体是________。
②装置C中三颈烧瓶置于冰水浴中的目的是______________;装置D的作用是_____________。
(2)制备K2FeO4。
①装置C中得到足量KClO后,将三颈烧瓶上的导管取下,加入KOH溶液、Fe(NO3)3溶液,水浴控制反应温度,搅拌,当溶液变为紫红色,该反应的离子方程式为________________________________。
②向装置C中加入饱和________溶液,析出紫黑色晶体,过滤。
(3)测定K2FeO4纯度。测定K2FeO4的纯度可用滴定法,滴定时有关反应的离子方程式为:
a.FeO42-+CrO2-+2H2O═CrO42-+Fe(OH)3↓+OH-
b.2CrO42-+2H+═Cr2O72-+H2O
c.Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O
称取2.0g制备的K2FeO4样品溶于适量KOH溶液中,加入足量的KCrO2,充分反应后过滤,滤液在250mL容量瓶中定容.取25.00mL加入稀硫酸酸化,用0.10 molL-1的(NH4)2Fe(SO4)2标准溶液滴定至终点,重复操作2次,平均消耗(NH4)2Fe(SO4)2溶液的体积为24.00mL,则该K2FeO4样品的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(s)+2B(g)===C(g)+D(g),在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A. 增加B的浓度
B. 将容器的体积缩小一半
C. 保持压强不变,充入He使容器体积增大
D. 保持体积不变,充入He使体系压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质按单质、氧化物、酸、碱分类顺序排列,其中正确的是
A. 氧气、干冰、硫酸、烧碱 B. 碘酒、冰、盐酸、烧碱
C. 氢气、二氧化硫、硝酸、纯碱 D. 铜、硫酸钠、醋酸、石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素形成的酸有硝酸、亚硝酸(HNO2)等,其中HNO2为一元弱酸。
(1)写出HNO2溶液与NaOH溶液反应的离子方程式:______;
(2)亚硝酸钠(NaNO2)像食盐一样有咸味,但有很强的毒性,误食NaNO2会使人中毒。已知亚硝酸钠能发生如下反应:2NaNO2 + 4HI ═ 2NO↑ + 2NaI + I2 + 2H2O,该反应被氧化的元素是______,
(3)实验室需配制0.1molL﹣1的NH4NO3溶液500mL。
①配制时,应用托盘天平称取NH4NO3的质量为_______;
②定容时俯视刻度线,所配得溶液的浓度________(填“偏高”、“偏低”或“无影响”);
(4)在浓硝酸中放入铜片:若将12.8 g铜跟一定量的浓硝酸反应,铜消耗完时,共产生5.6 L(标准状况)气体,则所消耗的HNO3的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应3NO2+H2O=2HNO3+NO中,若NA为阿伏加德罗常数,下列说法正确的是
A.NO2只是氧化剂B.H2O既不是氧化剂,也不是还原剂
C.NO2只是还原剂D.每生成1mol NO,转移1 NA电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组比较Cl-、Br-、I- 的还原性,实验如下:
实验1 | 实验2 | 实验3 | |
装置 |
|
|
|
现象 | 溶液颜色无明显变化;把蘸浓氨水的玻璃棒靠近试管口,产生白烟 | 溶液变黄;把湿KI淀粉试纸靠近试管口,变蓝 | 溶液变深紫色;经检验溶液含单质碘 |
下列对实验的分析不合理的是
A. 实验1中,白烟是NH4Cl B. 根据实验1和实验2判断还原性:Br->Cl-
C. 根据实验3判断还原性:I->Br- D. 上述实验利用了浓H2SO4的强氧化性、难挥发性等性质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
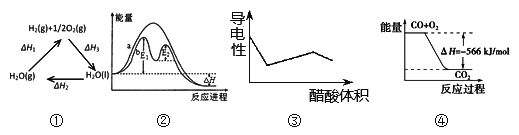
A. 图①中△H1=△H2+△H3
B. 图②在催化剂条件下,反应的活化能等于E1+E2
C. 图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的导电性变化曲线
D. 图④可表示由CO(g)生成CO2(g)的反应过程和能量关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由Al、Ca、Cu、Fe 四种金属元素组成,回答下列问题:
(1)基态Fe原子有_______个未成对电子,Fe3+的价电子排布式为__________。
(2)新制的Cu(OH)2可将乙醛氧化成乙酸,而自身还原成Cu2O。乙醛分子中含有的σ键与π键的比例为___。乙醛中碳原子的杂化轨道类型为_____,配合物[Cu(NH3)4](OH)2中含有的化学键类型有_________,1 mol该物质中有______个σ键。
(3)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______个铜原子。
(4)CaCl2熔点高于AlCl3的原因__________________________________。
(5)CaF2晶胞如图所示,已知:氟化钙晶体密度为ρg·cm-3,NA代表阿伏加德罗常数的值。氟化钙晶体中Ca2+和F-之间最近核间距(d)为______________pm(只要求列出计算式即可)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com