
【题目】下列说法正确的是
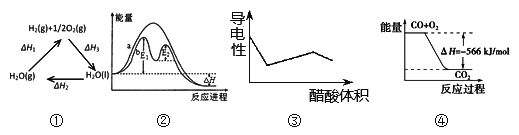
A. 图①中△H1=△H2+△H3
B. 图②在催化剂条件下,反应的活化能等于E1+E2
C. 图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的导电性变化曲线
D. 图④可表示由CO(g)生成CO2(g)的反应过程和能量关系
【答案】C
【解析】A.根据盖斯定律来分析;B.催化剂改变了反应历程, E1、E2分别代表各步反应的活化能;C.醋酸和一水合氨是弱电解质,在溶液里部分电离,氢氧化钠是强电解质,完全电离,向混合溶液中滴加醋酸,醋酸先和氢氧化钠反应生成强电解质醋酸钠,氢氧化钠完全反应后,醋酸再和氨水反应生成强电解质醋酸铵,根据溶液中离子浓度变化与电导率的关系分析解答;D.表示由CO(g)生成CO2(g)的反应能量关系,并不能表示反应过程。
根据盖斯定律可知△H3=-(△H1+△H2)则△H1=-(△H3+△H2),A错误;因为E1>E2图②在催化剂条件下,反应的活化能等于E1,B错误;NaOH 和氨水混合溶液滴入醋酸,NaOH先与醋酸反应生成醋酸钠,氢氧化钠与醋酸钠均为强电解质且离子带电荷数相同,但加入醋酸溶液体积增大,单位体积内电荷数目减少,故溶液导电能力减弱,当氢氧化钠反应完毕滴加醋酸,氨水与醋酸反应生成醋酸铵,醋酸铵为强电解质,一水合氨为弱电解质,故随着醋酸滴入溶液导电能力逐渐增大,当氨水反应完后加入醋酸溶液体积增大,故溶液导电能力逐渐减小,C正确;D项图④只表示由CO(g)生成CO2(g)的反应能量关系,并不能表示反应过程,D错误;正确选项C。


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
I.将 NaOH溶液与 NH4Cl 溶液混合生成 NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_________。
II.根据下图所示装置图回答以下问题。
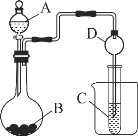
(1)实验室中现有药品Na2S、KMnO4、浓盐酸,某同学验证氯的非金属性大于硫,请写出试管中发的离子反应方程式______
(2)甲同学根据元素非金属性与对应最高价含氧酸之间关系,设计了如图装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;写出选用物质的名称:A__,B__,C___;上述反应的离子方程式_____;_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠又名大苏打、海波,可以用于治疗氰化物中毒等,某化学兴趣小组通过查阅资料,设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体并探究其性质。

已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l) ;S(s)+Na2SO3(aq) ![]() Na2S2O3(aq)
Na2S2O3(aq)
(1)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有_________________________(写一条)
(2)常温下,用pH试纸测定0.1 mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是_______________________________。
(3)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子方程式_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气污染问题日益引起全民关注。
(1)PM2.5是指大气中直径小于或等于2.5μm(1μm =103 nm)的颗粒物。下列说法不正确的是______(填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1 ~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)北京科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2。

①硫酸型酸雨的形成过程是大气中的SO2溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式依次为__________________、_________________。
②CaSO4可以调节水泥的硬化时间。尾气中SO2与石灰乳反应生成CaSO4的化学方程式为_________。
③Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式_______________。
(3)工业上利用NO电解制备NH4NO3,其工作原理如下图所示,阳极的电极反应为________________,阴极的电极反应为__________________________,为使电解产物全部转化为NH4NO3,需补充物质A,A可以是______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学活动小组欲制备一定量的氢气,下列方法不能达到目的的是( )
A.Cu和浓硝酸反应B.Zn和稀盐酸反应
C.Fe和稀硫酸反应D.A1和稀盐酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用硫铁矿烧渣(主要含 Fe2O3、SiO2 等)制备碱式硫酸铁[Fea(OH)b (SO4)c]溶液, 并测定其组成。

(1)酸浸时反应的化学方程式为___。
(2)操作 a 的名称为___,X 为___(填化学式)。
(3)加 CaCO3 调节溶液的 pH,其目的是中和溶液中的酸,并使 Fe2(SO4)3 转化为 Fea(OH)b (SO4)c。若溶 液的 pH 偏高,将会导致溶液中铁元素的含量降低,其原因是___(用文字表述)。
(4)为测定碱式硫酸铁的组成,取一定量样品与足量盐酸反应,所得溶液平均分为两份。一份溶液中加入足量的 BaCl2 溶液,得到白色沉淀 1.7475 g。另一份溶液,先将 Fe3+还原为 Fe2+,充分反应后向溶液中滴加 0.02000 mol·L-1 K2 Cr2O7溶液,完全反应时消耗K2 Cr2O7溶液 50.00 mL。求该样品的化学式(已知:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O)__________________。(请写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、E、F五种常见物质含有同一元素M,在一定条件下它们有如下转化关系,Z是NO,下列推断不合理的是:

A. X可能是一种氢化物
B. 若Y为单质,Y生成Z属于化合反应
C. E可能是一种有色气体
D. F中M元素的化合价可能为+5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com