
【题目】某有机化合物与金属钠反应放出氢气,充分燃烧8.88 g该有机物,将燃烧后的气体通入浓硫酸,浓硫酸质量增加10.8 g;将剩余气体通入NaOH溶液,溶液质量增加21.12 g。由质谱仪测得此种有机物的相对分子质量为74。该有机物在浓硫酸的作用下发生消去反应时能生成两种有机产物。则该有机物可能的结构简式为 ( )
A. CH3CH2CH2CH2OH
B. CH3CH2CHOHCH3
C. (CH3)2CHCH2OH
D. (CH3)3COH
【答案】B
【解析】
有机物的相对分子质量为74,8.88 g该有机物的物质的量是![]() 0.12mol;燃烧后的气体通入浓硫酸,浓硫酸质量增加10.8 g,则水的物质的量是
0.12mol;燃烧后的气体通入浓硫酸,浓硫酸质量增加10.8 g,则水的物质的量是![]() ,将剩余气体通入NaOH溶液,溶液质量增加21.12 g,则二氧化碳的物质的量是
,将剩余气体通入NaOH溶液,溶液质量增加21.12 g,则二氧化碳的物质的量是![]() ;根据有机物燃烧通式、及相对分子质量可计算其分子式;再根据性质推出结构式。
;根据有机物燃烧通式、及相对分子质量可计算其分子式;再根据性质推出结构式。
设有机物的分子式是CxHyOz,则
CxHyOz+(x+![]() -
-![]() )O2
)O2![]() xCO2+
xCO2+![]() H2O
H2O
1 x ![]()
0.12 0.48 0.6
![]()
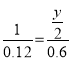
x=4 ,y=10
12×4+1×10+16z=74,z=1;
所以该有机物的分子式是C4H10O;该有机物与金属钠反应放出氢气说明含有羟基,CH3CH2CH2CH2OH消去反应的产物有1种、CH3CH2CHOHCH3消去反应的产物有2种、(CH3)2CHCH2OH消去反应的产物有1种、(CH3)3COH消去反应的产物有1种,故选B。


科目:高中化学 来源: 题型:
【题目】能够充分说明在恒温下的密闭容器中,反应2SO2+O2![]() 2SO3已达平衡状态的标志是
2SO3已达平衡状态的标志是
A. 容器中SO2.O2.SO3的物质的量之比为2:1:2
B. SO2 和SO3的物质的量浓度相等
C. 单位时间内生成2molSO3 时,即消耗1molO2
D. 反应容器内压强不随时间变化而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电炉加热时用纯氧氧化管内样品,根据产物的质量确定有机物的组成,下列装置是用燃烧法确定有机物分子式常用的装置。
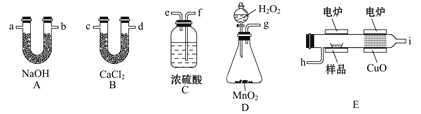
(1)产生的氧气按从左到右的流向,所选装置各导管的连接顺序是___________。
(2)C装置中浓H2SO4的作用是________。
(3)D装置中MnO2的作用是_____________。
(4)燃烧管中CuO的作用是______________。
(5)若准确称取0.90 g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32g,B管质量增加0.54 g,则该有机物的实验式为_______。
(6)要确立该有机物的分子式,还要知道___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
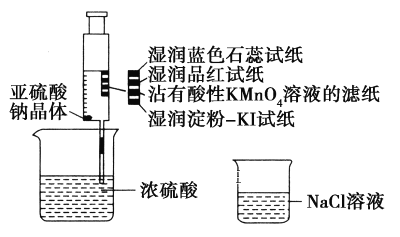
A. 蓝色石蕊试纸先变红后褪色
B. 品红试纸、沾有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性
C. 湿润淀粉-KI试纸未变蓝说明SO2的氧化性弱于I2
D. NaCl溶液可用于除去实验中多余的SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X是一种新型无机非金属材料,具有耐磨、耐腐蚀、抗冷热冲击性。有关生产过程如下:
![]()
为了确定C的组成,某同学进行了以下的探究过程。已知F、G都是难溶于水和稀硝酸的白色沉淀,I可作光导纤维。
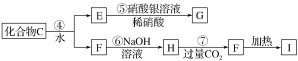
按要求回答下列问题:
(1)C的化学式为________;X的化学式为________。
(2)写出下列方程式:
反应②的化学方程式_________________________________________________;
反应⑦的离子方程式_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Cu和CuO的混合物中加入0.6 L 2.0 mol/L的稀硝酸,混合物完全溶解,同时生成标准状况下NO 4.48 L。向所得溶液中加入一定体积1.0 mol/L NaOH溶液,恰好使Cu2+完全沉淀,将沉淀洗涤,充分灼烧后得32.0 g固体。求:
(1)混合物中Cu的质量是____________。
(2)混合物消耗HNO3的物质的量是____________。
(3)NaOH溶液的体积是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙炔衍生物分子M的结构简式及M在稀硫酸作用下的水解反应如图所示。下列有关说法不正确的是 ( )
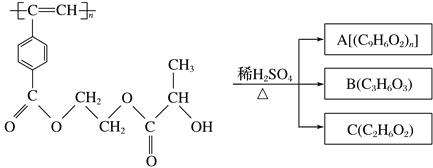
M
A. M与A均能使酸性高锰酸钾溶液和溴水褪色
B. B中含有羧基和羟基两种官能团,能发生消去反应和酯化反应
C. 1 mol M与热的烧碱溶液反应,可消耗2n mol NaOH
D. A、B、C各1 mol分别与金属钠反应,放出气体的物质的量之比为1∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,使H2和O2的混合气体26g充分发生反应,所得产物在适当温度下跟足量的固体Na2O2反应,使固体增重2g。原混合气体中H2和O2的物质的量之比为( )
A.1:10B.9:1C.4:1D.4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,体积均为20 mL、浓度均为0.1mol/L的两种酸HX、HY分别与0.1mol/L的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是( )
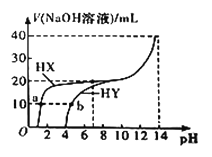
A. 加入10 mL NaOH溶液时,a点c(X)<b点c(Y)
B. HY中加NaOH溶液至pH=7时,所得溶液中c(Y)=c(Na+)=c(OH)=c(H+)
C. b点溶液中,c(Y)+2c(OH)=c(HY)+2c(H+)
D. 25℃时,HX为强酸,HY为弱酸且Ka=108
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com