
【题目】如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是( )
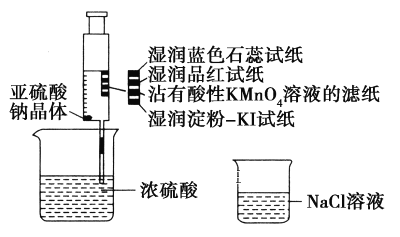
A. 蓝色石蕊试纸先变红后褪色
B. 品红试纸、沾有酸性KMnO4溶液的滤纸均褪色,证明SO2具有漂白性
C. 湿润淀粉-KI试纸未变蓝说明SO2的氧化性弱于I2
D. NaCl溶液可用于除去实验中多余的SO2
【答案】C
【解析】
浓硫酸具有强酸性、吸水性,亚硫酸钠是一种弱酸盐,亚硫酸钠能与浓硫酸反应:Na2SO4+H2SO4=Na2SO4+SO2![]() +H2O,吸入少量浓硫酸后,注射器中充满了干燥的SO2气体,SO2具有还原性、漂白性、具有酸性氧化物的通性等性质,由此分析。
+H2O,吸入少量浓硫酸后,注射器中充满了干燥的SO2气体,SO2具有还原性、漂白性、具有酸性氧化物的通性等性质,由此分析。
浓硫酸具有强酸性、吸水性,亚硫酸钠是一种弱酸盐,亚硫酸钠能与浓硫酸发生反应:Na2SO4+H2SO4=Na2SO4+SO2![]() +H2O,吸入少量浓硫酸后,注射器中充满了干燥的SO2气体。
+H2O,吸入少量浓硫酸后,注射器中充满了干燥的SO2气体。
A. SO2溶解在湿润试纸的水溶液里生成H2SO3,H2SO3属于中强酸使石蕊变红,但SO2不能漂白指示剂,所以试纸变红后不会褪色,A项错误;
B.SO2使品红试纸褪色能证明SO2具有漂白性;SO2与酸性KMnO4能发生氧化还原反应:5SO2+2MnO4-+ 2H2O=5SO42-+2Mn2++ 4H+,SO2将紫色的MnO4-还原为几乎为无色的Mn2+而使滤纸褪色,所以SO2使沾有酸性KMnO4溶液的滤纸褪色不能证明SO2具有漂白性,B项错误;
C.湿润淀粉KI试纸未变蓝,说明SO2不能将I-氧化为I2,弱氧化剂不能制取强氧化剂所以SO2的氧化性弱于I2,C项正确;
D.SO2是一种大气污染物,多余的SO2通常用NaOH溶液吸收,NaCl不跟SO2反应且SO2不能完全被水吸收,所以不能用NaCl溶液吸收多余的SO2,D项错误;答案选C。


科目:高中化学 来源: 题型:
【题目】地球上的物质不断变化,数10亿年来大气的成分也发生了很大的变化。下表是原始大气和目前空气的主要成分:
目前空气的成分 | N2、O2、CO2、水蒸气及稀有气体(如He、Ne等) |
原始氮气的主要成分 | CH4、NH3、CO、CO2等 |
用上表所涉及的分子填写下列空白。
(1)含有10个电子的分子有(填化学式,下同)______________________;
(2)由极性键构成的非极性分子有____________________;
(3)与H+可直接形成配位键的分子有________;
(4)沸点最高的物质是________,用所学的知识解释其沸点最高的原因_____________;
(5)分子中不含孤电子对的分子(稀有气体除外)有________,它的立体构型为________;
(6)极易溶于水、且水溶液呈碱性的物质的分子是________,它之所以极易溶于水是因为它的分子和水分子之间形成________;
(7)CO的结构可表示为O![]() C,与CO结构最相似的分子是________,这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个键不同,它叫________。
C,与CO结构最相似的分子是________,这两种结构相似的分子中,分子的极性________(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个键不同,它叫________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元弱碱B(OH)2(K1=5.9×10-2、K2=6.4×10-5)。向10mL稀B(OH)2溶液中滴加等浓度盐酸,B(OH)2、B(OH)+、B2+的浓度分数![]() 随溶液pOH[pOH=-lgc(OH-)]变化的关系如图,以下说法正确的是
随溶液pOH[pOH=-lgc(OH-)]变化的关系如图,以下说法正确的是
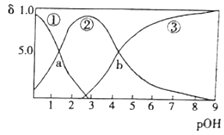
A.交点a处对应加入的盐酸溶液的体积为5mL
B.当加入的盐酸溶液的体积为10mL时存在c(Cl-)>c(B(OH)+)>c(H+)>c(OH-)>c(B2+)
C.交点b处c(OH-)=6.4×l0-5
D.当加入的盐酸溶液的体积为15mL时存在:c(Cl-)+c(OH-)>c(H+)>c(OH-)>c(B2+)+ c(B(OH)+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源与材料、信息被称为现代社会发展的三大支柱,化学与能源有着密切联系。
(1)下表中的数据表示破坏1mol化学键需消耗的能量(即键能,单位为kJmol-1)
化学键 | H-H | Cl-Cl | H-Cl |
键能/(kJmol-1) | 436 | 243 | 431 |
根据以上信息可知,1molH2在足量的氯气中燃烧生成氯化氢气体放出的热量是_______
(2)工业上有一种方法是用CO2来生产燃料甲醇,可以将CO2变废为宝。在体积为1L的密闭容器中充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示:
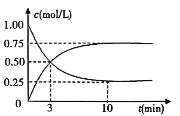
①从反应开始到平衡,CH3OH的平均反应速率υ(CH3OH)=_______________。
②若反应CO2(g)+3H2(g)CH3OH(g)+H2O(g)在四种不同情况下的反应速率分别为:
A.υ(CO2)=0.15molL-1min-1 B.υ(H2)=0.01molL-1s-1
C.υ(CH3OH)=0.2molL-1min-1 D.υ(H2O)=0.45molL-1min-1
该反应进行由快到慢的顺序为___________(填字母)
(3)海水化学资源的利用具有非常广阔的前景,从海水中提取溴的工业流程如图所示:
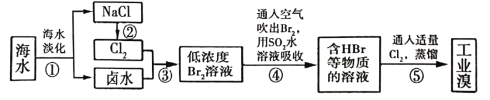
①以上五个过程中涉及氧化还原反应的有_____________个。
②步骤③中已获得游离态的溴,步骤④又随之转变成化合态的溴,其目的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的实验装置中,盛有足量水的水槽里放两个烧杯,小烧杯里放有适量铜片和过量硝酸,小烧杯外面倒扣一大烧杯,请回答下列问题:
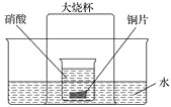
(1)实验过程中,观察到的主要现象是:
①____________________;
②_____________;
③________________;
④_____________________。
(2)用该装置做铜与浓硝酸反应的实验,最突出的特点是:_____________________。
(3)若要验证最终得到的气体生成物,最简便的方法是_______________。
(4)工业上吸收NO和NO2的混合气体,常使用NaOH溶液(NO+NO2+2NaOH===2NaNO2+H2O)。欲使NO和NO2被充分吸收,则NO和NO2的体积应满足________。
A V(NO)>V(NO2)
B V(NO)<V(NO2)
C V(NO)≤V(NO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键的断裂和新键的形成过程。化学键的键能是形成化学键时释放的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198P—O:360O=O:498,则反应P4(白磷)+3O2=P4O6的反应热ΔH为 ( )
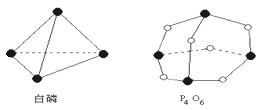
A. -1638 kJ·mol-1B. +1638 kJ·mol-1C. -126 kJ·mol-1D. +126 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物与金属钠反应放出氢气,充分燃烧8.88 g该有机物,将燃烧后的气体通入浓硫酸,浓硫酸质量增加10.8 g;将剩余气体通入NaOH溶液,溶液质量增加21.12 g。由质谱仪测得此种有机物的相对分子质量为74。该有机物在浓硫酸的作用下发生消去反应时能生成两种有机产物。则该有机物可能的结构简式为 ( )
A. CH3CH2CH2CH2OH
B. CH3CH2CHOHCH3
C. (CH3)2CHCH2OH
D. (CH3)3COH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,对此装置的下列说法正确的是( )

A. 外电路的电流方向为:X→外电路→Y
B. 若两电极分别为Zn和石墨棒,则X为石墨棒,Y为Zn
C. SO42-移向X电极,Y电极上有氢气产生
D. X极上发生的是还原反应,Y极上发生的是氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2010年美、日三位科学家因钯(Pd)催化的交叉偶联反应获诺贝尔化学奖。一种钯催化的交叉偶联反应如下:
![]() (R、R’为烃基或其他基团),应用上述反应原理合成防晒霜主要成分K的路线如下图所示(部分反应试剂和条件未注明):
(R、R’为烃基或其他基团),应用上述反应原理合成防晒霜主要成分K的路线如下图所示(部分反应试剂和条件未注明):

已知:① B能发生银镜反应,1 mol B 最多与2 mol H2反应。
② C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与NaHCO3反应生成CO2,其消去产物的分子中只有一个碳原子上没有氢。
③ G不能与NaOH溶液反应。
④核磁共振图谱显示J分子有3种不同的氢原子。
请回答:
(1)B中含有的官能团的名称是______________________________
(2)B→D的反应类型是___________
(3)D→E的化学方程式是_________________________________________
(4)有机物的结构简式:G_______________________; K__________________________
(5)符合下列条件的X的同分异构体有(包括顺反异构)_____种,其中一种的结构简式是__________。
a.相对分子质量是86 b.与D互为同系物
(6)分离提纯中间产物E的操作:先用碱除去D和H2SO4,再用水洗涤,弃去水层,最终通过________操作除去C8H17OH,精制得E。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com