
【题目】目前人们对环境保护、新能源开发很重视。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体。
4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
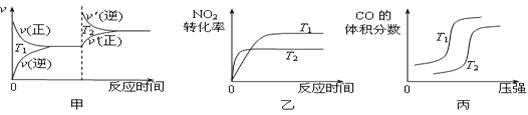
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 (填代号)。
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s) + 2NO(g) ![]() N2(g) + CO2(g) ΔH在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g) + CO2(g) ΔH在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(CO
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是 (填字母代号)。
A.加入一定量的活性炭 B.通入一定量的NO
C.适当缩小容器的体积 D.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率 (填“升高”或“降低”),ΔH 0(填“>”或“<”).
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -l59.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式 。
(4)一种氨燃料电池,使用的电解质溶液是2mol/L的KOH溶液。
电池反应为:4NH3+3O2=2N2+6H2O;
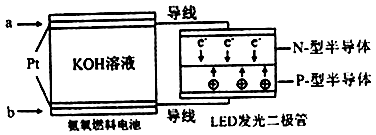
请写出通入a气体一极的电极反应式为 ;每消耗3.4g NH3转移电子的物质的量为 。
【答案】(1)乙;
(2)①0.015mol·L-1·min-1;0.56(或9/16)②bc;③降低;<;
(3)2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)ΔH=–87.0kJ·mol-1
(4)2NH3+6OH-–6e-=N2+6H2O 0.6mol
【解析】
试题分析:(1)甲:升高温度,化学平衡逆向移动,化学反应速率会迅速增大,会离开原来的速率点,错误;乙:升高温度,化学反应速率会迅速增大,所以T2 时先达到化学平衡状态,并且由于该反应的正反应是放热反应,所以升高温度,化学平衡向吸热的逆反应方向移动,使二氧化氮的转化率减小,正确;丙:对于该反应来说,正反应是气体体积减小的反应,在温度不变时,增大压强,平衡正向移动,一氧化碳的体积分数会减小,错误;(2) ①根据表格数据可知:在20min内CO2的浓度增大0.30mol/L,则用CO2的浓度改变表示反应速率是V(CO2)=0.30mol/L÷20min=0.015mol/(L·min);反应达到平衡时,各种物质的浓度分别是:c(NO)=0.48mol/L;c(N2)=c(CO2)=0.36mol/L,所以在该温度下的化学平衡常数K= c(N2)·c(CO2)÷c2(NO)= (0.36mol/L ×0.36mol/L )÷(0.48mol/L)2=9/16=0.56;②30min后,只改变某一条件,反应重新达到平衡,依据图表数据分析,平衡状态各物质浓度增大,而平衡常数只随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积或加入一定量一氧化氮;故答案为bc;③在原来平衡时,c(NO):c(N2):c(CO2)= 0.48:0.36:0.36=4:3:3,若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,氮气和二氧化碳浓度之比始终为1:1,所以5:3>4:3,说明平衡向逆反应方向移动,升高温度平衡逆向移动,根据平衡移动原理:升高温度,化学平衡向吸热的反应方向移动,说明逆反应是吸热反应,则正反应是放热反应,故△H<0;(3)依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ΔH= –87.0 kJ·mol-1;(4) 电池反应为:4NH3+3O2=2N2+6H2O.该电池负极是氨气失电子生成氮气,根据示意图可知a电极是负极,发生氧化反应,发生的电极反应式为2NH3+6OH-– 6e-=N2 + 6H2O,反应中2mol氨气反应电子转移6mol电子,每消耗3.4g NH3的物质的量=13.4g÷17g/mol=0.2mol,所以转移的电子数为0.36NA 。


科目:高中化学 来源: 题型:
【题目】某温度时,反应X(g)![]() 4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法不正确的是
4Y(g)+Z(g) ΔH=-Q kJ·mol-1在2 L恒容密闭容器中进行,X和Z的浓度随时间变化如图所示,下列说法不正确的是

A. 2 min内,X的平均反应速率为0.25 mol·L-1·min-1
B. 第t min时,该反应达到平衡状态
C. 第5 min后,X的生成速率与Z的生成速率相等且保持不变
D. 5 min内,反应放出的热量为1.6Q kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应①:CO(g)+CuO(s)CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)Cu(s)+H2O(g)在相同温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)CO2(g)+H2(g)的平衡常数为K.则下列说法正确的是
A. 反应①的平衡常数K1=![]()
B. 反应③的平衡常数K=![]()
C. 对于反应③,恒容时,若温度升高,H2的浓度减小,则该反应的焓变为正值
D. 对于反应②,恒温恒容时,若加入CuO,平衡向正向移动,H2的浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关W、X、Y、Z、R五种元素的叙述正确的是( )
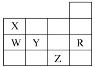
A. 常温下,Z的单质为气态物质
B. Y、Z的阴离子的电子层结构都与R原子的相同
C. W的氢化物的稳定性要比X的强
D. Y的元素的非金属性比W元素强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应2AB+3C,在下列四种状态中,处于平衡状态的是( )
选项 | 正反应速率 | 逆反应速率 |
A | vA=2 mol·L-1·min-1 | vB=2 mol·L-1·min-1 |
B | vA=2 mol·L-1·min-1 | vC=2 mol·L-1·min-1 |
C | vA=1 mol·L-1·min-1 | vB=2 mol·L-1·min-1 |
D | vA=1 mol·L-1·min-1 | vC=1.5 mol·L-1·min-1 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与阿伏加德罗常数的值( NA)有关的说法正确的是
A. 在标准状况下,2.24L水中含有氢原子的数目为2NA
B. 8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA
C. 在密闭容器中加入0.5 mol N2和1.5 mol H2,充分反应后可得到NH3分子数为NA
D. 2.3 g Na与氧气完全反应,反应中转移的电子数在0.1NA~0.2NA之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂,在山坡坑道的仓库里贮有氯气钢瓶。一天一只贮有氯气的钢瓶损坏,造成氯气泄漏,在场工人采取的措施正确的是
A.把钢瓶推到坡下的小河里B.把钢瓶扔到农田中
C.把钢瓶丢到深坑里,用石灰填埋D.钢瓶处理后,工人应转移到坡上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一定条件下,向容积为2L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),CH3OH(g) + H2O(g)![]() CO2(g) + 3H2(g)
CO2(g) + 3H2(g) ![]() H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
①达平衡时混合气体的压强是反应前的____________倍。
②该条件下反应达平衡状态的依据是(填序号)_______________。
A.v正(CH3OH)=v正(CO2) B.混合气体的密度不变
C.c(CH3OH)=c(H2O) D.混合气体的总物质的量不变
(2)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热Q kJ。则表示甲醇燃烧热的热化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A.Na2CO3用于制胃酸中和剂B.FeSO4用于制补铁剂
C.硬铝合金用于制造飞机和宇宙飞船D.14C用于测定文物年代
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com