
ҰңМвДүҰүПВБРТАңЭИИ»ҮС§·ҢіМКҢµГіцµДҢбВЫХэИ·µДКЗ
A. Иф2H2ӘЁgӘ©Ә«O2ӘЁgӘ©ӘҢ2H2OӘЁgӘ©¦¤HӘҢ-483Ә®6kJҰ¤molӘ1Ә¬ФтH2ИәЙХИИОҒ241Ә®8kJҰ¤molӘ1
B. ИфCӘЁКҮД«Ә¬sӘ©ӘҢCӘЁҢрёХКҮӘ¬sӘ©¦¤H>0Ә¬ФтКҮД«±ИҢрёХКҮОИ¶Ё
C. ТСЦҒNaOHӘЁaqӘ©Ә«HClӘЁaqӘ©ӘҢNaClӘЁaqӘ©Ә«H2OӘЁlӘ©¦¤HӘҢ-57Ә®4kJҰ¤molӘ1Ә¬Фт20Ә®0gNaOH№ММеУлПҰСОЛбНкИ«ЦРғНӘ¬·Еіц28Ә®7kJµДИИБү
D. ТСЦҒ2CӘЁsӘ©Ә«2O2ӘЁgӘ©ӘҢ2CO2ӘЁgӘ©¦¤H1Ә»2CӘЁsӘ©Ә«O2ӘЁgӘ©ӘҢ2COӘЁgӘ©¦¤H2Ә¬Фт¦¤H1>¦¤H2
Ұңөр°ёҰүB
ҰңҢвОцҰүКФМв·ЦОцӘғAӘ®СҰПоЦРЙъіЙµДЛ®КЗЖшМеӘ¬У¦ёГКЗТғМ¬Л®Ә¬ЛщТФІ»ДЬµГіцЗвЖшµДИәЙХИИКЗ241.8kJ/molӘ¬№КAөнОуӘ»BӘ®ТСЦҒC(КҮД«Ә¬s)=C(ҢрёХКҮӘ¬s)ҰчHӘң0Ә¬·өУ¦КЗОьИИ·өУ¦Ә¬КҮД«ДЬБүµНУЪҢрёХКҮӘ¬ДЬБүФҢµНФҢОИ¶ЁӘ¬ЛщТФКҮД«±ИҢрёХКҮОИ¶ЁӘ¬№КBХэИ·Ә»CӘ®ТСЦҒNaOH(ag)+HCl(aq)=NaCl(aq)+H2O(l)ҰчH=-57.4kJ/molӘ¬Фтғ¬20.0gNaOHОпЦКµДБүОҒ0.5molµДПҰИЬТғУлПҰСОЛбНкИ«ЦРғНӘ¬·Еіц28.7kJµДИИБүӘ¬№КCөнОуӘ»DӘ®ТСЦҒC(s)+O2(g)=CO2(g)ҰчH1ұЩӘ¬C(s)+ ![]() O2(g)=CO(g)ҰчH2ұЪӘ¬ұЩ-ұЪµГµҢӘғCO(g)+
O2(g)=CO(g)ҰчH2ұЪӘ¬ұЩ-ұЪµГµҢӘғCO(g)+ ![]() O2(g)=CO2(g)ҰчH1-ҰчH2Ә¬Т»Сх»ҮМәИәЙХЙъіЙ¶юСх»ҮМәКЗ·ЕИИ·өУ¦Ә¬мК±дКЗёғЦµӘ¬ЛщТФҰчH1ӘәҰчH2Ә¬№КDөнОуӘ¬№КСҰBҰӘ
O2(g)=CO2(g)ҰчH1-ҰчH2Ә¬Т»Сх»ҮМәИәЙХЙъіЙ¶юСх»ҮМәКЗ·ЕИИ·өУ¦Ә¬мК±дКЗёғЦµӘ¬ЛщТФҰчH1ӘәҰчH2Ә¬№КDөнОуӘ¬№КСҰBҰӘ


 іеөМ100·Ц1ғЕңнПµБРөр°ё
іеөМ100·Ц1ғЕңнПµБРөр°ё
| Дкә¶ | ёЯЦРүОіМ | Дкә¶ | іхЦРүОіМ |
| ёЯТ» | ёЯТ»Гв·СүОіМНЖәцӘҰ | іхТ» | іхТ»Гв·СүОіМНЖәцӘҰ |
| ёЯ¶ю | ёЯ¶юГв·СүОіМНЖәцӘҰ | іх¶ю | іх¶юГв·СүОіМНЖәцӘҰ |
| ёЯИэ | ёЯИэГв·СүОіМНЖәцӘҰ | іхИэ | іхИэГв·СүОіМНЖәцӘҰ |
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүёхКЗТ»ЦЦТш°ЧЙ«µДҢрКфӘ¬»ҮС§РФЦКОИ¶ЁӘ¬УГНң№г·ғҰӘ №¤ТµЙПТФёхМъүу[ЦчТҒіЙ·ЦКЗ Fe(CrO2)2]ОҒФБПТ±Б¶ёхә°»сµГЗүСх»ҮРФ Na2Cr2O7Ә¬Ж乤ТХБчіМИзПВНәЛщКңӘғ

 ӘЁ1Ә©Na2Cr2O7 ЦРёхФҒЛШµД»ҮғПәЫОҒ Ә¬ТСЦҒ Cr(OH)3 ОҒБҢРФЗвСх»ҮОпӘ¬РөіцЖдµзАл·ҢіМКҢ ҰӘ
ӘЁ1Ә©Na2Cr2O7 ЦРёхФҒЛШµД»ҮғПәЫОҒ Ә¬ТСЦҒ Cr(OH)3 ОҒБҢРФЗвСх»ҮОпӘ¬РөіцЖдµзАл·ҢіМКҢ ҰӘ
ӘЁ2Ә©РөіцАыУГВБИИ·өУ¦ЦЖИҰёхµД»ҮС§·ҢіМКҢ: Ә¬
КФәБ c НЁіӘ»№үЙТФКЗ (ЦБЙЩРөБҢЦЦ) ҰӘ
ӘЁ3Ә©Лб»Ү№эіМЦРӘ¬І»СҰУГСОЛбµДФТтКЗ ҰӘ
ӘЁ4Ә©№ММе a µДЦчТҒіЙ·ЦКЗ Na2SO4Ұ¤10H2OӘ¬ёщңЭУТНә·ЦОцӘ¬ІЩЧч aОҒ Ұұ Ұұ№эВЛҰӘ
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰү»рәэНЖҢшЖчЦРКұУРЗү»№ФәБТғМ¬лВӘЁN2H4Ә©ғНЗүСх»ҮәБТғМ¬N2O4ҰӘТСЦҒұЩ2O2ӘЁgӘ©+N2ӘЁgӘ©=N2O4ӘЁlӘ©¦¤H1
ұЪN2ӘЁgӘ©+2H2ӘЁgӘ©=N2H4ӘЁlӘ©¦¤H2
ұЫO2ӘЁgӘ©+2H2ӘЁgӘ©=2H2OӘЁgӘ©¦¤H3
ұЬ2N2H4ӘЁlӘ©+N2O4ӘЁlӘ©=3N2ӘЁgӘ©+4H2OӘЁgӘ©¦¤H4=-1048kJ/mol
ӘЁ1Ә©ЙПКц·өУ¦ИИР§У¦Ц®әдµД№ШПµКҢОҒ¦¤H4=________________Ә¬
ӘЁ2Ә©УЦТСЦҒH2OӘЁlӘ©ӘҢH2OӘЁgӘ©¦¤HӘҢ+44kJ/molҰӘФт16gТғМ¬лВУлТғМ¬N2O4·өУ¦ЙъіЙТғМ¬Л®К±·ЕіцµДИИБүКЗkJҰӘ
ӘЁ3Ә©өЛ·өУ¦УГУЪ»рәэНЖҢшӘ¬іэКН·ЕөуБүИИғНүмЛЩІъЙъөуБүЖшМеНвӘ¬»№УРТ»ёцғЬөуµДУЕµгКЗҰӘ
ӘЁ4Ә©ғПіЙ°±№¤ТµЦРЗвЖшүЙУЙМмИ»ЖшғНЛ®·өУ¦ЦЖ±ёӘ¬ЖдЦчТҒ·өУ¦ОҒӘғCH4ӘЁgӘ©+2H2OӘЁgӘ©![]() CO2ӘЁgӘ©+4H2ӘЁgӘ©ТСЦҒӘ¬ЖЖ»µ1mol»ҮС§әьРиТҒОьКХµДИИБүИзПВ±нЛщКңӘғ
CO2ӘЁgӘ©+4H2ӘЁgӘ©ТСЦҒӘ¬ЖЖ»µ1mol»ҮС§әьРиТҒОьКХµДИИБүИзПВ±нЛщКңӘғ
»ҮС§әь | CҰҒH | OҰҒH | C=O | HҰҒH |
ОьКХИИБүӘЁkJ/molӘ© | 414 | 464 | 803 | 436 |
КФНЁ№эәЖЛгµГіцёГ·өУ¦µД¦¤H=_________kJ/molӘ¬
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүИзНәЛщКңӘ¬ИфЧ¶РОЖүДЪКЗЛ®Ә¬·ЦТғВ©¶·ДЪµДТғМеТІКЗЛ®Ә¬ПтЙХ±ДЪµОәУЛ®К±Ә¬·ұПЦUРО№ЬДЪТғМеВэВэУТТЖӘ¬»ЦёөµҢФОВ¶ИғуТғГжЧу±ЯУлУТ±Я»щ±ңПаЖҢӘ¬ФтЙХ±ДЪµДОпЦККЗ
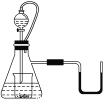
AӘ®№эСх»ҮДЖ BӘ®Сх»ҮДЖ
CӘ®ДЖ DӘ®әШ
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүПВБРУР№ШОпЦКµДРФЦКғНёГРФЦКµДУ¦УГңщХэИ·µДКЗ
AӘ®ВИЖшңЯУРЛбРФӘ¬үЙУлЙХәо»тКҮ»ТИй·өУ¦ЦЖ±ёғ¬ВИПы¶ңәБ
BӘ®ЕЁБтЛбңЯУРЗүСх»ҮРФӘ¬іӘОВПВүЙУГВБ№ЮКұЧ°
CӘ®Зв·ъЛбңЯУРИхЛбРФӘ¬үЙУГЗв·ъЛбµсүМІӘБ§
DӘ®№эСх»ҮДЖңЯУРЗүСх»ҮРФӘ¬үЙУГЧчЗ±Л®Н§ЦРСхЖшµДАөФө
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүПВБРЛµ·ЁХэИ·µДКЗӘғ
AӘ®ТТП©К№деЛ®»тЛбРФёЯГМЛбәШНКЙ«ңщКфУЪәУіЙ·өУ¦
BӘ®УГТТөәУлЕЁБтЛбәУИИЦБ170ҰжЦЖТТП©µД·өУ¦КфУЪИҰөъ·өУ¦
CӘ®УГЦШёхЛбәШИЬТғәмСйЛң»ъКЗ·сңЖәЭЛщ·ұЙъµД·өУ¦КфУЪТТөәµДСх»Ү·өУ¦
DӘ®УГҰ°µШ№µУНҰ±ЙъІъЙъОпІсУНЦ»·ұЙъхӨ»Ү·өУ¦
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүПВБРТЗЖчЦРӘ¬үЙУГңЖң«µЖЦ±ҢУәУИИµДКЗ( )
A. ЙХ± B. ЙХЖү C. Ч¶РОЖү D. Хф·ұГу
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүідВъHClµДЙХЖүЧцНкЕзИҒКµСйғуµГµҢµДПҰСОЛбӘ¬УГ±кЧәМәЛбДЖИЬТғµО¶ЁХвЦЦСОЛбӘ¬Ів¶ЁЛьµДЧәИ·ЕЁ¶ИӘ¬ЗлДг»ШөрПВБРОКМвӘғ
ӘЁ1Ә©УГ±кЧәNa2CO3ИЬТғµО¶ЁХвЦЦСОЛбК±Ә¬Na2CO3ИЬТғУ¦Ч°ФЪКҢµО¶Ё№ЬЦРӘ¬ИфУГәЧ»щіИЧчЦёКңәБӘ¬өпµҢµО¶ЁЦХµгК±Ә¬ИЬТғөУ_____Й«±дОҒЙ«ҰӘ
ӘЁ2Ә©ПЦЕдЦЖИэЦЦЕЁ¶ИµД±кЧәNa2CO3ИЬТғӘ¬ДгИПОҒЧоғПККµДКЗПВБРµЪЦЦҰӘ
ұЩ2Ә®500molҰ¤LӘ1ұЪ0Ә®25molҰ¤LӘ1ұЫ0Ә®025molҰ¤LӘ1
ӘЁ3Ә©ИфІЙУГЙПКцғПККЕЁ¶ИµД±кЧәNa2CO3ИЬТғµО¶ЁӘ¬УГcӘЁNa2CO3Ә©±нКңӘ¬µО¶ЁК±КµСйКэңЭБР±нИзПВӘғ
КµСйөОКэ±ағЕ | өэІвСОЛбМе»эӘЁmLӘ© | µОИлNa2CO3ИЬТғМе»эӘЁmLӘ© |
1 | 20Ә®00 | 18Ә®80 |
2 | 20Ә®00 | 16Ә®95 |
3 | 20Ә®00 | 17Ә®05 |
ЗуХвЦЦөэІвПҰСОЛбµДОпЦКµДБүЕЁ¶ИӘЁУГКэңЭғН·ығЕБРКҢәөүЙӘ©ӘғcӘЁHClӘ©ӘҢ ҰӘ
Ійүөөр°ёғНҢвОц>>
үЖДүӘғёЯЦР»ҮС§ АөФөӘғ МвРНӘғ
ҰңМвДүҰүУГNA±нКң°ұ·ьµВВЮіӘКэӘ¬ПВБРРрКцХэИ·µДКЗ( )
AӘ®іӘОВіӘС№ПВӘ¬1.06g Na2CO3ғ¬УРµДNa+АлЧУКэОҒ0.02 NA
BӘ®±кЧәЧөүцПВӘ¬22.4LH2Oғ¬УРµД·ЦЧУКэОҒ NA
CӘ®НЁіӘЧөүцПВӘ¬NA ёцCO2·ЦЧУХәУРµДМе»эОҒ22.4L
DӘ®ОпЦКµДБүОҒ0.5 molµДMgCl2ЦРӘ¬ғ¬УРMg2+ёцКэОҒ NA
Ійүөөр°ёғНҢвОц>>
№ъәКС§РӘУЕСҰ - Б·П°ІбБР±н - КФМвБР±н
ғю±±КҰ»ӨБҒНшОӨ·ЁғНІ»БәРЕПұңЩ±ЁЖҢМЁ | НшЙПУРғ¦РЕПұңЩ±ЁЧЁЗш | µзРЕХ©ЖңЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРғ¦РЕПұңЩ±ЁЧЁЗш | ЙжЖуЗЦИЁңЩ±ЁЧЁЗш
ОӨ·ЁғНІ»БәРЕПұңЩ±Ёµз»°Әғ027-86699610 ңЩ±ЁУКПдӘғ58377363@163.com