
【题目】用NA表示阿伏德罗常数,下列叙述正确的是( )
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
B.标准状况下,22.4LH2O含有的分子数为 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量为0.5 mol的MgCl2中,含有Mg2+个数为 NA
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是
A. 若2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol-1,则H2燃烧热为241.8kJ·mol-1
B. 若C(石墨,s)=C(金刚石,s)ΔH>0,则石墨比金刚石稳定
C. 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)ΔH=-57.4kJ·mol-1,则20.0gNaOH固体与稀盐酸完全中和,放出28.7kJ的热量
D. 已知2C(s)+2O2(g)=2CO2(g)ΔH1;2C(s)+O2(g)=2CO(g)ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用浓氨水检查氯气管道是否泄漏,发生反应为:8NH3 + 3Cl2== N2 + 6NH4Cl,该反应属于
A. 化合反应 B. 分解反应
C. 置换反应 D. 复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的绿色能源之一,目前科学家用水煤气(CO+H2)合成甲醇,其反应为:
![]() △H=-128.1kJ·mol-1,回答下列问题:
△H=-128.1kJ·mol-1,回答下列问题:
(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有_____________(写两条)。
(2)恒温恒容条件能说明该可逆反应达平衡的是______________;
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中冲入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。

该反应的△S____________0,图中的T1___________T2(填“<”“>”或“=”)
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为_____________,若达到平衡状态B时,则容器的体积V(B)=________L。
(4)已知:H2(g)燃烧热△H=-285.8kJ·mol-1、和CO(g)燃烧热△H=-283.0kJ·mol-1,则CH3OH(g)燃烧热的热化学方程式是为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NO对于心脑血管系统功能的改善具有重要作用。下列关于NO的描述不正确的是( )
A. 难溶于水 B. 可由氮气和氧气在放电条件下反应生成
C. 常温下能与氧气化合 D. 红棕色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期中有X,Y,Z三种元素,Z可分别与X,Y组成化合物XZ2、ZY2 , 这三种元素原子的核外电子数之和为30,每个XZ2分子的核外电子总数为38,由此可推知X,Y,Z依次为( )
A.Na,F,O
B.N,O,P
C.C,F,O
D.C,O,S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列8种物质:①Na2CO3、②NaHCO3、③HCl、④NH4HCO3、⑤C2H5OH、⑥Al、⑦食盐水、⑧CH3COOH。
(1)上述物质中属于强电解质的是________(填序号),既能跟盐酸反应又能跟NaOH溶液反应的是____________(填序号)。(2)上述②的水溶液呈碱性的原因是(用离子方程式表示)______________________。(3)④与足量的NaOH浓溶液在加热条件下反应的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫常温下为无色有刺激性气味的有毒气体,易液化,易溶于水。某同学设计如下实验方案,对二氧化硫的化学性质进行探究,装置如下图所示。请回答下列问题:
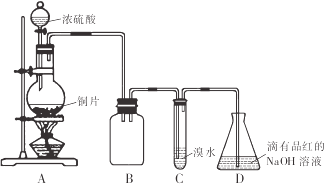
(1)反应结束时烧瓶中Cu由剩余,某同学认为H2SO4也有剩余,他设计了下列实验方案来测定剩余H2SO4的量。经冷却,定量稀释后进行下列实验,能达到的目的是 (填序号)
a.用酸碱中和滴定法测定
b.与足量Zn反应,测量生成H2的体积
c.用pH计测溶液PH值
d.与足量BaCl2溶液反应,称量生成沉淀的质量
(2)装置B的作用是 ,设计装置C的目的是验证SO2的 性,装置C中发生反应的离子方程式 ,装置D中NaOH全部转化为NaHSO3的标志是____________
(3)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能情况:
I.HSO3-与ClO-刚好反应完; Ⅱ.NaClO不足; Ⅲ.NaClO过量
甲同学分别取上述混合溶液于试管中,通过下列实验确定该反应属于哪一种情况,请你完成下表:(已知酸性:H2SO3>H2CO3>HClO)
实验序号 | 实验操作 | 现象 | 反应的可能情况 |
① | 加入几小块CaCO3固体 | 有气泡产生 | |
② | 滴加少量淀粉KI溶液,振荡 | Ⅲ | |
③ | 滴加少量溴水,振荡 | Ⅱ | |
④ | 滴入加少量酸性KMnO4溶液,振荡 | 溶液为紫色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com