
����Ŀ��Ϊȷ�������Ϸ����Ƶõ������������п��ܺ��е����ʣ�ͬѧ���ֽ���������ʵ��̽����
[��������]
����һ�������Լ�����ʱ�ֽܷ���������������ˮ(��Ӧ�и���Ԫ�صĻ��ϼ۲���)��
���϶�����������һ����̼��Ӧ�����¶����߶����еģ���������������������������������(��ɫ)�������������
[�������]
�����������п��ܺ��е������������������������е�һ�ֻ����֡�
[ʵ�����]
ͬѧ�dz�ȡ��23.28 g��������������Ʒ����������ʵ�飺
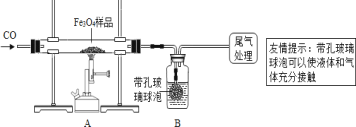
[ʵ�����]
��̽��˼·��ͬ����ȤС��ֳɼס�����С�顣
���飺
(1)����ͬѧ��ͨ��Bװ�÷�Ӧǰ��������仯������ȷ�ϸ�������������Ʒ�е����ʣ�B�е�����Լ���___(�����)��
�ٳ���ʯ��ˮ������������Ũ��Һ����ϡ���ᡡ����ˮ
(2)����ʵ������У�һ����̼�������Ϊ��Ӧ���⣬�����������ǣ���ʵ�鿪ʼʱ���ž�װ���еĿ�������ֹ����ʱ������ը����ֹͣ���Ⱥ�ֹA�������ﱻ������B�е���Һ������A�У���____��
(3)����ͬѧ��ΪBװ�÷�Ӧǰ����������ƫС��Ӱ����㡢����������Ϊ���ǵ�������____��
���飺���������ⶨ�����Ƴɷ�Ӧ������Aװ���в������ڵĹ����������¶ȵı仯����(��ͼ)��
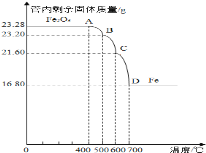
(1)д��BC�η�����Ӧ�Ļ�ѧ����ʽ____________��
(2)ͨ������ȷ������������������Ʒ�к��е�������_____�����к�������������������__g��(����Ҫд����)
���𰸡��� ��װ���еĶ�����̼ͨ������������Һ�� һ����̼��B����Һ���ݳ�ʱ���������ˮ���� Fe3O4��CO![]() 3FeO��CO2 ������ 20.88 g
3FeO��CO2 ������ 20.88 g
��������
����ʵ��Ŀ�ļ�װ��ͼ����װ����Ӧ��ѡ�õ��Լ�������CO�����ʼ�������ʵ������е����÷�����𣻸��������Ϣ�����п��ܲ�����ͼ�����ݷ���������Ӧ������ͼʾ���ݼ�����ɵ������������������Ʒ�������ʼ�������
���飺��1���������Ƶ��ܽ��Ժ�С�����ܱ�֤�����ɵĶ�����̼ȫ�����գ�������̼�ܽ�ˮ������Ҳ�����ܱ�֤�����ɵĶ�����̼ȫ�����գ�ϡ����Ͷ�����̼����Ӧ��ֻ������������Һ��֤�����ɵĶ�����̼ȫ�����գ���ѡ����������Ũ��Һ���ʴ�Ϊ���ڣ�
��2������ʵ������У�һ����̼�������Ϊ��Ӧ���⣬�����������ǣ�
��ʵ�鿪ʼʱ���ž�װ���еĿ�������ֹ����ʱ������ը��
��ֹͣ���Ⱥ�ֹA�������ﱻ������B�е���Һ������A�У�
�۽�װ���еĶ�����̼ͨ������������Һ�У�
�ʴ�Ϊ����װ���еĶ�����̼ͨ������������Һ�У�
��3��һ����̼��B����Һ���ݳ�ʱ���������ˮ������ʹB���ص�����ƫС���Ӷ�Ӱ�������Ʒ�����ʵ��������ʴ�Ϊһ����̼��B����Һ���ݳ�ʱ���������ˮ������
���飺��1���������϶�����������һ����̼��Ӧ�����¶����߶����еģ���������������������������������(��ɫ)���������������֪��AB��������������������BC����������������CD��������������BC�η�����Ӧ�Ļ�ѧ����ʽ��Fe3O4��CO![]() 3FeO��CO2��
3FeO��CO2��
��2����700 ��ʱֻʣ����������ʱ��������һ����̼��ԭΪ�����ʣ����������Ԫ�ص�����������![]() =72.16%��������������Ԫ�ص�����������
=72.16%��������������Ԫ�ص�����������![]() ��72.4%������������Ԫ�ص�����������
��72.4%������������Ԫ�ص�����������![]() ��77.8%����������Ԫ�ص�����������
��77.8%����������Ԫ�ص�����������![]() =70%�����Ը�������������Ʒ�к��е����������������������к�����������������Ϊx����
=70%�����Ը�������������Ʒ�к��е����������������������к�����������������Ϊx����![]() ��x��20.88g���ʴ�Ϊ����������20.88 g��
��x��20.88g���ʴ�Ϊ����������20.88 g��


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ȼ�����ӡˢ��ҽҩ�����ϡ���ˮ�����Լ��л��ϳɴ�����������Ҫ��Ӧ�á���ҵ�ϳ��Է���м������SiO2��Al2O3��MgO��Fe2O3�����ʣ�Ϊԭ���Ʊ��Ȼ�����������������ͼ��
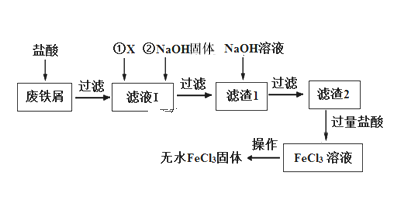
��֪�����������Ksp���±���
�������� | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
Ksp | 1.0��10-36 | 1.6��10-14 | 2.0��10-33 | 1.2��10-11 |
��ش��������⣺
��1������X����ѡ�����������е�____��ѡ����ţ�
A��NaCl B��FeCl3 C��H2O2 D��H2SO4
��2����Һ�����NaOH�����Ŀ���ǵ�����Һ��pH�����Լ���NaOH�����Ժ���Һ����ı仯������֪��Һ����c(Fe3+)Ϊ1.0 mol��L-1��c(Al3+)Ϊ0.03 mol��L-1��c(Mg2+)Ϊ0.01 mol��L-1����Fe3+ǡ�ó�����ȫʱ[c(Fe3+)=1��10-5 mol��L-1]��Al3+�Ƿ��Ѿ���ʼ����______����������������������
��3��д������1��NaOH��Һ������Ӧ�����ӷ���ʽ_____________________��
��4�������������������FeCl3��Һ�õ���ˮFeCl3�������IJ�����Ϊ��������һ��������ȴ�ᾧ�õ�FeCl3��6H2O���壻�ڶ���������ˮFeCl3���塣�ڶ�������ȷ������_____��
��5��FeCl3���о�ˮ���ã�����ʴ�豸�����ۺ��Ȼ�����һ�����͵���������������ˮ��FeCl3��Ч���Ҹ�ʴ��С��
��FeCl3��ˮ��ԭ����____________________�������ӷ���ʽ��ʾ��
��ͨ�������������ɾۺ��Ȼ��������ӷ���ʽΪxFe3����yH2O![]() Fex(OH)y(3x-y)+��yH���������Ӿۺ��Ȼ����IJ��ʿɲ�ȡ�ķ�����_____������ĸ����
Fex(OH)y(3x-y)+��yH���������Ӿۺ��Ȼ����IJ��ʿɲ�ȡ�ķ�����_____������ĸ����
a�����¡� b���Ӱ�ˮ c������NH4Cl d������NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������������MnO2�ͺ���4 mol���ʵ�Ũ�����ַ�Ӧ������������˵����ȷ����(����)
A. ��ʵ���й�����1 mol MnO2������1 mol����
B. Ϊ�˳�ȥ�����л��е��������壬��������ͨ������ʳ��ˮ�ͼ�ʯ��
C. �ڸ÷�Ӧ��MnO2����������Ũ��������ԭ��
D. ���������������ſ���������ˮ���ռ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£�aA��bB![]() cC�Ŀ��淴Ӧ�ﵽƽ�⣺
cC�Ŀ��淴Ӧ�ﵽƽ�⣺
��1����֪A��B��C�������壬�ڼ�ѹ��ƽ�����淴Ӧ�����ƶ�����a��b��c�Ĺ�ϵ�ǣ�_____��
��2����֪AΪ���塢BΪ��ɫ���塢C����ɫ���壬�ң�a��b��=c���ڼ�ѹʱ��ƽ����____�����ƶ����������ɫ��___��������dz�����䡱����
��3�����Ⱥ�C�������������٣�������Ӧ��___�ȷ�Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ϊ1 L��pH������2������ʹ����У��ֱ�Ͷ��0.12 gþ�۳�ַ�Ӧ����ͼ�бȽϷ��Ϸ�Ӧ��ʵ��������
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڴ��Թ��ڽ�����NaHCO3���ȵ� 200�����������Ļ������ͨ�뵽ʢ��1.87 g Na2O��Na2O2���ܱ������У���Na2O��Na2O2ȫ����Ӧ�õ���״����224 mL O2���ٽ���Ӧ���ܱ������ڵĹ���ȫ������ˮ��� 100 mL ��Һ������˵����ȷ����
A.Na2O��Na2O2 ������������
B.�μӷ�Ӧ��NaHCO3���ʵ���Ϊ 0.04 mol
C.��Ӧ�������ܹ�ת�� 0.04 mol ����
D.��ɵ� 100 mL ��Һ�� c(Na+) = 0.5 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3���о�ˮ���ã�����ʴ�豸�����ۺ��Ȼ�����һ�����͵���������������ˮ��FeCl3��Ч���Ҹ�ʴ��С����ش��������⣺
(1)FeCl3��ˮ��ԭ����______��FeCl3��Һ��ʴ�����豸����H�������⣬��һ��Ҫԭ����(�����ӷ���ʽ��ʾ)______��
(2)Ϊ��Լ�ɱ�����ҵ����NaClO3��������FeCl2��Һ�õ�FeCl3��
��������FeCl2��Һ��c(Fe2��)=2.0��10-2mol��L-1��c(Fe3��)=1.0��10-3mol��L-1��c(Cl��)=5.3��10-2mol��L-1�������Һ��pHԼΪ______��
�����NaClO3����FeCl2�����ӷ���ʽ��
___![]() +___Fe2++___=___Cl+___Fe3++__
+___Fe2++___=___Cl+___Fe3++__
(3)FeCl3����Һ�з�����ˮ�⣺
Fe3��+H2O![]() Fe(OH)2++H�� K1
Fe(OH)2++H�� K1
Fe(OH)2++H2O![]()
![]() +H�� K2
+H�� K2
![]() +H2O
+H2O![]() Fe(OH)3+H�� K3
Fe(OH)3+H�� K3
����ˮ�ⷴӦ��ƽ�ⳣ��K1��K2��K3�ɴ�С��˳����__________��
ͨ����������������ˮ�����ۺϣ����ɾۺ������������ӷ���ʽΪ��xFe3++yH2O![]() Fex(OH)y(3x-y)++yH+����ʹƽ�������ƶ��ɲ��õķ�����(�����)______��
Fex(OH)y(3x-y)++yH+����ʹƽ�������ƶ��ɲ��õķ�����(�����)______��
a������ b����ˮϡ��
c������NH4Cl d������NaHCO3
�����£�ʹ�Ȼ�����Һת��Ϊ��Ũ�Ⱦۺ��Ȼ����Ĺؼ�������___��
(4)���ij��ˮ���������Ȼ���������ˮ�Ľ������ͼ��ʾ����ͼ�����ݵó�ÿ����ˮ��Ͷ�žۺ��Ȼ���[��Fe(mg��L-1)��ʾ]����ѷ�ΧԼΪ_____mg��L-1��
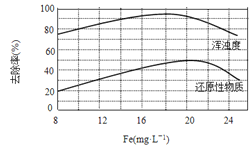
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��RԪ����ͬλ�ء�21gR2+���������ں���22��3.01��1023�����ӣ�ȡ�������ĸ�Ԫ�ص������ᷴӦ���ڱ�״��������11.2LH2��
(1)21g R2+�����������к���_________mol���ӣ�_________________mol���ӣ�
(2)R��__________Ԫ�أ�д����Ԫ��ԭ�Ӻ˵����_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2L�ĺ����ܱ������з�����ӦA(g)��2B(g)![]() 3C(g)����Ӧ�����еIJ����������±���ʾ��
3C(g)����Ӧ�����еIJ����������±���ʾ��
n/mol t/min | n(A) | n(B) | n(C) |
0 | 2.0 | 2.4 | 0 |
5 | 0.9 | ||
10 | 1.6 | ||
15 | 1.6 |
����˵����ȷ���ǣ� ��
A.0��5min��A��ʾ��ƽ����Ӧ����Ϊ0.09mol��L-1��min-1
B.�÷�Ӧ��10min��Ŵﵽƽ��
C.����B��ƽ��ת����Ϊ20%
D.ƽ��״̬ʱ��c(C)=0.6mol��L-1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com