
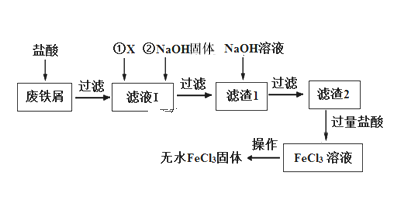
【题目】三氯化铁在印刷、医药、颜料、污水处理以及有机合成催化剂方面有重要的应用。工业上常以废铁屑(含有SiO2、Al2O3、MgO、Fe2O3等杂质)为原料制备氯化铁。其生产流程如图:
已知:氢氧化物的Ksp如下表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
Ksp | 1.0×10-36 | 1.6×10-14 | 2.0×10-33 | 1.2×10-11 |
请回答下列问题:
(1)物质X可以选用下列物质中的____(选填序号)
A.NaCl B.FeCl3 C.H2O2 D.H2SO4
(2)滤液Ⅰ加入NaOH固体的目的是调节溶液的pH(忽略加入NaOH固体以后溶液体积的变化)。已知滤液Ⅰ中c(Fe3+)为1.0 mol·L-1,c(Al3+)为0.03 mol·L-1,c(Mg2+)为0.01 mol·L-1,当Fe3+恰好沉淀完全时[c(Fe3+)=1×10-5 mol·L-1],Al3+是否已经开始沉淀______(填“是”或“否”)。
(3)写出滤渣1加NaOH溶液发生反应的离子方程式_____________________。
(4)生产流程中最后“从FeCl3溶液得到无水FeCl3固体”的操作分为两步:第一步,先冷却结晶得到FeCl3·6H2O晶体;第二步,制无水FeCl3固体。第二步的正确操作是_____。
(5)FeCl3具有净水作用,但易腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3高效,且腐蚀性小。
①FeCl3净水的原理是____________________(用离子方程式表示)
②通过控制条件生成聚合氯化铁,离子方程式为xFe3++yH2O![]() Fex(OH)y(3x-y)++yH+,欲增加聚合氯化铁的产率可采取的方法是_____(填字母)。
Fex(OH)y(3x-y)++yH+,欲增加聚合氯化铁的产率可采取的方法是_____(填字母)。
a.降温 b.加氨水 c.加入NH4Cl d.加入NaHCO3
【答案】C 是 Al(OH)3 + OH- = AlO2- + 2H2O 在HCl气流中加热 Fe3++3H2O![]() 3Fe(OH)3+3H+ b、d
3Fe(OH)3+3H+ b、d
【解析】
废铁屑中加入盐酸,过滤除去不溶性杂质二氧化硅,滤液1加入过氧化氢溶液将亚铁离子氧化为铁离子,然后加入氢氧化钠固体并控制pH,使铁离子、铝离子转化为沉淀,过滤之后得滤渣1(含有氢氧化铁和氢氧化铝),加入氢氧化钠溶液除去氢氧化铝,过滤得滤渣2即为氢氧化铁,加入过量的盐酸将其转化为氯化铁,在氯化氢的氛围下加热即可得到无水氯化铁固体。
(1)加入H2O2溶液,使滤液Ⅰ中的Fe2+转化为Fe3+,便于制备FeCl3;
(2)当Fe3+恰好沉淀完全时,c(Fe3+)=1×10-5 mol·L-1,根据Ksp(Fe(OH)3)=1.0×10-36 可知此时c(OH-)3=![]() mol3·L-3,又c(Al3+)为0.03 mol·L-1,所以此时有:c(Al3+)·c(OH-)3=0.03×1.0×10-31=3×10-33>Ksp (Al(OH)3)=2.0×10-33,所以当Fe3+恰好沉淀完全时,Al3+已经开始沉淀;
mol3·L-3,又c(Al3+)为0.03 mol·L-1,所以此时有:c(Al3+)·c(OH-)3=0.03×1.0×10-31=3×10-33>Ksp (Al(OH)3)=2.0×10-33,所以当Fe3+恰好沉淀完全时,Al3+已经开始沉淀;
(3)滤渣1加NaOH溶液发生反应的离子方程式:Al(OH)3 + OH- = AlO2- + 2H2O;
(4)由FeCl3·6H2O晶体制无水FeCl3固体时,在加热脱水时为防止铁离子水解,所以正确操作是:在HCl气流中加热;
(5)①FeCl3净水的原理是:Fe3++3H2O![]() 3Fe(OH)3+3H+,生成的Fe(OH)3胶体吸附杂质;
3Fe(OH)3+3H+,生成的Fe(OH)3胶体吸附杂质;
②水解是吸热反应,降温会降低聚合氯化铁的产率;加氨水,消耗生成的H+,促使反应向右进行,会增大聚合氯化铁的产率;加入NH4Cl后,NH4+水解会生成H+(NH4+ +H2O![]() NH3·H2O+H+),所以会抑制Fe3+的水解,平衡向左移动,降低聚合氯化铁的产率;加入NaHCO3,HCO3-与溶液中生成的H+反应生成CO2和H2O, 平衡向右移动,会增大聚合氯化铁的产率。
NH3·H2O+H+),所以会抑制Fe3+的水解,平衡向左移动,降低聚合氯化铁的产率;加入NaHCO3,HCO3-与溶液中生成的H+反应生成CO2和H2O, 平衡向右移动,会增大聚合氯化铁的产率。


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。
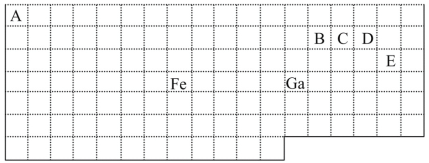
根据信息回答下列问题:
(1)周期表中基态Ga原子的电子排布式为___。
(2)Fe元素位于周期表的___分区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为___。
(3)已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为___和___(填化学式)。在CO、CH3OH中,碳原子采取sp3杂化的分子有___。
(4)根据VSEPR理论预测ED4-离子的空间构型为___。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子有__(任写2种化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关溶液的说法正确的是( )
A. pH相等的①NH4Cl、②NH4Al(SO4)2、③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×1010,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F) >c(K+ ) c(CH3COO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理利用资源成为当今研究热点。CH3NH2、PbI2及HI常用作合成太阳能电池的敏化剂甲胺铅碘(CH3NH3PbI3)的主要原料。
(1)制取甲胺的反应为CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
CH3NH2(g)+H2O(g) ΔH。已知该反应中相关化学键的键能数据如下:
共价键 | C-O | H-O | N-H | C-N |
键能/kJ·mol-1 | E1 | E2 | E3 | E4 |
则上述热化学方程式中ΔH=___kJ·mol-1。
(2)可利用水煤气合成上述反应所需甲醇。反应为CO(g)+2H2(g)![]() CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:
CH3OH(g)ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为___。
②图中Y轴表示温度,其判断的理由是__。
(3)可利用四氧化三铅和氢碘酸反应制备难溶PbI2,若反应中生成amolPbI2,则转移电子的物质的量为___。
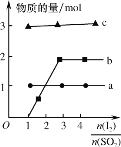
(4)将二氧化硫通入碘水制备HI的反应曲线如图所示,其反应原理为:SO2+I2+2H2O=3H++HSO4-+2I-,I2+I-![]() I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。
I3-,图中曲线a、b分别代表的微粒是__和__(填微粒符号);由图知要提高碘的还原率,除控制温度外,还可以采取的措施是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双功能手性催化剂在药物合成中起到重要的作用。其中一种催化剂I的合成路线如下:
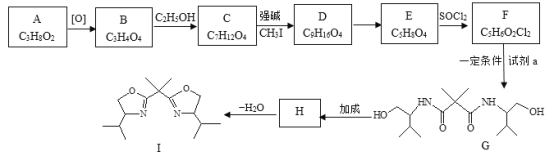
已知:R-NH2+![]()
![]()
![]()
(1)A可与Na反应可生成H2,则A中的官能团名称是_________。
(2)下列关于A的说法中,正确的是_________。
a.与乙醇互为同系物
b.与B在一定条件下可发生缩聚反应
c.发生消去反应的试剂和条件是:NaOH的醇溶液、加热
(3)写出B→C的化学方程式:___________。
(4)D的结构简式是__________。
(5)E→F的反应类型是___________。
(6)已知:NH3+![]() →H2N-CH2CH2OH,NH3和物质K发生反应可以制备试剂a,K的结构简式是__________。
→H2N-CH2CH2OH,NH3和物质K发生反应可以制备试剂a,K的结构简式是__________。
(7)F与对苯二胺(![]() )在一定条件下可发生缩聚反应制备尼龙MXD6的衍生品,该反应的化学方程式是___________。
)在一定条件下可发生缩聚反应制备尼龙MXD6的衍生品,该反应的化学方程式是___________。
(8)H的结构简式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,体积为2L的密闭容器中,2mol X和3mol Y进行反应:X(g)+Y(g)![]() Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是
Z(g),经12s达到平衡,生成0.6molZ。下列说法正确的是
A. 以X浓度变化表示的反应速率为0.05 mol/(Ls)
B. 其他条件不变,增大X的浓度,平衡右移,X的转化率增大
C. 其他条件不变,12s后将容器体积扩大为10L,Z的平衡浓度变为0.06mol/L
D. 其他条件不变,若移走1molX和1.5molY,再达平衡时Z的物质的量小于0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型NaBH4/H2O2燃料电池DBFC的结构如图所示,该电池总反应方程式:NaBH4 +4H2O2= NaBO2+ 6H2O,有关的说法不正确的是

A. 电极B为正极
B. 放电过程中,Na+从正极区向负极区迁移
C. 电池负极的电极反应为:BH4-+8OH8e=BO2-+6H2O
D. 在电池反应中,每消耗1L6mol/LH2O2溶液,理论上流过电路中的电子为12NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R、X、Y、Z的原子序数依次增大,且都不超过10.这四种元素可组成一种化合物的结构如图所示。下列说法正确的是( )
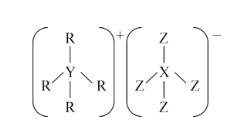
A.常温常压下,上述元素的单质都呈气态
B.最高价氧化物对应水化物的酸性:X>Y
C.Y、Z的气态氢化物能发生化合反应
D.由R、X两种元素只能形成一种化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定用以上方法制得的四氧化三铁中可能含有的杂质,同学们又进行了下列实验探究。
[查阅资料]
资料一:难溶性碱受热时能分解产生金属氧化物和水(反应中各种元素的化合价不变);
资料二:氧化铁和一氧化碳反应是随温度升高而逐步进行的,先生成四氧化三铁,再生成氧化亚铁(黑色),最后生成铁。
[提出猜想]
四氧化三铁中可能含有的杂质是氧化铁和氧化亚铁中的一种或两种。
[实验设计]
同学们称取了23.28 g该四氧化三铁样品进行了下列实验:
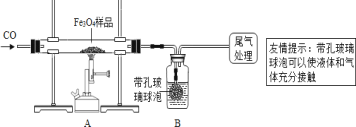
[实验分析]
因探究思路不同,兴趣小组分成甲、乙两小组。
甲组:
(1)该组同学欲通过B装置反应前后的质量变化来计算确认该四氧化三铁样品中的杂质,B中的最佳试剂是___(填序号)。
①澄清石灰水 ②氢氧化钠浓溶液 ③稀盐酸 ④水
(2)上述实验过程中,一氧化碳气体除作为反应物外,还能起到的作用是:①实验开始时,排尽装置中的空气,防止加热时发生爆炸;②停止加热后,防止A中生成物被氧化,B中的溶液倒吸入A中;③____。
(3)乙组同学认为B装置反应前后的质量差会偏小而影响计算、分析,你认为他们的理由是____。
乙组:利用仪器测定并绘制成反应过程中A装置中玻璃管内的固体质量随温度的变化曲线(如图):
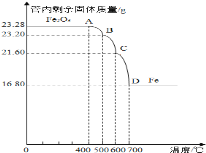
(1)写出BC段发生反应的化学方程式____________。
(2)通过计算确定:该四氧化三铁样品中含有的杂质是_____,其中含四氧化三铁的质量是__g。(不需要写过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com