
下列有关说法正确的是( )
A.反应NH3(g)+HCl(g)=NH4Cl(s)在室温下可自发进行,则该反应的△H<0
B.电解法精炼铜时,以粗铜作阴极,纯铜作阳极
C.CH3COOH 溶液加水稀释后,溶液中 的值增大
的值增大
D. 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届湖北省高三上学期起点考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )。
A.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O
B.将少量SO2通入苯酚钠溶液中:2C6H5O-+SO2+H2O=2C6H5OH+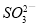
C.用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-=Fe(SCN)3↓
D.向碘化亚铁溶液中通入过量的氯气:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高二下学期期中联考化学试卷(解析版) 题型:填空题
(1)为实现以下各步的转化,请在括号中填入适当的试剂
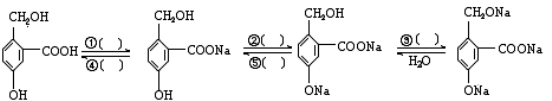
① ② ③ ④ ⑤
(2)分子式为C4H10O的有机化合物,能在催化剂作用下连续氧化生成羧酸,请写出它可能的结构简式为_____________ 、_____________ 。当C与4个不同的原子或基团相连时该碳原子称作“手性”碳原子。则分子式为C4H10O的有机化合物中,含有“手性”碳原子的结构简式为________________。该有机物的系统命名为:
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高二下学期期中联考化学试卷(解析版) 题型:选择题
有关化学用语正确的是 ( )
A.溴乙烷的分子式C2H5Br
B.乙醇的结构简式C2H6O
C.四氯化碳的电子式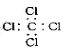
D.乙烯的结构简式CH2CH2
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期初联考化学试卷(解析版) 题型:填空题
(14分)A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、
D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶
液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图 ,E元素在周期表中的位置是 。
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为 。
(3)D与C按原子个数比为1:1形成化合物的电子式是 。
(4)B、C所形成氢化物的稳定性由强到弱的顺序是 (填具体的化学式)。
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与 C形成的化合物甲反应的离子方程式 。
(6)有人设想寻求合适的催化剂和电极材料,以A2、B2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极电极反应式: ;放电时溶液中H+移向 (填“正”或“负”)极。
(7) E(s)+O2(g) EO2(g) △H1 E(g)+O2(g) EO2(g) △H2,则△Hl △H2(填“>”或“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期初联考化学试卷(解析版) 题型:选择题
下列叙述I和II均正确并有因果关系的是( )
选项 | 叙述I | 叙述II |
A | KNO3的溶解度大 | 用重结晶法除去KNO3中混有的NaCl |
B | BaSO4难溶于酸 | 用盐酸和BaCl2溶液检验SO42- |
C | NH3能使酚酞溶液变红 | NH3可用于设计喷泉实验 |
D | Ca(OH)2能制成澄清石灰水 | 可配制2.0 mol?L-1的Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期初联考化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A.把100mL3mol/L的硫酸与100mLH2O混合,硫酸的物质的量浓度变为1.5mol/L
B.用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2
C.用CO2鉴别NaAlO2溶液和CH3COONa溶液
D.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小。
查看答案和解析>>
科目:高中化学 来源:2015届浙江省杭州地区六校高二下学期期中联考化学试卷(解析版) 题型:选择题
诺贝尔物理学奖曾授予“光纤之父”英国华裔科学家高锟以及两位美国科学家威拉德·博伊尔和乔治·史密斯。光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是
A.二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B.用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
C.二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
D.二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应
查看答案和解析>>
科目:高中化学 来源:2015届浙江省嘉兴市高二暑假作业检测(开学作业检测)化学试卷(解析版) 题型:计算题
将50.0g含有NH4NO3、(NH4)2SO4及其它难溶物的混合物样品,溶于水,过滤后加入足量浓NaOH溶液共热,在标准状况下收集到13.44 L氨气,再向溶液中加入足量BaCl2溶液,产生沉淀46.6g,试计算混合物中NH4NO3的物质的量及(NH4)2SO4的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com