
【题目】下列卤代烃在KOH醇溶液中加热不反应的是( )
① ![]() ② (CH3)2CHCH2Cl ③ (CH3)3CCH2Cl ④ CHCl2-CHBr2 ⑤
② (CH3)2CHCH2Cl ③ (CH3)3CCH2Cl ④ CHCl2-CHBr2 ⑤ ![]() ⑥ CH2Cl2
⑥ CH2Cl2
A.①③⑥ B.②③⑤ C.全部 D.②④
【答案】B
【解析】
试题分析:①、氯苯分子中含有稳定的大π键或苯环结构,假设氯苯与KOH醇溶液共热发生消去反应,必须断C-Cl键和相邻碳原子的C-H键,同时形成不饱和的C=C键或C≡C键,该方向违反了焓判据和熵判据,将破坏苯环的稳定性,因此不能发生消去反应,①正确;②、和氯相连的碳原子的相邻碳原子上有氢原子,因此该卤代烷烃能发生消去反应,生成对应的烯烃和氯化钾,②错误;③、和氯相连的碳原子的相邻碳原子上没有氢原子,因此该卤代烷烃不能发生消去反应,③正确;④、和氯或溴相连的碳原子相邻碳原子上有氢原子,因此该多卤代烷烃能发生消去反应,生成对应的烯烃或炔烃和氯化钾,④错误;⑤、和溴原子相连的碳原子上有氢原子,因此一溴环己烷能发生消去反应,生成环己烯和氯化钾,⑤错误;⑥、CH2Cl2不能发生消去反应,因二氯甲烷分子中只有一个碳原子,没有相邻的碳原子和氢原子,答案选D。


 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等。按要求回答下列问题:
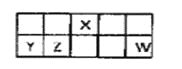
(1)写出W的离子结构示意图________________
(2)比较W 与Z的最高价氧化物对应水化物酸性的强弱 (写化学式)
(3)写出X的氢化物的电子式 ,写出X氢化物的水溶液与X的最高价氧化物对应的水化物的水溶液反应的离子方程式_____________________
(4)已知:①C(s)+ O2(g)= CO2(g) △H="a" kJ· mol-1;
②CO2(g) +C(s)="2CO(g)" △H="b" kJ· mol-1;
③Si(s)+ O2(g)=SiO2(s) △H="c" kJ· mol-1。写出工业生产中用碳粉还原二氧化硅制取粗硅的热化学方程式_________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质及变化分类或归类正确的是
①混合物:聚氯乙烯、焦炉气、水银 ②化合物:烧碱、蔗糖、CuFeS2
③电解质:明矾、冰醋酸、硫酸钡 ④同位素:HD、HT、DT
⑤化学变化:风化、钝化、煤的液化
A. ①③ B. ②③⑤ C. ②③④ D. ①②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个10 L的密闭容器发生反应A(g)+B(g) C(g)+D(g),测得平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | K | 0.6 | 0.4 |
回答下列问题:
(1)△H ____________ 0(填“<”或 “>”)。
(2)830℃时,向一个10 L的密闭容器中充入1mol的A和1mol的B,则:
①反应达平衡时,n (D)=0.5 mol,则A的平衡转化率为 ,
②该温度下平衡常数K= 。
(3)判断该反应是否达到平衡的依据为
a.c(A)不再改变 b.混合气体的密度不再改变
c.体系内压强不再改变 d.单位时间内生成C和消耗D的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分元素,用元素符号或化学式回答下列问题:

① 表中用字母标出的14种元素中,化学性质最不活泼的是________,主族元素中金属性最强的是_______,常温下单质为液态的非金属元素是_______;属于过渡元素的是_________。
②C、G、F气态氢化物的稳定性顺序是______________________ 。
③第三周期中原子半径最小的元素是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
A. 硝酸钠、氢氧化钠 B. 氧化铜、二氧化锰
C. 氯化钾、二氧化锰 D. 硫酸铜、氢氧化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(9分)某化学兴趣小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸试管壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,看到的现象是 ,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)

乙方案:将盛放有生石灰的小试管插入带支管的试管中,支管接①或②,用胶头滴管向小试管中缓缓滴入水,看到的现象是(接①) ,(接②) ,说明反应放热。
丙方案:用胶头滴管向盛放有生石灰且带支管的试管中滴加水,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是 ,说明反应放热,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。
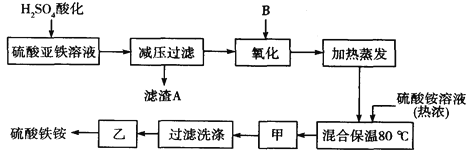
请回答下列问题:
(1)下列物质中最适合的氧化剂B是 ;
a.NaClO b.H2O2c.KMnO4d.K2Cr2O7
反应的离子方程式 。
(2)上述流程中,用足量最适合的氧化剂B氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,能否用酸性的KMnO4溶液?并说明理由 。(可用文字或方程式说明)
(3)检验硫酸铁铵中NH4+的方法是 。
(4)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba (NO3)2的溶液,恰好完全反应。则该硫酸铁铵的化学式为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com