
����Ŀ����һ��10 L���ܱ�����������ӦA(g)+B(g) C(g)+D(g)�����ƽ�ⳣ�����¶ȵĹ�ϵ���£�
�¶�/ �� | 700 | 800 | 830 | 1000 | 1200 |
ƽ�ⳣ�� | 1.7 | 1.1 | K | 0.6 | 0.4 |
�ش��������⣺
(1)��H ____________ 0(����<���� ��>��)��
(2)830��ʱ����һ��10 L���ܱ������г���1mol��A��1mol��B����
����Ӧ��ƽ��ʱ��n (D)��0.5 mol����A��ƽ��ת����Ϊ ��
�����¶���ƽ�ⳣ��K= ��
(3)�жϸ÷�Ӧ�Ƿ�ﵽƽ�������Ϊ
a��c(A)���ٸı� b�����������ܶȲ��ٸı�
c����ϵ��ѹǿ���ٸı� d����λʱ��������C������D�����ʵ������
(4)1200��ʱ��ӦC(g)+D(g) A(g)+B(g)��ƽ�ⳣ��Ϊ ��
���𰸡�
(1)<��(2)50%��1��(3)ad��(4)2.5��
��������
���������(1)���ݱ������ݣ������¶ȣ�ƽ�ⳣ��K��С��ƽ�������ƶ���˵����H �� 0���ʴ�Ϊ������
(2)����Ӧ��ƽ��ʱ��n (D)��0.5 mol����Ӧ��AΪ0.5mol����A��ƽ��ת����=![]() ��100%=50%���ʴ�Ϊ��50%��
��100%=50%���ʴ�Ϊ��50%��
����������֪��ƽ��ʱ�������ʵ����ʵ�����Ϊ0.5mol��Ũ�Ⱦ�Ϊ0.5mol/L�����¶���ƽ�ⳣ��K=![]() =1���ʴ�Ϊ��1��
=1���ʴ�Ϊ��1��
(3)a��c(A)���ٸı䣬˵���ﵽ��ƽ��״̬����ȷ��b��������������䣬������������䣬���������ܶ�ʼ�ղ��䣬�����ж��Ƿ���ƽ��״̬������c���÷�Ӧ������������ʵ�������ķ�Ӧ����ϵ��ѹǿʼ�ղ��䣬�����ж��Ƿ���ƽ��״̬������d����λʱ��������C������D�����ʵ�����ȣ�˵�����淴Ӧ������ȣ�˵���ﵽ��ƽ��״̬����ȷ����ѡad��
(4)1200��ʱ��ӦC(g)+D(g) A(g)+B(g)��ƽ�ⳣ����A(g)+B(g) C(g)+D(g)��Ϊ���������C(g)+D(g) A(g)+B(g)��ƽ�ⳣ��=![]() =2.5���ʴ�Ϊ��2.5��
=2.5���ʴ�Ϊ��2.5��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������뻯ѧ��Ӧ�����仯��ص�������ȷ����
A���������������һ�����ڷ�Ӧ���������
B���������еĻ�ѧ��һ����Ҫ��������
C��Ӧ�ø�˹���ɣ�������ijЩ����ֱ�Ӳ����ķ�Ӧ�ʱ�
D����ѧ��Ӧ��������������������������ij���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʳƷ��ѧ֪ʶ��������ȷ����
A. �����߲����������ά����C������ʧ
B. ��֬�����ۡ������ʾ�Ϊ��ˮ��ĸ߷��ӻ�����
C. ��ά���������ڿ�ˮ��Ϊ�����ǣ��ʿ��������Ӫ������
D. ĥ�����Ĵ��������ʣ�������к��ʱ���˰�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. �������ȿ���������ˮ������ B. ����þ�������������²���
C. �ѹ���ըҩ�Ƴɽ������������ D. ������������Ư��ֽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������б������������й��ɣ��ж������ڵ�15λ���ķ���ʽ��
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | �� |
C2H2 | C2H4 | C2H6 | C3H4 | C3H6 | C3H8 | C4H6 | C4H8 | C4H10 | �� |
A. C6H12 B. C6H14 C. C7H12 D. C7H14
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ҽ����ʾ��θ�������ˣ�Ӧ��ʳƻ������ôƻ��֭��pH �� ��
A.����7 B.����7 C.С��7 D.���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������±������KOH����Һ�м�������Ӧ������ ��
�� ![]() �� ��CH3��2CHCH2Cl �� ��CH3��3CCH2Cl �� CHCl2��CHBr2 ��
�� ��CH3��2CHCH2Cl �� ��CH3��3CCH2Cl �� CHCl2��CHBr2 �� ![]() �� CH2Cl2
�� CH2Cl2
A���٢ۢ� B���ڢۢ� C��ȫ�� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)����H ��0�Ļ�ѧ��Ӧ������������ȷ����
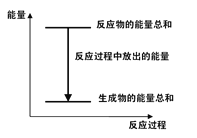
A����Ӧ������������ϵ������ͼ��ʾ
B�������÷�Ӧ��Ƴ�ԭ���пΪ����
C����H��ֵ�뷴Ӧ����ʽ�ļ���ϵ����
D�����������Ϊԭ��ص���32.5gп�ܽ�ʱ�������ų�����һ��Ϊ11.2L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1�ǵ�ⱥ���Ȼ�����Һʾ��ͼ��ͼ2�У�x���ʾʵ��ʱ���������ĵ��ӵ����ʵ�����y���ʾ
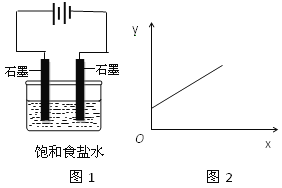
A��n(Na��) B��n(Cl��)
C��c(OH��) D��c(H��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com