
【题目】在容积为2.0L的恒容密闭容器中充入3.0molCl2和4.0molPCl5,473K 时发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1,各物质的物质的量随时间变化关系如图所示:
PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1,各物质的物质的量随时间变化关系如图所示:
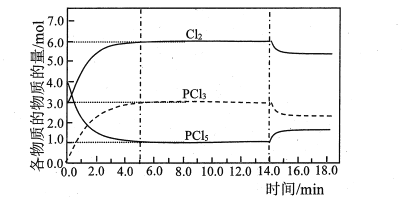
下列说法正确的是
A.0.0~5.0min,PCl5分解的平均速率为0.6mol·L-1·min -1
B.起始时,若用3.0mol37Cl2和4.0mol P35Cl5,达平衡时,PCl3 中不含37C1
C.图中14.0min时,改变的外界条件可能是缩小容器的体积
D.若在14.0min时,向容器中各充入1.0mol 的Cl2、PCl5 及PCl3,维持其他条件不变,重新达到平衡前,v(正)>v(逆)
【答案】CD
【解析】
A.根据![]() ,则0.0~5.0min,PCl5分解的平均速率
,则0.0~5.0min,PCl5分解的平均速率![]() ,A错误;
,A错误;
B.该反应为可逆反应,在达到平衡的过程中,反应既正向进行,又逆向进行,因此各个物质中均存在37Cl,B错误;
C.根据图示,14.0min时,Cl2和PCl3的物质的量在减小,而PCl5的物质的量在增加,说明平衡逆向移动,若压缩体积,压强增大,平衡向气体体积减小的方向移动,与图像相符,C正确;
D.达到平衡时,Cl2、PCl3、PCl5的物质的量分别为6mol、3mol、1mol,容器的体积为2L,则可求得平衡常数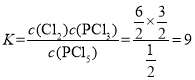 ,若向容器中各充入1.0mol的Cl2、PCl5及PCl3,此时Cl2、PCl3、PCl5的物质的量分别为7mol、4mol、2mol,浓度商
,若向容器中各充入1.0mol的Cl2、PCl5及PCl3,此时Cl2、PCl3、PCl5的物质的量分别为7mol、4mol、2mol,浓度商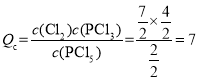 ,小于K,平衡正向移动,则v(正)>v(逆),D正确。
,小于K,平衡正向移动,则v(正)>v(逆),D正确。
答案选CD。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是
A. 标准状况下,2.24 L![]() 中含有碳碳双键数为0.3NA
中含有碳碳双键数为0.3NA
B. 0.1mol甲烷和乙烯组成的混合气体完全燃烧,生成的水分子数为0.2NA
C. 0.1molCH4与0.1molCl2混合充分光照,生成CH3Cl分子数为0.1 NA
D. 0.1molN2和0.3molH2在高温、高压及催化剂下充分反应,产物的分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一。在恒容密闭容器中,CO2和H2在催化剂作用下发生反应:CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g)。CO2、H2、CH3OH、H2O的浓度均不再改变时,下列说法正确的是
CH3OH(g) + H2O(g)。CO2、H2、CH3OH、H2O的浓度均不再改变时,下列说法正确的是
A. CO2、H2、CH3OH、H2O的浓度一定相等
B. 该反应已经达到化学平衡状态
C. CO2和H2完全转化为CH3OH和H2O
D. CO2、H2的反应速率等于CH3OH、H2O的反应速率且为零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH=CH2+HBr→CH3-CHBr-CH3(主要产物),1mol某烃充分燃烧后得8mol CO2 和4mol H2O ,该烃A在不同条件下能发生如下变化

(1)A的化学式:________,A的结构简式:________。
(2)上述反应中,①是________反应,⑦是________反应。(填反应类型)
(3)写出C、D、E、H物质的结构简式:C_____,D_______,E_______,H________。
(4)写出D→F反应的化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是制备某褪黑素受体激动剂的中间体,其合成路线如下:
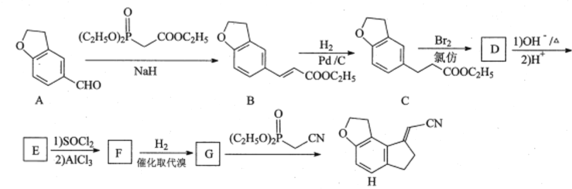
已知:RCOOH![]()
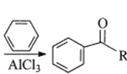 ,其中—R为烃基。
,其中—R为烃基。
(1)A中含氧官能团的名称为__________和__________。
(2)B→C的反应类型为___________。
(3)F的分子式为C11H8O2Br2,写出F的结构简式:________
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_____。
①能与FeCl3溶液发生显色反应;
②碱性条件水解生成两种产物,酸化后两种分子中均只有2种不同化学环境的氢。
(5)写出以![]() 和
和![]() 为原料制备
为原料制备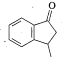 的合成路线流程图______________(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图______________(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于下列化学平衡在一定条件下发生移动的描述,不正确的是
A. Cl2+H2O![]() HCl+HClO,氯水中加入碳酸钙,漂白性增强
HCl+HClO,氯水中加入碳酸钙,漂白性增强
B. ZnS + Cu2+![]() CuS + Zn2+,闪锌矿(ZnS)遇CuSO4溶液转化为铜蓝(CuS)
CuS + Zn2+,闪锌矿(ZnS)遇CuSO4溶液转化为铜蓝(CuS)
C. 2NO2![]() N2O4 ΔH<0,将装有NO2的玻璃球浸入热水中,红棕色变浅
N2O4 ΔH<0,将装有NO2的玻璃球浸入热水中,红棕色变浅
D. Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色) +2H+,K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深
2CrO42-(黄色) +2H+,K2Cr2O7溶液中滴加几滴浓硫酸,橙色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种重要的结构陶瓷材料,可用作LED的基质材料,通过等离子法由SiH4(沸点-111.9℃)与氨气反应制取的方程式如下:3SiH4+4NH3=Si3N4+12H2。设NA是阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,1.8gSiH4所含质子的数目为3.2NA
B.标准状况下,4.48LNH3和H2的混合气体所含分子总数为0.2NA
C.NA个NH3分子溶于1L的水,所得溶液的物质的量浓度为1mol·L-1
D.当生成1molSi3N4时,转移电子数目为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属(M)空气电池的工作原理如图所示。下列说法正确的是( )
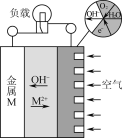
A.金属M作电池正极
B.电解质是熔融的MO
C.电路中转移2 mol电子,理论上约消耗空气56 L
D.电池总反应为2M+O2+2H2O=2M(OH)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com