
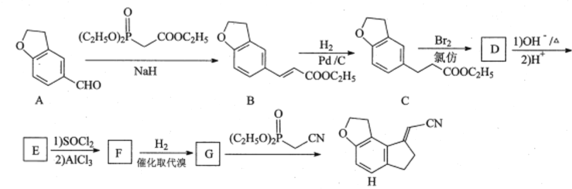
【题目】化合物H是制备某褪黑素受体激动剂的中间体,其合成路线如下:
已知:RCOOH![]()
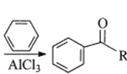 ,其中—R为烃基。
,其中—R为烃基。
(1)A中含氧官能团的名称为__________和__________。
(2)B→C的反应类型为___________。
(3)F的分子式为C11H8O2Br2,写出F的结构简式:________
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_____。
①能与FeCl3溶液发生显色反应;
②碱性条件水解生成两种产物,酸化后两种分子中均只有2种不同化学环境的氢。
(5)写出以![]() 和
和![]() 为原料制备
为原料制备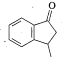 的合成路线流程图______________(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图______________(无机试剂任用,合成路线流程图示例见本题题干)。
【答案】醚键 醛基 加成反应 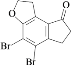
![]()
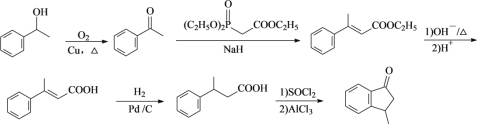 或
或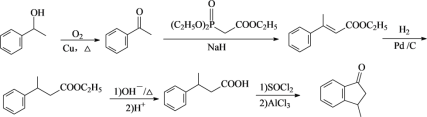
【解析】
A到B,A中的-CHO转化为-CH=CHCOOC2H5,B和H2发生加成,得到C,C和Br2发生反应,结合F的分子式C11H8O2Br2[问(3)提供的信息]以及F到G反应的条件提供的信息,C苯环上的H原子被Br取代,是为了E到F第二步成环的过程中,只有一种取向,则D的结构简式为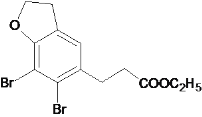 ,D到E,E中的酯基在碱性环境下发生水解,再酸化,得到羧基,E的结构简式为
,D到E,E中的酯基在碱性环境下发生水解,再酸化,得到羧基,E的结构简式为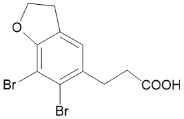 。根据已知信息,E到F,首先-COOH转化为-COCl,再在AlCl3的作用下成环,F的结构简式为
。根据已知信息,E到F,首先-COOH转化为-COCl,再在AlCl3的作用下成环,F的结构简式为 ,F到G,H取代F中的Br,G的结构简式为
,F到G,H取代F中的Br,G的结构简式为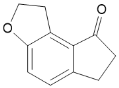 ,最后得到H。
,最后得到H。
(1)根据A的结构简式,A的含氧官能团有醛基、醚键;
(2)根据B和C的结构简式,可知B中的碳碳双键H2发生加成反应,得到C,该反应类型为加成(还原)反应;
(3)根据H的结构简式,以及A生成B的信息,可知G的结构简式为 ,再根据F与H2反应生成G,是H替代了Br,则F的结构简式为
,再根据F与H2反应生成G,是H替代了Br,则F的结构简式为 ;
;
(4)B的分子式为C13H14O3,与相同的碳原子数的烷烃少了14个H原子。B的同分异构体,能够与FeCl3溶液发生显色反应,说明含有酚羟基;能够碱性条件水解生成两种产物,则含有酯基,再酸化,理应得到酸和“醇”两种产物,但分子中均只有2种不同化学环境的氢,苯环上已有酚羟基,如果只有2种不同化学环境的氢,则两个取代基相同,且处于对位,可知水解后得到的不是醇羟基,而是酚羟基,第一种产物为对苯二酚,结构简式为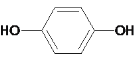 。根据水解方程式可知,另一种产物的分子式为C7H10O3,含有的-COOH,含有一种H原子,说明其他氢原子的化学环境相同,则含有-C(CH3)3的结构,根据分子式,可知分子中还含有碳碳三键,则羧酸的结构简式为(CH3)3C-C≡C-COOH。则B同分异构体的结构简式为
。根据水解方程式可知,另一种产物的分子式为C7H10O3,含有的-COOH,含有一种H原子,说明其他氢原子的化学环境相同,则含有-C(CH3)3的结构,根据分子式,可知分子中还含有碳碳三键,则羧酸的结构简式为(CH3)3C-C≡C-COOH。则B同分异构体的结构简式为![]() ;
;
(5)目标产物的结构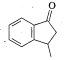 类似于F,根据题中的信息,得到F需要E,E中含有羧基,羧基来自与酯的水解,模仿A到B,在分子中引入酯基,根据A的结构,引入酯基,需要分子中含有碳氧双键,则
类似于F,根据题中的信息,得到F需要E,E中含有羧基,羧基来自与酯的水解,模仿A到B,在分子中引入酯基,根据A的结构,引入酯基,需要分子中含有碳氧双键,则![]() 发生催化氧化即可以引入碳氧双键,则合成路线流程图为
发生催化氧化即可以引入碳氧双键,则合成路线流程图为 或
或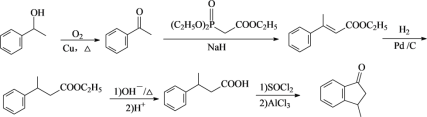 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】大环多醚称为冠醚。二苯并-18-冠-6的结构简式如图所示。下列说法不正确的是
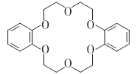
A.该有机物的分子式为C20H24O6
B.该有机物中所有原子不可能共平面
C.在光照下,该有机物与氯气反应的一氯代物有4种(不考虑立体异构)
D.1 mol该有机物的苯环最多可与6 mol H2发生加成反应(不考虑开环加成)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯酸钾熔化,粒子间克服了__的作用力;二氧化硅熔化,粒子间克服了__的作用力;碘的升华,粒子间克服了__的作用力.三种晶体的熔点由高到低的顺序是__.
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为__(填序号).
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有__,由非极性键形成的非极性分子有__,能形成分子晶体的物质是__,含有氢键的晶体的化学式是__,属于离子晶体的是__,属于原子晶体的是__,五种物质的熔点由高到低的顺序是__.
(4)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__.
(5)图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:
A.__;B.__;C.__;D.__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,用排饱和食盐水法先后收集20mL甲烷和80mL氯气,放在光亮的地方(注意:不要放在日光直射的地方,以免引起爆炸),等待片刻,观察发生的现象。回答下列问题:
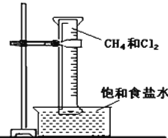
(1)大约30min后,可以观察到量筒内壁出现___________状液体,量筒内液面___________(填“上升”、“下降”或“不变”)。
(2)使1mol甲烷和氯气发生取代反应,生成相同物质的量的四种有机取代物,则需要氯气的物质的量是___________,写出其中常作为有机溶剂和灭火剂的物质的电子式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2.0L的恒容密闭容器中充入3.0molCl2和4.0molPCl5,473K 时发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1,各物质的物质的量随时间变化关系如图所示:
PCl3(g)+Cl2(g)△H= 92.5 kJ·mol-1,各物质的物质的量随时间变化关系如图所示:
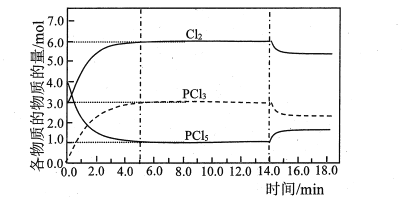
下列说法正确的是
A.0.0~5.0min,PCl5分解的平均速率为0.6mol·L-1·min -1
B.起始时,若用3.0mol37Cl2和4.0mol P35Cl5,达平衡时,PCl3 中不含37C1
C.图中14.0min时,改变的外界条件可能是缩小容器的体积
D.若在14.0min时,向容器中各充入1.0mol 的Cl2、PCl5 及PCl3,维持其他条件不变,重新达到平衡前,v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其合金可用作材料、铝热剂等,在环境修复等方面也有着巨大的应用潜力。
(1)铝的冶炼、提纯的方法很多。
①高温碳热歧化氯化法冶铝包含的反应之一为:Al2O3(s)+AlCl3(g)+3C(s)![]() 3CO(g)+3AlCl(g),其平衡常数表达式为K=_______________。
3CO(g)+3AlCl(g),其平衡常数表达式为K=_______________。
②碳热还原Al2O3冶铝的部分反应如下:
Ⅰ.2Al2O3(s)+9C(s)=Al4C3(s)+6CO(g) △H1=akJ/mol
Ⅱ. 4Al2O3(s)+Al4C3(s)=3Al4O4C(s) △H2=bkJ/mol
Ⅲ. Al4O4C(s)+Al4C3(s)=8Al(g)+4CO(g) △H3=ckJ/mol
反应Al2O3(s)+3C(s)=2Al(g)+3CO(g)的△H=__________kJ/mol
③用离子液体AICb-BMIC(阳离子为EMIM+、阴离子为AlCl4-、Al2Cl7-)作电解质,可实现电解精炼铝。粗铝与外电源的_____________极(填“正”或“负")相连;工作时,阴极的电极反应式为_______________。
(2)真空条件及1173K时,可用铝热还原Li5AlO4制备金属锂(气态),写出该反应的化学方程式:__________________________。
(3)用Al、Fe或Al-Fe合金还原脱除水体中的硝态氮(NO3--N),在45℃,起始c(KNO3-N)为50mg·L-1、维持溶液呈中性并通入Ar等条件下进行脱除实验。结果如图所示(c0为起始浓度、c为剩余浓度):
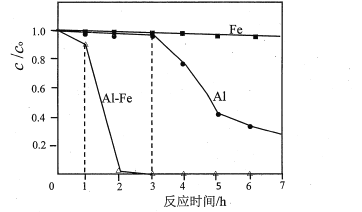
①纯Al在0~3h时,NO3-几乎没有被脱除,其原因是_______________________;写出3h后NO3-被还原为N2的离子方程式:____________________________。
②Al-Fe合金1~2h比纯A13~4h的脱除速率快得多的可能原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青菜含有维生素C和植物纤维有助于清除人体吸入的粉尘颗粒。已知维生素C的结构如图所示,有关判断不正确的是

A. 维生素C中含有3种官能团
B. 维生素C分子式为C6H8O6
C. 维生素C能使酸性高锰酸钾溶液褪色
D. 维生素C在碱性溶液中能稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍(Ni)及其化合物广泛应用于生产电池、电镀和催化剂等领域。
(1)某蓄电池反应为2NiO(OH)+Cd+2H2O![]() Cd(OH)2+2Ni(OH)2。该蓄电池充电时,被氧化的物质是__(填化学式),放电时若生成73gCd(OH)2,则外电路中转移的电子数是___。
Cd(OH)2+2Ni(OH)2。该蓄电池充电时,被氧化的物质是__(填化学式),放电时若生成73gCd(OH)2,则外电路中转移的电子数是___。
(2)镍的羰化反应为:Ni(s)+4CO(g)![]() Ni(CO)4(g) ΔH。
Ni(CO)4(g) ΔH。
①一定温度下,将一定量的粗镍和CO加入到1L的恒容密闭容器中反应,5s后测得Ni(CO)4的物质的量为1.5mol,则0~5s内平均反应速率v(CO)=__mol·L·s-1。
②该反应的平衡常数K随温度升高而减小,则该反应的ΔH__0(填“>”或“<")。
(3)NiSO4·6H2O晶体是一种绿色易溶于水的晶体,广泛应用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Zn、Fe等元素)为原料制取。制取步骤如下:
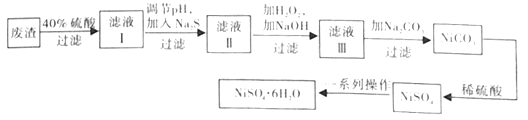
①在实验室中,欲用98%的浓硫酸(密度1.84g·mL-1)配制40%的稀硫酸,需要的玻璃仪器除玻璃棒外,还有__。
②向滤液Ⅰ中加入Na2S的目的是_。(已知:Ksp[FeS]=6.3×10-18,Ksp[CuS]=1.3×10-36,Ksp[ZnS]=1.3×10-24,Ksp[NiS]=1.1×10-21)
③滤液Ⅲ中所含的阳离子主要有__。
④NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiOOH。该反应的离子方程式为__。
⑤在制备NiSO4·6H2O晶体时,常用无水乙醇代替蒸馏水做洗涤剂,原因是__(写出一条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种可再生绿色新能源,被誉为“21世纪的清洁燃料”。
(1)写出二甲醚一种同分异构体的结构简式:____________。
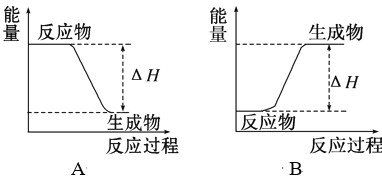
(2)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)是____________反应(填“吸热”或“放热”),该反应过程的能量变化示意图可用下图中的____________表示(填“A”或“B”)。
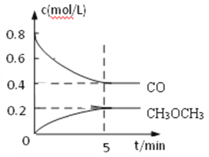
(3)工业上可用水煤气合成二甲醚:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)
①测得CO和CH3OCH3(g)的浓度随时间变化如图所示,则反应开始至平衡时CO的平均反应速率v(CO)=________mol/(L·min)。
②该反应在恒容密闭容器中进行,下列叙述中能表示该反应达到平衡状态的是____________。
A.单位时间内生成CO和H2的物质的量之比为1﹕2
B.CH3OCH3的浓度不再变化
C.容器内压强不再变化
D.CH3OCH3与H2O的物质的量相等
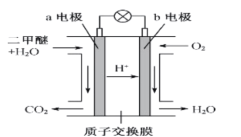
(4)二甲醚燃料电池工作原理如图所示,则a电极的电极名称为____________极(填“正”或“负”)。
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com