
【题目】实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如图所示.回答下列问题:
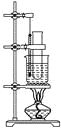
(1)反应需在50℃~60℃的温度下进行,图中给反应物加热的方法是________,其优点是________和________;
(2)在配制混合酸时应将__________加入到________中去;
(3)该反应的化学方程式是___________________________________________;
(4)由于装置的缺陷,该实验可能会导致的不良后果是________。
【答案】水浴加热 便于控制温度 受热均匀 浓硫酸 浓硝酸  苯、浓硝酸等挥发到空气中,造成污染
苯、浓硝酸等挥发到空气中,造成污染
【解析】
(1)图中给反应物加热的方法是水浴加热,水浴加热便于控制温度,受热均匀;
(2)配制混合酸时应将浓硫酸加入浓硝酸中,并不断振荡,以防止溅出伤人;
(3)苯与浓硝酸在浓硫酸、加入条件下发生取代反应生成硝基苯与水;
(4)由于苯和硝酸都是易挥发、有毒的物质,设计实验时应考虑它们可能产生的污染和由挥发导致的利用率降低。
(1)图中给反应物加热的方法是水溶加热,水域加热便于控制温度,受热均匀,
故答案为:水浴加热;便于控制温度、受热均匀。
(2)配制混合酸时应将密度大的浓硫酸加入到密度小的浓硝酸中去,配制混合酸时应将浓硫酸加入浓硝酸中,并不断振荡,以防止溅出伤人,
故答案为:浓硫酸、浓硝酸;
(3)苯与浓硝酸在浓硫酸、加入条件下发生取代反应生成硝基苯与水,反应方程式为:![]() ,
,
故答案为:![]() 。
。
(4)由于苯和硝酸都是易挥发、有毒的物质,应考虑它们可能产生的污染和由挥发导致的利用率降低,装置缺少冷凝回流装置,
故答案为:苯、浓硝酸等挥发到空气中,造成污染。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】我国规定饮用水质量标准必须符合下表所示要求:
项目 | pH | Ca2+、Mg2+总浓度 | 细菌个数 |
相关值 | 6.5~8.5 | <0.0045mol·L-1 | <100个·mL-1 |
下图是源水处理成自来水的工艺流程示意图。
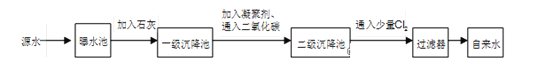
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,在一级沉降池中所得沉淀的主要成分为 _____ 和_______ (化学式)。
(2)FeSO4·7H2O是常用的凝聚剂,它在水中最终生成胶状Fe(OH)3沉淀。凝聚剂除去悬浮固体颗粒的过程______________(填写编号)。
①只是物理过程; ②只是化学过程; ③是物理和化学过程。
(3)Cl2的作用是______ ,这种作用是基于Cl2和水反应的产物具有 _______ 性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期,世界范围内有许多湖泊为鱼类绝迹的死湖,数以千万公顷的森林衰败枯萎,大片土地沙漠化……将这些现象与频繁降落的酸雨相联系,人们认为,酸雨是肇事主因。某研究小组研究某地硫酸型酸雨的形成,有人提出以下猜想:
猜想一:SO2![]() SO3
SO3![]() H2SO4
H2SO4
猜想二:SO2![]() H2SO3
H2SO3![]() H2SO4
H2SO4
猜想三:以上两过程同时存在( )
有关上述猜想,收集一定量该地区刚下的雨水进行实验,下列判断中错误的是( )
A.若猜想一或猜想三正确,则该雨水加入盐酸后,再加入BaCl2溶液,有白色沉淀生成
B.若存在猜想二的过程,则该雨水可能使品红溶液褪色
C.若只存在猜想一的过程,则该雨水的pH随时间延长而增大
D.上述任意一个猜想正确,该地区雨水的pH均小于5.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组进行Na2O2与水反应的实验,如下图所示,该小组对试管c中红色褪去的原因进行探究。
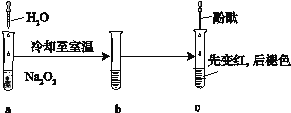
(1)Na2O2中含有的化学键类型:__________;请写出a中反应的化学方程式______。
查阅资料:
①当NaOH溶液pH≥13时,可以使酚酞由红色褪为无色;
②Na2O2与水反应分两步进行:Na2O2+ H2O =" NaOH" + H2O22H2O2= 2H2O + O2↑
(2)请设计实验验证Na2O2与水反应后的溶液中有H2O2残留:取少量b溶液于试管中,____________,证明溶液中有H2O2残留。
(3)结合资料,该小组同学针c中溶液红色褪去的原因提出以下假设:
①_____________________;
② 溶液中H2O2破坏酚酞的结构;
③ NaOH和H2O2共同作用结果。
(4)该小组同学测出c中溶液的pH为14,认为还不能排除假设②、③,于是又进行了如下实验,请完成下表空白处:
实验 | 操作 | 现象 | 结论 |
1 | 向少量H2O2中滴加2滴酚酞,放置一段时间,再加入NaOH溶液至pH=12 | 加入NaOH后,无色溶液先变红,后褪色 | ①___________ |
2 | 向少量 NaOH溶液(pH=14)中滴加2滴酚酞;再加适量稀盐酸至溶液 pH=12 | 溶液先变红,后褪色;加盐酸后,又出现红色,且不褪色 |
|
3 | 向Na2O2与水反应后的溶液(pH=14)中滴加2滴酚酞;再加适量稀盐酸至溶液 pH=12…… | ②_____________________________…… | 溶液pH大于13时,NaOH使变红的溶液褪色;pH在8~13时, NaOH和H2O2共同作用使溶液褪色 |
(5)某同学按取(4)中述实验2褪色后的溶液,加水稀释至pH=12,没有观察到溶液变红。该同学推测实验2加盐酸后溶液变红还可能与温度有关,请写出理由:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃含C 85.7%,含H 14.3%,在标准状况下的密度是2.5g/L.经红外光谱测定该烃分子中含一个双键.
(1)求该烃的实验式;
(2)求该烃的分子式;
(3)并写出它的各种同分异构体的结构简式及名称.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分.该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊又变澄清,由此该小组成员对气体的成分提出猜想.
(提出猜想)
猜想1:
猜想2:
猜想3:
为了验证猜想,该小组设计实验加以探究.
(实验探究)该小组同学按如图所示装置,将气体从a端通入,则;

![]() 中应该装 ______ 试剂
中应该装 ______ 试剂![]() 填编号
填编号![]() .
.
A 氢氧化钠溶液 ![]() 酸性高锰酸钾溶液
酸性高锰酸钾溶液 ![]() 饱和碳酸钠溶液
饱和碳酸钠溶液 ![]() 饱和碳酸氢钠
饱和碳酸氢钠
![]() 中品红溶液的作用是 ______ .
中品红溶液的作用是 ______ .
![]() 中澄清石灰水的作用是 ______ .
中澄清石灰水的作用是 ______ .
通过该实验,该小组同学观察到以下三个实验现象:
①![]() 中品红溶液褪色②
中品红溶液褪色②![]() 中品红溶液不褪色③
中品红溶液不褪色③![]() 中澄清石灰水变浑浊
中澄清石灰水变浑浊
(得出结论)
![]() 由上述现象该小组同学确认该气体为 ______ .
由上述现象该小组同学确认该气体为 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由黄铜矿![]() 主要成分
主要成分![]() ,质量分数为
,质量分数为![]() 冶炼铜的主要流程如图:
冶炼铜的主要流程如图:
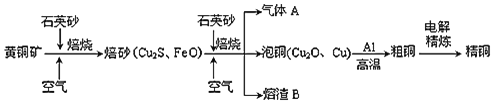
己知:一定条件下,铝可以和某些金属氧化物反应置换金属。
(1)高温焙烧前要将黄铜矿粉碎的目的是______。
(2)气体A中的大气污染物可选用下列试剂中的______吸收。
![]() 浓
浓![]()
![]() 稀
稀![]()
![]() 溶液
溶液![]() 氨水
氨水
(3)用稀![]() 浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在______,欲检验溶液中还存在
浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在______,欲检验溶液中还存在![]() ,所需试剂是______。
,所需试剂是______。
(4)由泡铜冶炼粗铜的化学反应方程式为______。
(5)某同学用铜、稀硫酸和![]() 制备
制备![]() 溶液,其化学反应方程式为______。
溶液,其化学反应方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求对下图中两极进行必要的连接并填空:

(1)在A图中,使铜片上冒气泡。请加以必要联接,则联接后的装置叫_______________。电极反应式:锌电极:________________________________;铜电极:_____________________________。
(2)在B图中(a,b都为惰性电极),使a极析出铜,则b析出:_______________。加以必要的联接后,该装置叫________________。电极反应式: b极:________________________________。经过一段时间后,停止反应并搅均溶液,溶液的pH值____________(升高、降低、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。下列判断正确的是

A. e、f两管中的试剂可以分别是浓氨水和NaOH固体
B. 玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
C. c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
D. Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com