
【题目】我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:气体A的饱和溶液![]() A和食盐的饱和溶液
A和食盐的饱和溶液![]() 悬浊液
悬浊液![]() 晶体
晶体![]() 纯碱,则下列叙述错误的是( )
纯碱,则下列叙述错误的是( )
A.A气体是CO2,B气体是NH3
B.第Ⅲ步得到的晶体是发酵粉的主要成分
C.第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D.第Ⅳ步操作的主要过程有溶解、蒸发、结晶
科目:高中化学 来源: 题型:
【题目】某有机物M的结构简式如下,在足量NaOH水溶液中加热,然后用足量盐酸酸化后得到三种不同的有机物A、B、C,且A、B、C中所含碳原子数依次增加。回答下列问题:
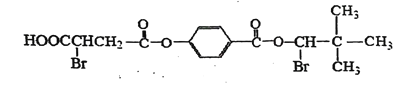
已知:同一个碳原子上结合两个羟基会自动脱水生成醛基。
(1) 1mol M加热条件下与足量的NaOH水溶液反应,消耗NaOH的物质的量为___。
(2) B中含有的官能团名称为____。
(3) C不能发生的反应类型有____。(填序号)
①加成反应②消去反应③显色反应④取代反应
(4)A在浓H2SO4作用下可生成六元环状化合物,其化学方程式为___。
(5)A的两种同分异构体E、F分别有如下特点:
①lmol E或F可以和3mol Na发生反应,放出标准状况下33.6L H2;
②lmol E或F可以和足量NaHCO3溶液反应,生成lmol CO2;
③lmol E或F可以发生银镜反应,生成2mol Ag。
则E和F的结构简式分别是_____、_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】MnO2在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO2(含有杂质MnO和MnCO3)制取纯MnO2的流程如图。
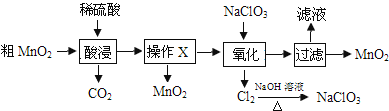
下列说法错误的是( )
A.酸浸过程中稀硫酸可用稀硝酸、稀盐酸代替
B.操作X的名称是过滤
C.氧化过程发生反应的离子方程式为5Mn2++2ClO![]() +4H2O=5MnO2↓+Cl2↑+8H+
+4H2O=5MnO2↓+Cl2↑+8H+
D.电解MnSO4溶液也可制得MnO2,阳极电极式为Mn2+-2e-+2H2O=MnO2↓+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸阿比多尔是一种盐酸盐,其主要作用是通过抑制流感病毒脂膜与宿主细胞的融合而阻断病毒的复制,结构如图。回答下列问题:
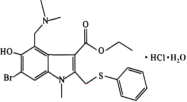
(1)盐酸阿比多尔中所含N、O、S三种元素第一电离能由大到小的顺序为___。O原子核外有___种不同运动状态的电子,基态S原子的价电子排布图不是![]() ,是因为该排布方式违背了___。
,是因为该排布方式违背了___。
(2)该结构中N原子的杂化方式是___。已知在氨分子中,H—N—H键角为107.3°,但是在[Zn(NH3)6]2+离子中H—N—H键角变为109.5°,分析原因为___。
(3)盐酸阿比多尔中不含有的化学键类型为___(填选项字母)。
A.离子键 B.配位键 C.金属键 D.σ键 E.π键 F.极性键 G.非极性键
(4)以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点。GaN晶胞如图1所示,图2为晶胞沿y轴的投影1∶1平面图。
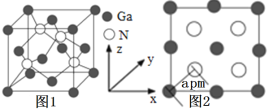
①氮化硼与氮化镓的结构类似,氮化硼熔点3000℃,氮化镓熔点1700℃,分析它们熔点不同的原因____。
②晶胞中与一个Ga原子距离最近且相等的N原子有____个。
③设阿伏加德罗常数的值为NA,则该晶胞的密度是___g·cm3(列出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下面两种方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入__。
(2)除去蒸馏水中溶解的O2常采用___的方法。
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是__。
方法二:在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。
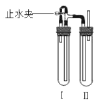
(1)在试管I里加入的试剂是___。
(2)在试管II里加入的试剂是___。
(3)为了制得白色Fe(OH)2沉淀,在试管I和II中加入试剂,打开止水夹,塞紧塞子后的实验步骤是:先___,后__。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,用0.1 mol·L-1NaOH溶液分别滴定20.00mL 0.1 mol·L-1的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是
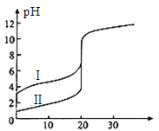
A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.pH=7时,滴定盐酸和醋酸消耗NaOH溶液的体积相等
C.V(NaOH)=10.00mL时,醋酸溶液中c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
D.V(NaOH)=20.00mL时,两溶液中c(CH3COO-)> c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是一种重要金属:
(1)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为:___
(2)铝与NaOH溶液反应的离子方程式为:___。
(3)工业上用铝土矿(主要成分为A12O3,还有少量的Fe2O3,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
①I和II步骤中分离溶液和沉淀的操作是;___;
②沉淀M中除含有泥沙外,一定还含有___,固体N是___;
③滤液X中,含铝元素的溶质的化学式为___,它属于___(填“酸”、“碱”或“盐”)类物质;
④实验室里常往AlCl3溶液中加入___(填“氨水”或“NaOH溶液”)来制取A1(OH)3。其反应的离子方程式为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞试液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是____。若测定结果偏高,其原因可能是_____。
A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装待测液的锥形瓶用蒸馏水洗过后未用待测液润洗
D.滴定管滴定前无气泡,滴定后有气泡
(2)判断滴定终点的现象是________。
(3)如图是某次滴定时的滴定管中的液面,其读数为_____mL。
![]()
(4)根据下列数据,请计算待测盐酸的浓度:_________mol·L-1。
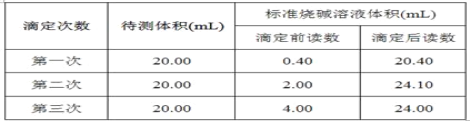
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态,其电路工作原理如图所示。下列说法中正确的是( )
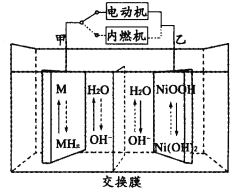
A.放电时乙为正极,充电时乙为阴极
B.汽车上坡时发生图中虚线所示的过程
C.放电时负极的电极反应式为:MHn-ne-=M+nH+
D.电池充电时,OH-由甲侧向乙侧移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com