
【题目】下列各组离子中,因发生氧化还原反应而不能大量共存的是( )
A. K+、H+、Fe2+、NO3-B. Fe3+、Ba2+、SO42-、NO3-
C. Al3+、Na+、SO42-、CO32-D. Fe3+、H+、SO42-、ClO﹣
科目:高中化学 来源: 题型:
【题目】Ⅰ.下图所示是分离混合物时常用的仪器,回答下列问题:

(1)写出仪器C、E的名称分别是_______________、______________。
(2)若向C装置中加入碘水和足量CCl4,充分振荡后静置,观察到现象是:C内液体分两层,上层液体呈________色,下层液体呈______________色。
(3)碘单质和溴单质有相类似的性质,都可以用有机溶剂萃取水溶液中的单质,若利用C仪器提取溴水中的溴单质,下列有机溶剂中不能选用的是_____________(填字母)。
A.汽油 B.CCl4 C.酒精 D.苯
Ⅱ.配制一定物质的量浓度的溶液是化学实验室的基本实验操作之一。请回答下列问题:
(1)配制0.5 mol/L的硫酸溶液450 mL,需用量筒量取质量分数98%、密度1.84 g/cm3的浓硫酸的体积为_____mL,如果实验室有15 mL、20 mL、50 mL 量筒,应最好选用_____mL量筒。
(2)配制上述溶液,除用到量筒、烧杯、玻璃棒外,还需要的两种玻璃仪器是________________。
(3)关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是__________(填字母)。
A.①②③④ B.②③ C.①②④ D.②③④
(4)配制时,其正确的操作顺序是__________(用字母表示,每个操作只用一次)。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有水的烧杯中加入浓硫酸稀释
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(5)下面操作造成所配稀硫酸溶液浓度偏高的是___________(填序号)。
A.浓硫酸稀释后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量浓硫酸后洗涤量筒并将洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用双线桥法标出下列反应中电子转移的方向和数目:
3Cu + 2NO3— + 8H+![]() 3Cu2+ + 2NO↑ + 4H2O __________________
3Cu2+ + 2NO↑ + 4H2O __________________
(1)此反应中,还原剂是 _____,氧化剂是 _____;__元素被还原。
(2)由此可知,氧化还原反应的实质是__________________________。
(3)据你的理解再写一个常见的氧化还原反应的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,炽热的铁与水蒸气在一个体积不变的密闭容器中进行反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是( )
A. 把铁块变成铁粉B. 升高温度
C. 增加铁的量D. 增加水蒸气的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
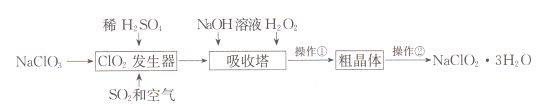
已知:①HC1O2可视为强酸,NaClO2的溶解度随温度升高而增大。②ClO2的沸点为283K,纯ClO2易分解爆炸。回答下列问题:
(1)ClO2发生器中发生反应的离子方程式为____;向其中鼓入空气的作用可能是____。
(2)吸收塔中发生反应的化学方程式为____;为防止生成的NaClO2被继续还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是____(填序号)。
A.Na2O2 B.Na2S C. FeCl2 D.KMnO4
(3)操作①的实验方法依次是_____、_____、过滤;操作②实验方法是_____。
(4)akg NaClO3理论上可制___ kg NaClO2·3H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关13C、15N的叙述正确的是( )
A. 13C与15N有相同的中子数B. C60与13C互为同素异形体
C. 15N与14N互为同位素D. 15N的核外电子数与中子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质溶液的电导率越大,导电能力越强。用 0.100 mol·L-1 的 NaOH 溶液滴定 10.00 mL 浓度均为 0.100 mol·L-1 的盐酸和 CH3COOH 溶液。利用传感器测得滴定过程中溶液的电导 率如图所示。下列说法正确的是( )

A. 曲线①代表滴定 HCl 溶液的曲线
B. A 点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.1 mol·L-1
C. 在相同温度下,A、B、C 三点溶液中水的电离程度:C<B=A
D. D 点溶液中:c(Cl-)=2c(OH-)-2c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰化钠是一种重要的基本化工原料,同时也是一种剧毒物质。一旦泄漏需要及时处理,一般可以通过喷洒双氧水或过硫酸钠(Na2S2O8)溶液来处理,以减轻环境污染。
Ⅰ.已知:氰化钠是一种白色结晶颗粒,化学式为NaCN,有剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。
(1)请用最常见的试剂和简单操作设计实验证明N、C元素的非金属性强弱:__________________(只说明操作及现象)。
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,该反应的离子方程式是___________________________。
Ⅱ.工业制备过硫酸钠的反应原理如下:
主反应:(NH4)2S2O8+2NaOH![]() Na2S2O8+2NH3
Na2S2O8+2NH3![]() +2H2O
+2H2O
副反应:2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
某化学兴趣小组利用上述原理在实验室制备过硫酸钠,并检测用过硫酸钠溶液处理后的氰化钠废水是否达标排放。
(实验一)实验室通过如图所示装置制备Na2S2O8。
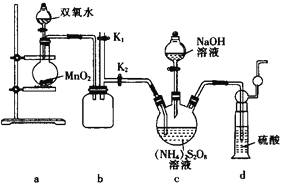
(3)欲控制通入O2的通入速率,采取的有效措施为____________________(答一条)
(4)装置a中反应产生的气体需要持续通入装置c的原因是____________________。
(5)上述装置中还需补充的实验仪器或装置有_______(填字母)。
A.温度计 B.洗气瓶 C.水浴装置 D.酒精灯
(实验二)测定用过硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50 mg·L-1。
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI![]() ,AgI呈黄色,且CN-优先与Ag+反应。实验如下:取100.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4 mol·L-1的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50 mL。
,AgI呈黄色,且CN-优先与Ag+反应。实验如下:取100.00 mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4 mol·L-1的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50 mL。
(6)滴定终点的现象是________________________________________。
(7)处理后的废水中氰化钠的浓度为________mg·L-1。(保留3位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将4molA和3molB充入体积为1L的密闭容器中,发生如下反应:aA(g)+2B(g)![]() 3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com