
【题目】1,2二氯乙烷是一种广泛使用的有机溶剂、黏合剂,也用作谷物和粮仓的熏蒸剂,沸点83.5 ℃,熔点35 ℃。某研究性学习小组的同学利用下图(加热装置省略)装置制备一定量的 1,2二氯乙烷,制备原理为:C2H5OH![]() C2H4
C2H4![]() CH2ClCH2Cl。装置A中的浓硫酸是催化剂、脱水剂,乙醇的密度约为0.8 g·mL1。
CH2ClCH2Cl。装置A中的浓硫酸是催化剂、脱水剂,乙醇的密度约为0.8 g·mL1。
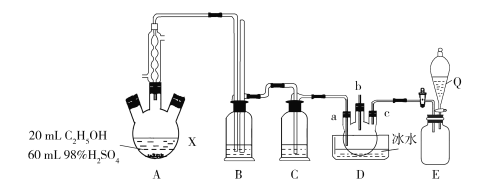
(1)根据制备原理,可知装置A中还缺少的一种实验仪器是_____。使用冷凝管的目的是_______。
(2)实验时A中三颈烧瓶内有刺激性气味的无机气体产生,为吸收反应中生成的无机气体,在装置B中应加入________(填字母)。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)D中a、c两个导管进入仪器中的长度不同,其优点是________,对导管b的进一步处理方法是_____________,装置E是氯气的贮气瓶,则Q中的物质是______________。
(4)写出D中反应的化学方程式________________________。
(5)若得到a g 1,2-二氯乙烷,则乙醇的利用率为___________。
【答案】温度计 使乙醇冷凝回流,提高原料的利用率 c 有利于Cl2、C2H4充分混合反应 将用b管逸出的Cl2引入到NaOH溶液中 饱和食盐水 CH2=CH2+ Cl2![]() CH2ClCH2Cl
CH2ClCH2Cl ![]()
【解析】
(1)A中反应需控制温度在170 ℃,所以还缺少的仪器是温度计。由于反应温度高于乙醇的沸点,反应中会有大量的乙醇气化,因此使用冷凝管的目的是使已经气化的乙醇冷凝回流,提高乙醇的利用率。
(2)浓硫酸能使乙醇碳化生成单质碳,C与浓硫酸反应生成的CO2、SO2,可用NaOH溶液吸收除去。
(3)C2H4密度小而Cl2的密度大,按图中方式将两种气体通入到容器中,有利于二者充分混合反应。Cl2有毒且在容器中难以完全反应,故要将从b中逸出的Cl2通入到NaOH溶液中,防止其污染空气。Q中液体下滴,从而将Cl2排入到D中,因此Cl2不能被Q中液体吸收或溶解,故Q中是饱和食盐水。
(5)由C2H5OH~C2H4Cl2可求出转化为C2H4Cl2的乙醇质量为46a/99 g,20 mL乙醇质量为16 g,故乙醇的利用率为![]() 。
。
(1)A中反应需控制温度在170 ℃,所以还缺少的仪器是温度计。由于反应温度高于乙醇的沸点,反应中会有大量的乙醇气化,因此使用冷凝管的目的是使已经气化的乙醇冷凝回流,提高乙醇的利用率,答案为:温度计;使乙醇冷凝回流,提高原料的利用率。
(2)浓硫酸能使乙醇碳化生成单质碳,C与浓硫酸反应生成的CO2、SO2,可用NaOH溶液吸收除去,答案为:c。
(3)C2H4密度小而Cl2的密度大,按图中方式将两种气体通入到容器中,有利于二者充分混合反应。Cl2有毒且在容器中难以完全反应,故要将从b中逸出的Cl2通入到NaOH溶液中,防止其污染空气。Q中液体下滴,从而将Cl2排入到D中,因此Cl2不能被Q中液体吸收或溶解,故Q中是饱和食盐水,答案为:有利于Cl2、C2H4充分混合反应;将用b管逸出的Cl2引入到NaOH溶液中;饱和食盐水。
(4)装置D中为乙烯与氯气的加成反应,其反应式为:CH2=CH2+ Cl2![]() CH2ClCH2Cl;
CH2ClCH2Cl;
(5)由C2H5OH~C2H4Cl2可求出转化为C2H4Cl2的乙醇质量为46a/99 g,20 mL乙醇质量为16 g,故乙醇的利用率为![]() 。
。


科目:高中化学 来源: 题型:
【题目】有机物甲的分子式为C4H9Br,在适宜的条件下能发生如下转化关系:
B![]() A
A![]() 甲(C4H9Br)
甲(C4H9Br)![]() D
D![]() E
E
已知:B能发生银镜反应,核磁共振氢谱显示其有三个吸收峰。试回答下列问题:
(1)甲的名称:____。甲生成A的反应类型是___。
(2)B与新制氢氧化铜悬浊液反应的化学方程式:____。
(3)甲与NaOH醇溶液共热的化学方程式为:___。
(4)A的同类同分异构体中,不能被催化氧化的物质的结构简式为___。
(5)D生成E的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+B(g)![]() 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
A. v(A)=0.15mol·(L·min) -1B. v (B)=0.2 mol·(L·min) -1
C. v (C)=0.3 mol·(L·min) -1D. v (D)=0.1 mol·(L·min) -1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿巴卡韦(Abacavir)是一种核苷类逆转录酶抑制剂,存在抗病毒功效。关于其合成中间体M(![]() ),下列说法正确的是( )
),下列说法正确的是( )
A.与环戊醇互为同系物
B.分子中所有碳原子共平面
C.能使酸性高锰酸钾溶液和溴水褪色,且反应类型相同
D.可用碳酸钠溶液鉴别乙酸和M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。下列说法正确的是
A.常温常压下,2.8g 由CO与CO2组成的混合物中含有的质子总数为1.4NA
B.标准状况下,22.4 L H2O中含有的分子数为NA
C.2.3g Na与100 mL 0.1mol·L-1盐酸反应,转移的电子数为0.01NA
D.1L 1 mol·L-1 CaCl2溶液中含有的氯离子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石蜡是石油减压分馏的产品,某实验小组利用如图的实验探究石蜡油(液态石蜡)分解的部分产物。下列说法正确的是( )
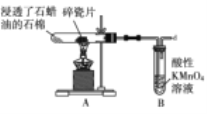
A.石蜡属于油脂
B.该实验证明石蜡油分解产物只有乙烯
C.B中发生氧化反应,所以溶液褪色
D.碎瓷片的作用是防止暴沸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2 mol·L-1的CH3COOH溶液中,当CH3COOH![]() H++CH3COO-已达平衡时,若要使CH3COOH的电离程度减小,溶液中的c(H+)增大,应加入( )
H++CH3COO-已达平衡时,若要使CH3COOH的电离程度减小,溶液中的c(H+)增大,应加入( )
A.CH3COONa固体B.氨水C.HClD.H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。已知Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
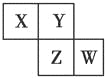
A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:Z>W>X
C. 氢化物的稳定性:X>Y>Z
D. 四种元素的单质中,Z单质的熔、沸点最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用如图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:
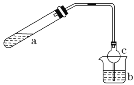
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,正确的加入顺序及操作是______。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是_____________________。
(3)实验中加热试管a的目的是:
①_____________________________________________________;
②______________________________________________________。
a中反应的化学方程式:__________________________________。
(4)球形干燥管c的作用是_________________________________, b烧杯中加有饱和Na2CO3溶液,其作用是_____________________。
(5)若反应前向b中加入几滴酚酞,溶液呈红色,反应结束后b中的现象是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com