
【题目】室温下,某兴趣小组用下图装置在通风橱中进行如下实验:

下列说法正确的是
A. 试管 I 中浅红棕色气体为 NO2,由硝酸还原生成
B. 等质量的 Cu 完全溶解时, I 中消耗的 HNO3 更多
C. 换成 Fe 之后重复实验,依然是试管 II 中反应更剧烈
D. 试管 II 中反应后溶液颜色与试管 I 中的不同, 是由于溶有 NO2
【答案】D
【解析】A. 试管 I 中浅红棕色气体为NO和NO2的混合物,Cu与稀硝酸反应,硝酸被还原为NO,部分NO遇到空气中的氧气被氧化为红棕色的NO2,A不正确;B. 等质量的 Cu 完全溶解时, 因稀硝酸被还原为NO,N的化合价由+5降到+2,而浓硝酸被还原为NO2,N的化合价由+5降低到+4,故I 中消耗的 HNO3 较少,B不正确;C. 换成 Fe 之后重复实验,Fe遇浓硝酸发生钝化,试管 II 中无明显变化,C不正确;D.试管II中持续通入氮气后,可以把溶液中溶解的NO2带走,溶液由绿色变为蓝色,说明试管 II 中反应后溶液颜色与其溶解的NO2有关,D正确。本题选D。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】实验室利用下图装置制备H2S气体,并探究H2S的有关性质。回答下列问题:
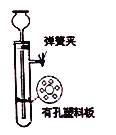
(1)实验开始时,检查装置气密性的方法是_________________。
(2)若装置不漏气,加入装置中的药品为_________(填字母)。
a.FeS和稀硫酸 b.Na2S和稀硫酸 C.ZnS和稀硝酸d.CuS和稀盐酸
该反应的离子方程式为_________________。
(3)打开弹簧夹使反应发生,将生成的H2S气体通入1.0mol/LFe(NO3)3溶液中,观察到有浅黄色固体析出。为探究实际参与该反应的微粒种类,设计如下图装置:

若A装置中加入1.0mol/L的FeCl3溶液,并测其pH=1,则B装置中加入的试剂是______;实验观察到A、B中均有浅黄色固体析出,则H2S与Fe(NO3)3溶液反应的离子方程式为_______。
(4)实验结束时,使反应停止的操作是______;此时反应停止的原因是______________。
(5)常温下,以Na2S为样品,选择合理的仪器和试剂设计实验①证明氢硫酸为二元弱酸②测量并估算氢硫酸的Ka2(H2S),则需要的主要计量仪器为电子天平、容量瓶、_____、_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是重要的化工原料,在工业上可用于制造化肥、农药、炸药和染料等。下列关于浓硝酸性质的描述不正确的是
A.难挥发B.能溶于水C.能与碳反应D.能与氨气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜是一种重要的化工原料,广泛应用于有机合成、石油、油脂、染料等工业。一种利用低品位铜矿(Cu2S、CuS及FeO和Fe2O3等)为原料制取CuCl的工艺流程如下:
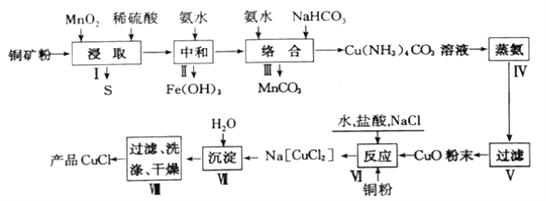
回答下列问题:
(1)步骤Ⅰ“浸取”前需将铜矿粉碎的目的是______;“浸取”时,被氧化的元素有___(填元素符号)。
(2)已知Cu2+、Mn2+、Fe3+开始生成沉淀和沉淀完全的pH如下表,则步骤Ⅱ“中和”时,pH应控制的范围为_______________;
物质 | Cu(OH)2 | Mn(OH)2 | Fe(OH)3 |
开始沉淀pH | 4.7 | 8.3 | 1.2 |
完全沉淀pH | 6.7 | 9.8 | 3.2 |
已知25℃时Ksp(MnCO3)=2.4×10—11、离子浓度为1.0×10-5mol/L时即完全沉淀,步骤Ⅲ中Mn2+完全沉淀时c(CO32—)= ________________。
(3)步骤IV加热“蒸氨”时发生反应的化学方程式为________________。
(4)步骤VI反应的离子方程式为______________,其中盐酸需过量,其原因是________________。
(5)步骤Ⅶ获得CuCl晶体需经过滤、洗涤、干燥。洗涤时,常有无水乙醇代替蒸馏水做洗涤剂的优点是______________(写一点)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是利用无土栽培法培养蔬菜时,培养液中元素的配方,其中根细胞吸收最少的是
离子 | K+ | M g2+ | Ca2+ | NO3- | H2PO4- | SO42- | Zn2+ |
培养液浓度(mol/L) | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
A. H2PO4-B. SO42-C. Ca2+D. Zn 2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苏轼的《格物粗谈》中记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指( )
A.甲烷B.新戊烷C.乙烯D.苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是生物必须的营养元素之一,含硫化合物在自然界中广泛存在,循环关系如下图所示:
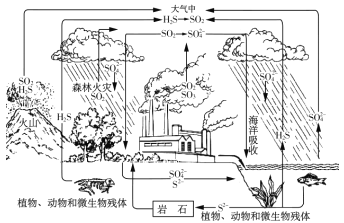
(1)自然界地表层原生铜的硫化物经氧化、淋滤作用后变成 CuSO4溶液,向地下深层渗透遇到难溶的ZnS,慢慢转变为铜蓝( CuS), 请用化学用语表示 ZnS 转变为 CuS 的过程 __________。
(2) 火山喷发产生 H2S 在大气当中发生如下反应:
①2H2S(g)+O2(g) =2S(g) +2H2O(g) △H=﹣442.38kJ/mol
②S(g)+O2(g)=SO2(g) △ H=﹣297.04kJ/mol。
H2S(g)与 O2(g)反应产生 SO2(g)和 H2O(g)的热化学方程式是__________。
(3) 降低 SO2的排放量已经写入 2018 年政府工作报告, 化石燃料燃烧时会产生含 SO2的废气进入大气,污染环境,有多种方法可用于 SO2的脱除。
①NaClO 碱性溶液吸收法。工业上可用 NaClO 碱性溶液吸收 SO2。
i.反应离子方程式是__________。
为了提高吸收效率,常用 Ni2O3作为催化剂。在反应过程中产生的四价镍和原子氧具有极强的氧化能力,可加快对 SO2的吸收。该催化过程的示意图如下图所示:
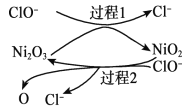
ii.过程 1 的离子方程式是__________。
iii.Ca(ClO)2也可用于脱硫,且脱硫效果比 NaClO 更好,原因是__________。
②电化学脱硫法。某种电化学脱硫法装置如下图所示,不仅可脱除烟气中的SO2还可以制得 H2SO4。
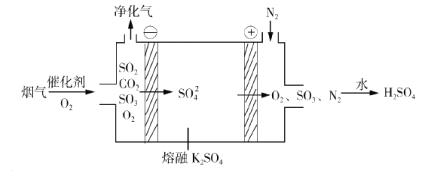
i.在阴极放电的物质是______。
ii.在阳极生成 SO3的电极反应式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】电化学还原技术是一种处置CO2的绿色环保、有发展潜力的方法。铜、铂、铟(In)等金属都是该反应的催化剂。
(1)In元素基态原子的价电子排布式为____________。与Cu元素同周期,且基态原子有2个未成对电子的过渡元素是_________________(填元素符号)。
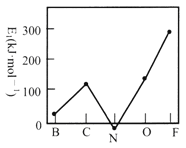
(2)第一电子亲和能(E1)是元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量。第二周期部分元素的E1变化趋势如图所示。试分析碳元素的E1较大的原因_____________________________。
(3)[PtC14(NH3)2]中N原子的杂化方式为________,所含化学键类型包括_______(填字母)。
a.离子键b.共价键c.金属键d.配位键e.氢键
[PtCl4(NH3)2]中H-N-H键之间夹角______(填“>”“<”或“=”)NH3分子中H-N-H键之间夹角,原因是__________________________________。
(4)C60晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体,如图为K3C60的面心立方晶胞。则K+占据的是C60围成的正四面体空隙和_____空隙,若C60分子的原子坐标参数分别为A(0,0,0),B(![]() ),C(1,1,1)等,则距离A位置C60分子最近的K+的原子坐标参数为_____________。判断晶体熔沸点高低:C60_________K3C60(填“>”“<”或“=”)。
),C(1,1,1)等,则距离A位置C60分子最近的K+的原子坐标参数为_____________。判断晶体熔沸点高低:C60_________K3C60(填“>”“<”或“=”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com