
两份等体积等浓度的NaOH溶液,分别与体积相等的![]() 、
、![]() 溶液混合,充分反应后
溶液混合,充分反应后![]() 、
、![]() 均恰好形成沉淀,则原
均恰好形成沉淀,则原![]() 、
、![]() 溶液中
溶液中![]() 浓度之比是( )
浓度之比是( )
A.1∶1
B.1∶2
C.2∶3
D.3∶2
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L(标准状况) |
| 1 | 7.24 | 50.00 | 1.792 |
| 2 | 14.48 | 50.00 | 3.584 |
| 3 | 21.72 | 50.00 | 4.032 |
| 4 | 36.20 | 50.00 | 2.240 |
查看答案和解析>>
科目:高中化学 来源: 题型:
方法一:将尾气通入氨水,再向吸收液中加入浓硫酸,以制取高浓度的SO2及(NH4)2SO4和NH4HSO4固体。已知SO2及(NH4)2SO4和NH4HSO4的分解温度均高于200 ℃,欲测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液50.00 mL,加热至120 ℃左右,使氨气全部逸出,测得有关实验数据如下:
实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L(标准状况) |
① | 7.24 | 50.00 | 1.792 |
② | 14.48 | 50.00 | 3.584 |
③ | 21.72 | 50.00 | 4.032 |
④ | 28.96 | 50.00 | 3.136 |
(1)若取3.62 g样品用同样方法实验时,生成氨气的体积(标准状况)为_________L。
(2)该混合物中(NH4)2SO4和NH4HSO4的物质的量之比为_________。
(3)求所用NaOH溶液的物质的量浓度_________。
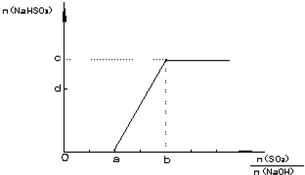
方法二:用NaOH溶液、石灰及O2吸收尾气,以制取石膏(CaSO4·2H2O),此过程的中间产物是NaHSO3。实际操作中以调节尾气排放的流量来取得SO2与NaOH间物质的量的最佳比值,从而提高亚硫酸氢钠的产量。试写出n(SO2)/n(NaOH)在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)的关系式,填入下表:
n(SO2)/n(NaOH) | n(NaHSO3) |
|
|
|
|
|
|
查看答案和解析>>
科目:高中化学 来源:2013届湖南省高二上学期期中考试化学(理)试卷 题型:填空题
 当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是
。
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是
。
⑷在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀。制备CuCl的离子方程式是 。
28. (9分)下列一句话中叙述了两个值,前者记为M,后者记为N,M和N的关系从A、B、C、D中选择
A. M>N B. M<N C. M=N D. 无法比较
⑴相同温度下,1L 1mol/L 的NH4Cl溶液中的NH4+个数和2 L 0.5mol·L-1NH4Cl溶液中NH4+的个数: ;
⑵相同温度下,pH值为12的烧碱溶液中水的电离度和pH值为12的CH3COONa溶液中水的电离度: ;
⑶两份室温时的饱和石灰水,一份升温到50℃;另一份加入少量CaO,恢复至室温,两溶液中的c(Ca2+): ;
⑷常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中c(HCO3-): ;
⑸将pH值为2的醋酸和盐酸都稀释相同倍数所得稀溶液的pH值: ;
⑹常温下0.1mol/L的CH3COOH与0.1mol/LCH3COONa等体积混合后溶液中c(Na+)和c(CH3COO-): ;
⑺同温度下,0.1mol/LFeCl3溶液中Fe3+水解百分率与0.01mol·L-1FeCl3溶液中Fe3+ 的水解百分率: ;
⑻室温下某强酸和某强碱溶液等体积混合后,溶液的pH值为7,原酸溶液和原碱溶液的物质的量浓度: ;
⑼PH值相同的醋酸和盐酸,分别用蒸馏水稀释至原来的M倍和N倍,稀释后两溶液的PH值仍然相同, 则M和N的关系是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 。
⑷在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀。制备CuCl的离子方程式是 。
28. (9分)下列一句话中叙述了两个值,前者记为M,后者记为N,M和N的关系从A、B、C、D中选择
A. M>N B.M<N C.M=N D. 无法比较
⑴相同温度下,1L 1mol/L 的NH4Cl溶液中的NH4+个数和2 L 0.5mol·L-1NH4Cl溶液中NH4+的个数: ;
⑵相同温度下,pH值为12的烧碱溶液中水的电离度和pH值为12的CH3COONa溶液中水的电离度: ;
⑶两份室温时的饱和石灰水,一份升温到50℃;另一份加入少量CaO,恢复至室温,两溶液中的c(Ca2+): ;
⑷常温下两份等浓度的纯碱溶液,将第二份升高温度,两溶液中c(HCO3-): ;
⑸将pH值为2的醋酸和盐酸都稀释相同倍数所得稀溶液的pH值: ;
⑹常温下0.1mol/L的CH3COOH与0.1mol/LCH3COONa等体积混合后溶液中c(Na+)和c(CH3COO-): ;
⑺同温度下,0.1mol/LFeCl3溶液中Fe3+水解百分率与0.01mol·L-1FeCl3溶液中Fe3+ 的水解百分率: ;
⑻室温下某强酸和某强碱溶液等体积混合后,溶液的pH值为7,原酸溶液和原碱溶液的物质的量浓度: ;
⑼PH值相同的醋酸和盐酸,分别用蒸馏水稀释至原来的M倍和N倍,稀释后两溶液的PH值仍然相同, 则M和N的关系是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com