
在Fe(NO3)2溶液中存在下列平衡:Fe2++2H2O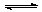 Fe(OH)2+2H+,现向上述溶液中加入稀硫酸,产生的现象是
Fe(OH)2+2H+,现向上述溶液中加入稀硫酸,产生的现象是
A.溶液的颜色变得更绿 B.溶液中出现白色沉淀
C.溶液颜色由绿变黄 D.上述现象均不可能出现
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在标准状况下,1体积水溶解336体积氯化氢,所得溶液密度为1.1g/cm3,溶液中气体的物质的量浓度和溶质的质量分数分别为( )
A.10.7mol/L 35.4% B.14.8 mol/L 28.8%
C.14.8 mol/L 35.4% D.10.7mol/L 28.8%
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列化学反应的离子方程式是 ( )
A. 过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
B. 硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓
C. NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O
D. 向碳酸氢钠溶液中滴加少量稀硝酸:CO32 - + 2H + = CO2 + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
开发新型储氢材料是氢能利用的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Ti3+的未成对电子数有______个。
②LiBH4由Li+和BH4-构成,BH4 -呈正四面体构型。LiBH4中不存在的作用力有______(填标号)。
A.离子键 B.共价键 C.金属键 D.配位键
③Li、B、H元素的电负性由大到小排列顺序为______。
(2) 金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+______H-(填“>”、“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:

M是______(填元素符号)。
某种新型储氧材料的理论结构模型如下图所示,图中虚线框内碳原子的杂化轨道类型有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A. 第VIA族元素从上到下,其氢化物的稳定性逐渐减弱
B. L层电子数为奇数的所有元素都是非金属元素
C. VIIA族元素阴离子的还原性越强,元素的最高价氧化物对应水化物的酸性也越强
D. 同一主族的甲乙两种元素,甲的原子序数为a,则乙的原子序数可能为:a+4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作不能达到目的的是
| 选项 | 目的 | 操作 |
| A. | 配制100 mL 1.0 mol·L-1 CuSO4溶液 | 将25 g CuSO4·5H2O溶于100 mL蒸馏水中 |
| B. | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 |
| C. | 在溶液中将 | 向酸性KMnO4溶液中滴加H2O2溶液至紫色消失 |
| D. | 确定NaCl溶液中是否混有Na2CO3 | 取少量溶液滴加CaCl2溶液,观察是否出现白色浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
(1)已知相关物质之间存在如下变化:
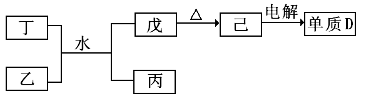
①丁与乙和水反应生成戊和丙的离子方程式为__________________,由物质己电解得到单质D 的化学方程式为_________________________;
②请同学们写出丙的溶液中阳离子的检验方法:____________________________________________________________________。
(2)已知E 及其化合物有以下变化:
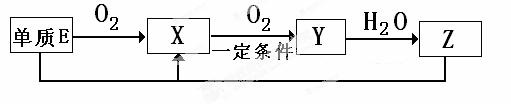
写出单质E 与化合物Z在一定条件下反应生成X和水的化学方程式________;
由A、B、C、D、E 5种元素中的两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为________________(任写一个即可)。
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2 L的该无色气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的C的含氧酸盐的化学式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
选择萃取剂将碘水中的碘萃取出,这中萃取剂应具备的性质是
A.不溶于水,且必须易与碘发生化学反应 B.不溶于水,且比水更容易使碘溶解
C.不溶于水,且必须比水密度大 D.不溶于水,且必须比水密度小
查看答案和解析>>
科目:高中化学 来源: 题型:
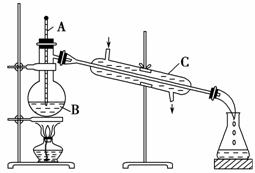 工业上通常用工业酒精和生
工业上通常用工业酒精和生 石灰混合蒸馏法制取无水乙醇。如图是实验室中模拟工业原理制取无水乙醇的装置。
石灰混合蒸馏法制取无水乙醇。如图是实验室中模拟工业原理制取无水乙醇的装置。
回答下列问题:
(1)指出图中的三处错误: 、
、 。
(2)在除去工业酒精中的水时,下列做法不可取的是 。
A.加入过量的生石灰后过滤
B.加入过量的生石灰后蒸馏
C.加入过量的生石灰后分液
(3)由(2)可知除去工业酒精中的水的原理是(用化学方程式表示) 。
(4)装置中仪器A、B、C的名称分别是A ;B ;C 。
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片)的作用是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com