
【题目】已知草酸为二元中强酸,具有较强还原性,且![]() ,下列说法正确的是
,下列说法正确的是![]()
A.草酸与氢氧化钠溶液混合呈中性时,溶液中存在:![]()
B.![]() 与NaClO溶液混合,反应的离子方程式为:
与NaClO溶液混合,反应的离子方程式为:![]()
C.![]() 溶液中:
溶液中:![]()
![]()
![]()
![]()
D.草酸使酸性![]() 溶液褪色,离子方程式为:
溶液褪色,离子方程式为:![]()
【答案】D
【解析】
A.溶液中的阴离子有HC2O4—、C2O42—、OH—,由电荷守恒知c(H+)+c(Na+)=c(HC2O4—)+2c(C2O42—)+c(OH—),由于溶液呈中性,所以c(H+)= c(OH—),c(Na+)=c(HC2O4—)+2c(C2O42—),故A错误;
B.NaHC2O4与NaClO溶液混合,草酸具有较强还原性,ClO—有强氧化性,发生氧化还原反应反应:HC2O4—+ClO—=HCO3—+CO2↑+Cl—,故B错误;
C. NH4+也会水解,依据原子守恒可知:c(NH3H2O)+c(NH4+)=2c(H2C2O4)+2 c(HC2O4—)+2 c(C2O42—),故C错误;
D.草酸有较强还原性,使酸性KMnO4溶液褪色,离子方程式为:5H2C2O4+2MnO4—+6H+=2Mn2++10CO2↑+8H2O,故D正确;
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】根据题目要求,回答下列问题:
(1)下列现象和应用与电子跃迁无关的是___。
A.激光 B.焰色反应 C.燃烧放热 D.原子光谱
(2)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用__形象化描述。
(3)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)__I1(Cu)(填“大于”或“小于”)。原因是__。
(4)ZnF2具有较高的熔点(872℃),其化学键类型是___;
(5)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为___,![]() 原子的杂化形式为__。
原子的杂化形式为__。
(6)与H2O分子互为等电子体的阴离子为__。
(7)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为__。
(8)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313kJ/mol,F—F键的键能为159kJ/mol,Cl—Cl键的键能为242kJ/mol,则ClF3中Cl—F键的平均键能为__kJ/mol。ClF3的熔、沸点比BrF3的__(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是

A. 图甲表示反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
B. 图乙表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,乙的压强比甲的压强大
3C(g)+D(g)的影响,乙的压强比甲的压强大
C. 图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
D. 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沙罗特美是一种长效平喘药,其合成的部分路线如下:
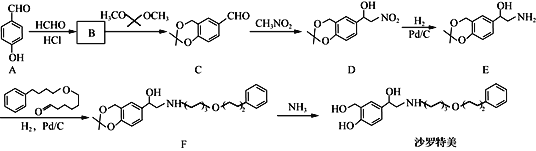
(1)F中的含氧官能团名称为____________。
(2)A的名称为____________。
(3)D→E的反应类型为____________,沙罗特美的分子式为____________。
(4)B的分子式为C8H8O3,与(CH3)2C(OCH3)2发生取代反应得到物质C和CH3OH,写出B的结构简式:____________________。
(5)判断同时满足下列条件的C的同分异构体的数目:_______。(不考虑立体异构)
①分子中含有![]() 结构且只有一个环状结构,与FeCl3发生显色反应;
结构且只有一个环状结构,与FeCl3发生显色反应;
②能与NaHCO3发生反应放出CO2。
③苯环上有且只有三个取代基
(6)请写出以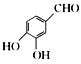 、(CH3)2C(OCH3)2、CH3NO2为原料制备
、(CH3)2C(OCH3)2、CH3NO2为原料制备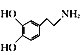 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。_____________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖酸亚铁((C6H11O7)2Fe)是常用的补铁剂,易溶于水,几乎不溶于乙醇。用下图装置制备FeCO3,并利用FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:
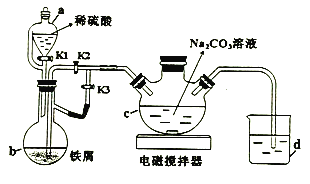
(1)a的名称为_________。
(2)打开a中K1、K3,关闭K2,一段时间后,关闭K3,打开K2。在_________(填仪器标号)中制得碳酸亚铁。实验过程中产生的H2作用有_________、____________。(写2条)
(3)将制得的碳酸亚铁浊液过滤、洗涤。如过滤时间过长会发现产品部分变为红褐色。用化学方程式说明原因____________。
(4)将葡萄糖酸与碳酸亚铁混合,加入乙醇、过滤、洗涤、干燥。加入乙醇的目的是_________________。
(5)用 NaHCO3溶液代替Na2CO3溶液制备碳酸亚铁,同时有气体产生,离子方程式为______________,此法产品纯度更高,原因是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是( )
A.![]() 和
和![]() 不属于同分异构体
不属于同分异构体
B.质量相同的![]() 和
和![]() 完全燃烧时消耗氧气的质量较少的是
完全燃烧时消耗氧气的质量较少的是![]()
C.连接四个不同基团的碳原子为“手性碳原子”,![]() 含有两个手性碳原子
含有两个手性碳原子
D.标准状况下![]() L溴乙烷所含化学键总数为
L溴乙烷所含化学键总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或描述中,正确的是
A.离子结构示意图  既可以表示35Cl-,也可以表示37Cl-
既可以表示35Cl-,也可以表示37Cl-
B.SO3的水溶液能导电,说明SO3是电解质
C.NaHSO3在水中的电离方程式:NaHSO3=Na++H++SO32-
D.同素异形体间的转化和同位素间的转化都是化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电絮凝的反应原理是以铝、铁等金属为阳极,在直流电的作用下,阳极被溶蚀,产生金属离子,在经一系列水解、聚合及氧化过程,发展成为各种羟基络合物、多核羟基络合物以及氢氧化物,使废水中的胶态杂质、悬浮杂质凝聚沉淀而分离。下列说法不正确的是

A.每产生1molO2,整个电解池中理论上转移电子数为4NA
B.阴极电极反应式为2H2O + 2e- = H2↑+2OH—
C.若铁为阳极,则阳极电极方程式为Fe-2e-=Fe2+和2H2O - 4e- = O2↑+4H+
D.若铁为阳极,则在处理废水的过程中阳极附近会发生:4Fe2++O2+4H+=4Fe3++2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com