
【题目】回答下列问题:
(1)已知铜是29号元素,写出Cu的价层电子排布式________,在元素周期表中的位置______,该元素在________(填“s”“p”“d”“f”或“ds”)区。
(2)写出与N同主族的As的基态原子的价电子排布图:______________。从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为________。
(3)写出Fe2+的核外电子排布式:________。
(4) 下列三种晶体:①CO2,②NaCl,③金刚石,它们的熔点从低到高的顺序____(填序号)。
【答案】(1)3d104s1 第四周期第ⅠB族 ds区
(2)![]() N>O>B
N>O>B
(3)1S22S22P63S23P63d6或者[Ar]3d6 (4)①<②<③
【解析】试题分析:(1)Cu原子核外有29个电子,其基态原子的电子排布式为[Ar]3d104s1,价电子排布式为3d104s1,位于元素周期表的第四周期第IB族,该元素在ds区;
(2)As原子序数为33,最外层有5个电子,根据构造原理知,其价电子的电子排布式为4s24p3,则核外价电子排布图为:![]() ;同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素的第一电离能大于其相邻元素,所以三种元素的第一电离能由大到小的顺序为N>O>B;
;同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素的第一电离能大于其相邻元素,所以三种元素的第一电离能由大到小的顺序为N>O>B;
(3)Fe的原子核外电子数为26,原子核外电子排布式为1s22s22p6 3s23p63d6 4s2,失去2个电子生成Fe2+,则Fe2+的核外电子排布式为1S22S22P63S23P63d6或者[Ar]3d6;
(4)①CO2为分子晶体,②NaCl是离子晶体,③金刚石为原子晶体,它们的熔点从低到高的顺序①<②<③。


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
【题目】为确定某溶液由以下离子Na+、Mg2+、Ba2+、SO42﹣、I﹣、CO32﹣中的哪几种微粒组成.进行以下实验,分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象.为确定该溶液的组成,还需检验的离子是( )
A.Na+ B.SO42﹣ C.Ba2+ D.Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种重要的有机化工原料有机物X,下面是以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。Y是一种功能高分子材料。

已知:(1)X为芳香烃,其相对分子质量为92
(2)烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:![]()
(3)![]() (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为______________。
(2) 中官能团的名称为____________________;
中官能团的名称为____________________;
(3)反应③的反应类型是___________;已知A为一氯代物,则E的结构简式是____________;
(4)反应④的化学方程式为_______________________;
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有________种:①含有苯环;②既不能发生水解反应,也不能发生银镜反应;③1mol该有机物能与2molNaHCO3完全反应。
(6)请写出以A为原料制备![]() 的合成路线流程图 (无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图 (无机试剂任用)。合成路线流程图示例如下:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s) = CuSO4(s)+5H2O(l) △H=+Q2 kJ·mol1则Q1、Q2的关系为
A.Q1<Q2 B.Q1>Q2 C.Q1=Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分) 东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_ _,提供孤电子对的成键原子是__ ___。
③氨的沸点_____(“高于”或“低于”)膦(PH3),原因是____ ;氨是____ _分子(填“极性”或“非极性”),中心原子的轨道杂化类型为____。
(3)单质铜及镍都是由______键形成的晶体:元素同与镍的第二电离能分别为:I(Cu)=1959kJ/mol,I(Ni)=1753kJ/mol,I(Cu)>I(Ni)的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
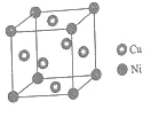
晶胞中铜原子与镍原子的数量比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z在周期表中的相对位置如图所示。已知Y元素原子的外围电子排布为ns(n-1)np(n+1),则下列说法不正确的是( )
![]()
A. Y元素原子的外围电子排布为4s24p4
B. Y元素在周期表的第三周期ⅥA族
C. X元素所在周期中所含非金属元素最多
D. Z元素原子的核外电子排布式为1s22s22p63s23p63d104s24p3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭.导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca =CaCl2+Li2SO4+Pb。

下列有关说法正确的是
A .正极反应式:Ca+2Cl- - 2e- =CaCl2
B.放电过程中,Li+向负极移动
C.常温时,在正负极间接上电流表或检流计,指针不偏转
D.每转移0.1mol电子,理论上生成20.7g Pb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,美国正在研究用锌电池取代目前广泛使用的蓄电池,它具有容量大、污染小的特点,其电池反应为:2Zn+O2=2ZnO ,其原料为锌、空气和电解质溶液,则下列叙述正确的是
A.锌为正极,空气在负极反应
B.负极还原反应,正极氧化反应
C.负极的电极反应为:Zn-2e-+2OH-=ZnO+H2O
D.电池工作时溶液的pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是地壳中含量最高的金属元素,其单质及化合物在生产生活中有广泛的应用。
(1)普通水泥的主要成分之一是铝酸三钙(3CaO·Al2O3),3CaO·Al2O3中Al的化合价为__________;
(2)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉(Al2O3)与炭粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式__________;
(3)现将一定量的铝粉和镁粉的混合物与100mL稀硝酸充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐渐加入4mol·L-1的NaOH溶液,加入NaOH溶液的体积(mL)与产生沉淀的质量的关系如图所示。
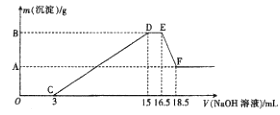
①D→E过程中反应的离子方程式为____________________;
②A点对应纵坐标的数值是__________,原稀硝酸的浓度是__________mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com