
| V |
| Vm |
| n |
| V |
| 6.72L |
| 22.4L?mol -1 |
| 0.3mol×2 |
| 1 |
| 0.3mol×1 |
| 1 |
| 0.6mol |
| 0.5L |


 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
| A、对垃圾进行分类要严格执行国际统一的标准 |
| B、对垃圾进行分类的主要目的是便于垃圾的存放 |
| C、凡是废纸都可以归为纸类垃圾进行回收 |
| D、学生在课堂上用过的废纸可以积攒起来进行回收利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CuCl2溶液 |
| B、FeCl3溶液 |
| C、饱和Ca(OH)2溶液 |
| D、NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
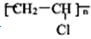 )就是以乙炔为原材料制得的.写出以乙炔和HCl为原料制聚氯乙烯的化学方程式.
)就是以乙炔为原材料制得的.写出以乙炔和HCl为原料制聚氯乙烯的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
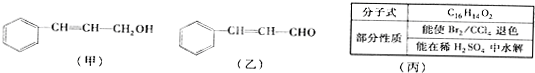
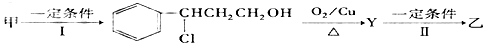
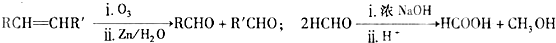
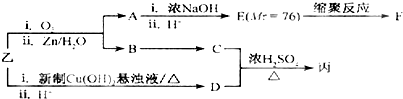
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com