
【题目】科学家研究发现纳米TiO2的混凝土可以适度消除汽车尾气中的氮氧化物,其原理如下。下列关于“消除”过程的叙述错误的是( )
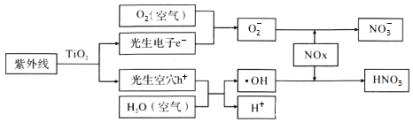
A.纳米TiO2作催化剂,NOx消除效率更高
B.NOx消除总反应为:4NOx+(5-2x)O2+2H2O![]() 4HNO3
4HNO3
C.1mol羟基(-OH)比1molO2少8NA个电子(NA为阿伏加德罗常数)
D.纳米TiO2属于胶体,能产生丁达尔现象
【答案】CD
【解析】
含TiO2的混凝土或沥青可以部分消除汽车尾气中的氮氧化物,在TiO2催化作用下,紫外线提供能量、发生反应4NOx+(5-2x)O2+2H2O![]() 4HNO3,纳米TiO2与紫外线接触面积更大,反应更充分,反应速率更快,由此分析解答。
4HNO3,纳米TiO2与紫外线接触面积更大,反应更充分,反应速率更快,由此分析解答。
A.纳米TiO2作催化剂时,与紫外线接触面积更大,反应更充分,反应速率更快,NOx消除效率更高,故A正确;
B.分析过程可知消除总变化为:4NOx+(5-2x)O2+2H2O![]() 4HNO3,故B正确;
4HNO3,故B正确;
C.1mol O2的电子的物质的量为:16mol,而1mol羟基电子的物质的量为9mol,所以1mol羟基(-OH)比1molO2少7NA个电子,故C错误;
D.纳米TiO2不属于胶体,属于纯净物,胶体是一种混合物,指的是分散质粒子直径在1nm-100nm之间的分散系,故不能产生丁达尔现象,故D错误;
答案选CD。


科目:高中化学 来源: 题型:
【题目】CO2 的资源化利用能有效减少 CO2 排放,充分利用碳资源。
⑴在海洋碳循环中,通过如图所示的途径固碳。
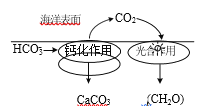
①写出钙化作用的离子方程式_____。
②同位素示踪法证实光合作用释放出的O2 只来自于H2O。用18O标记物质的光合作用的化学方程式如下,将其补充完整:
______________+________________![]()
⑵电解法转化 CO2 可实现 CO2 资源化利用。电解 CO2 制 HCOOK 的原理示意图如下。
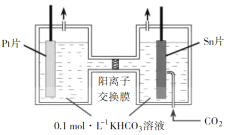
①阴极的电极反应式为_____。
②电解一段时间后,阳极区KHCO3 浓度下降,原因是______________________________________。
⑶CO2 催化加氢合成二甲醚是一种 CO2 转化方法,其过程中主要发生下列反应:
反应Ⅰ:CO2(g) + H2(g) === CO(g) + H2O(g) ΔH = +41.2 kJ·mol1
反应Ⅱ:2CO2(g) + 6H2(g) === CH3OCH3(g) + 3H2O(g) ΔH = 122.5 kJ·mol1
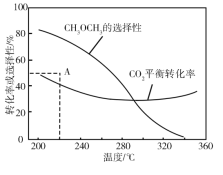
在恒压、CO2 和H2 的起始量一定的条件下,CO2 平衡转化率和平衡时 CH3OCH3 的选择性随温度的变化如图。
CH3OCH3 的选择性 =2CH3OCH3的物质的量反应的CO2的物质的量×100%
①温度高于300 ℃时,CO2 平衡转化率随温度升高而上升的原因是____________。
②220℃时,在催化剂作用下 CO2 与H2 反应一段时间后,测得 CH3OCH3 的选择性为48%(图中 A 点)。反应时间和温度不变,提高 CH3OCH3 选择性的措施有_________________。
A.增大压强 B. 使用对反应Ⅱ催化活性更高的催化剂 C. 及时移走产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL混合液中,HNO3和H2SO4的物质的量浓度分别为0.4mol/L和0.1mol/L。向该混合液中加入1.92g铜粉,加热使反应发生完全。下列说法正确的是(忽略反应前后溶液体积变化)( )
A.所得溶液中c(Cu2+)=0.225mol/L B.所得溶液中c(Cu2+)=0.03mol/L
C.所得气体在标准状况下的体积为0.448L D.反应中转移0.06mol的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生兴趣小组模拟工业制取无水Na2SO3的过程如下:
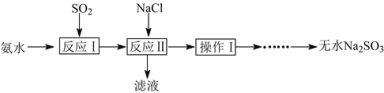
已知:①反应Ⅰ在三颈烧瓶中发生,装置如图1所示(固定及加热类仪器省略);
②H2SO3、HSO3-、SO32-在水溶液中的物质的量分数随pH的分布如图2;
③Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。
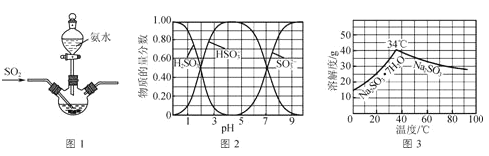
(1)为提高Na2SO3产率,反应Ⅰ应控制pH在____左右。
(2)反应Ⅱ所得滤液的主要成分是____和Na2SO3。
(3)将操作Ⅰ后所得的Na2SO3溶液加热浓缩、____(填操作),过滤出的固体用无水乙醇洗涤、在真空干燥箱中采用150℃干燥,得无水Na2SO3固体。
(4)可以用KIO3测定产品中无水Na2SO3的纯度:称取0.1260 g样品于锥形瓶中,用蒸馏水溶解,并加入淀粉做指示剂,滴加酸性KIO3溶液(amol·L-1)至Na2SO3恰好完全氧化成Na2SO4,发生反应3Na2SO3 +KIO3=3Na2SO4+KI,消耗KIO3溶液体积为bmL。通过计算确定样品中Na2SO3的质量分数____。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A对氢气的相对密度为30,分子中含碳40%,含氢6.6%,其余为氧。
(1)通过计算确定该有机物的分子式;____
(2)按中学常见官能团,写出其可能的结构简式。____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉和油脂为原料,制备生活中的某些物质。
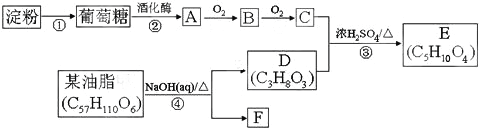
请回答:
(1)D中含有官能团的名称是____。
(2)反应④的有机反应类型是____。
(3)写出E可能的结构简式____。
(4)下列说法不正确的是____。
A.1molD最多可以和3mol金属Na反应,生成标准状况下336L氢气
B.葡萄糖、B以及淀粉这三者均能发生银镜反应
C.反应①和反应②的反应类型相同
D.A和D有相同的官能团,两者属于同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据不完全统计,全世界每年约有10%~20%的农副产品,水产品会因腐败变质而无法食用,经济损失巨大,所以研究安全无害的食品防腐剂很重要,山梨酸及其盐,尼泊金酯等可作为食品防腐剂,其结构简式如图:
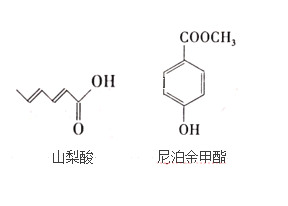
按要求回答下列问题:
(1)写出山梨酸中含氧官能团的名称__。
(2)尼泊金甲酯的1H核磁共振谱图中有____个峰。
(3)写出山梨酸与NaOH溶液反应的化学方程式____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应X2+3Y2![]() 2Z2在反应过程中,反应速率(v)与时间(t)的关系曲线如图所示,下列叙述正确的是
2Z2在反应过程中,反应速率(v)与时间(t)的关系曲线如图所示,下列叙述正确的是
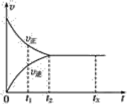
A.t1时,只有正方向反应
B.t2时,反应未达到限度
C.t2~t3,正、逆反应速率相等
D.t2~t3,各物质的浓度相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com