
| 选项 | A | B | C | D |
| 实验 方案 |  | 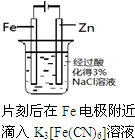 |  | 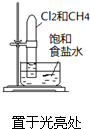 |
| 实验 目的 | 验证铁钉发生了 析氢腐蚀 | 验证Fe电极被保护 | 验证乙烯的产生 | 验证甲烷与氯气发生了化学反应 |
| A、A | B、B | C、C | D、D |


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
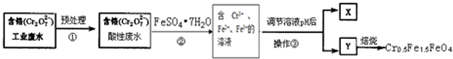
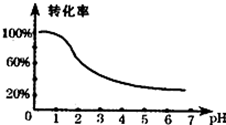
查看答案和解析>>
科目:高中化学 来源: 题型:
A、异戊二烯(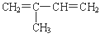 )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 |
| B、CH3CH2CH2Cl在碱性溶液中水解 |
| C、甲苯在一定条件下发生硝化生成一硝基甲苯的反应 |
| D、2-氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、原子半径:Z>Y>X |
| B、R元素的含氧酸和W元素的含氧酸,酸性一定前者强 |
| C、X和Z形成的化合物能溶于NaOH溶液 |
| D、Y和W形成的化合物中,阴阳离子的个数可能比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、次氯酸钠溶液中通入过量二氧化硫ClO-+H2O+SO2→HClO+HSO3- |
| B、向碳酸氢钠溶液中加入过量氢氧化钙溶液2HCO3-+Ca2++2OH-→CaCO3↓+2H2O+CO32- |
| C、氢氧化钡溶液与硫酸溶液反应得到中性溶液Ba2++OH-+H++SO42-→BaSO4↓+H2O |
| D、50 mL 1mol/L的NaOH溶液中通入0.03mol H2S:5OH-+3H2S→HS-+2S2-+5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L的Na2A溶液中:c(A2-)+c(HA-)+c(H2A)=0.1mol/L |
| B、常温下,将pH=3的H2A溶液稀释到原来的100倍,则稀释后溶液的pH<5 |
| C、常温下,将pH=3的H2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性 |
| D、常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na+)-c(HA-)-c(A2-)=10-5-10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol的K+ |
| B、0.5 mol的H+ |
| C、1.0 mol的H+ |
| D、1.0 mol的OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
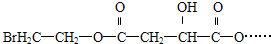
 )的原料,试写出其结构简式
)的原料,试写出其结构简式查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com