
在实验室里将浑浊的自来水制成蒸馏水,最好的方法是( )
|
| A. | 过滤 | B. | 萃取 | C. | 蒸发 | D. | 先过滤后蒸馏 |
科目:高中化学 来源: 题型:
已知HI为无色气体,在一定条件下,对于可逆反应H2(g)+I2(g) 2HI(g),下列叙述中能表明该反应已达到化学平衡状态的是( )
2HI(g),下列叙述中能表明该反应已达到化学平衡状态的是( )
A.HI的生成速率与H2的生成速率相等 B.H2的生成速率与I2的生成速率相等
C.混合物的颜色不再发生变化 D.H2、I2、HI的分子数之比为1∶1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
燃烧热是指一定条件下1 mol可燃物完全燃烧生成稳定的氧化物时放出的热量。已知热化学方程式:①CO(g)+1/2 O2(g)====CO2(g)ΔH = -283.0 kJ·mol-1
②H2(g)+ 1/2O2(g)====H2O(g)ΔH = -241.8 kJ·mol-1
则下列说法正确的是( )
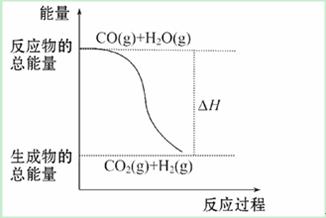
A. 由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)==== CO2(g)+H2(g)ΔH = -41.2 kJ·mol-1
B. H2的燃烧热为241.8 kJ·mol-1
C.H2(g)转变成H2O(g)的化学反应一定要释放能量
D.根据②推知反应H2(g)+1/2O2(g)==== H2O(l)ΔH > -241.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液c ;
A、B是两块电极板,通过导线与直流电相连。请回答以下问题:
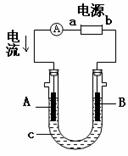 (1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
(1)若A、B都是惰性电极,c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞试液,则:
① B是 极(填“阴”或“阳”), B极逸出
(填:黄绿或无色)气体,同时B极附近溶液呈 色。
② 电解池中A极上的电极反应式为 。
B极上的电极反应式为 。
(2)如要进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,电解液c选用CuSO4溶液,则:
① A电极的材料是 ,电极反应式是 。
② B电极的材料是 ,电极反应式是 。
(说明:杂质发生的电极反应不必写出)
③下列说法正确的是________。
a.电能全部转化为化学能
b.在电解精炼过程中,电解液中伴随有Al3+、Zn2+产生
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(3)用惰性电极电解CuSO4溶液。若阴极析出Cu的质量为12.8 g ,则阳极上产生的气体在标准状况下的体积为 L 。
(4)利用反应2Cu+O2+2H2SO4===2CuSO4+2H2O可制备CuSO4,若将该反应设计为电解池,其电解质溶液需用 ,阳极材料是用 ,阴极电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求完成下列填空:
(1)已知在标准状况下的四种气体 ①8.96L CH4 ②3.01×1022个HCl分子 ③10.2克H2S ④0.5molNH3用相应的序号填写下列空白:体积最大的是 ④ ;含氢原子数最多的是 .
(2)等物质的量的氧气与臭氧质量之比为 2:3 ,分子个数之比为 1:1 ,电子个数之比为 .
(3)某金属氯化物MCl3 26.7g,含有0.600mol Cl﹣.则金属M的摩尔质量为 27g/mol .
(4)现有10克H218O中,中子数目为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
双酚A作为食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。下列有关双酚A的叙述不正确的是( )
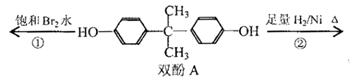
A.双酚A的分子式是C15H16O2
B.双酚A的核磁共振氢谱显示氢原子数之比是1:2:2:3
C.反应①中,1mol双酚A最多消耗2 mol Br2
D.反应②的产物中只有一种官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温恒压下,向密闭容器中充入4mol A和2 mol B,发生如下反应:2A(g)+B(g)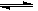 2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是
2C(g) ΔH<0。2min后,反应达到平衡,生成C为1.6mol。则下列分析正确的是
A.若反应开始时容器体积为2L,则v(C)=0.4mol?L-1?min-1
B.若该反应在恒温恒容下进行,放出热量将增加
C.若2min后,向容器中再投入等物质的量A、C,B的转化率不变
D.若在恒压绝热条件下反应,平衡后n(C)<1.6mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com