
【题目】某课外小组对金属钠进行了研究。已知C、D都是单质,F的水溶液是一种常见的强酸。
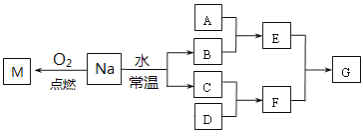
(1)F的名称是:______________
(2)金属Na在空气中放置足够长时间,最终的生成物是:________________
(3)该小组同学应该如何取用金属钠:_________________________________________
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是_________________________。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,请写出该过程的离子方程式:___________________

(6)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如右图所示,由此可知,该溶液中肯定含有的离子及其物质的量浓度之比为__________________________。
(7)将NaHCO3与M的混合物在密闭容器中充分加热后排出气体,经测定,所得固体为纯净物,则NaHCO3与M的质量比为____________。
【答案】氯化氢 Na2CO3 用镊子从试剂瓶中取出一小块金属钠放在表面皿(或玻璃片)上,用滤纸吸干表面的煤油,用小刀切下一小块金属钠备用,剩余的金属钠放回原试剂瓶。 溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失。 4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓ c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3 大于或等于168:78(或84:39)
【解析】
根据转化关系图可知:2Na+O2![]() Na2O2确定M为Na2O2;2Na+2H2O=2NaOH+H2↑,C、D都是单质,F的水溶液是一种常见的强酸,确定B为NaOH,C为H2,D为Cl2,F为HCl。
Na2O2确定M为Na2O2;2Na+2H2O=2NaOH+H2↑,C、D都是单质,F的水溶液是一种常见的强酸,确定B为NaOH,C为H2,D为Cl2,F为HCl。
(1)由上述分析可知,F为氯化氢;
答案:氯化氢。
(2)Na在空气中放置足够长时间,发生4Na+O2=2Na2O、Na2O+H2O=2NaOH、2NaOH+CO2=Na2CO3+H2O、Na2CO3+10H2O=Na2CO310H2O、Na2CO310H2O=Na2CO3+10H2O,则最终生成物为Na2CO3;
答案:Na2CO3。
(3)Na为活泼金属,保存在煤油中,取用方法为用镊子从试剂瓶中取出一小块金属钠放在表面皿(或玻璃片)上,用滤纸吸干表面的煤油,用小刀切下一小块金属钠备用,剩余的金属钠放回原试剂瓶,
答案:用镊子从试剂瓶中取出一小块金属钠放在表面皿(或玻璃片)上,用滤纸吸干表面的煤油,用小刀切下一小块金属钠备用,剩余的金属钠放回原试剂瓶。
(4)若A是一种常见金属单质,能与NaOH反应,则A为Al,E为NaAlO2,G为NaCl,将过量的F(HCl)溶液逐滴加入E(NaAlO2)溶液,边加边振荡,发生NaAlO2+HCl+H2O=NaCl+Al(OH)3↓、Al(OH)3+3HCl=AlCl3+3H2O,所看到的实验现象是溶液中逐渐有白色絮状沉淀生成,且不断增加,然后又由多到少,最后消失;
答案:溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,则A为可溶性亚铁盐,E为Fe(OH)3,则A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E这一过程的离子方程式为4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓。
答案:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓。
(6)A加入氢氧化钠溶液,分析图像可知:第一阶段是H++OH-=H2O,所以溶液呈酸性,不可能存在CO32-;第二阶段金属阳离子与氢氧根离子生成沉淀,第三阶段应该是NH4++OH-=NH3H2O;第四阶段氢氧化物沉淀与氢氧化钠反应最后全溶解,肯定没有Mg2+、Fe3+,必有Al3+。由此确定溶液中存在的离子H+、NH4+、Al3+、SO42-;假设图像中横坐标一个小格代表1molNaOH,则根据前三阶段化学方程式:H++OH-=H2O,Al3++3OH-=Al(OH)3,,NH4++OH-=NH3H2O,可知n(H+)=1mol,n(Al3+)=1mol,n(NH4+)=2mol,
再利用电荷守恒n(SO42-)×2=n(H+)×1+n(Al3+)×3+n(NH4+)×1,得出n(SO42-)=3mol,根据物质的量之比等于物质的量浓度之比得结论;
答案:c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3
(7)将NaHCO3与M(过氧化钠)的混合物在密闭容器中充分加热发生的反应有三个:2NaHCO3![]() Na2CO3+CO2+H2O, 2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2,所得固体为纯净物,说明碳酸氢钠加热分解的二氧化碳必须把过氧化钠反应完,写出总的方程式
Na2CO3+CO2+H2O, 2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2,所得固体为纯净物,说明碳酸氢钠加热分解的二氧化碳必须把过氧化钠反应完,写出总的方程式
4NaHCO3+ 2Na2O2![]() 4Na2CO3+2H2O↑+O2↑
4Na2CO3+2H2O↑+O2↑
84×4g 78×2g
m(NaHCO3):m(Na2O2)=(84×4g):(78×2g)=168:78(或84:39),
碳酸氢钠可以过量,得到的还是纯净物,2NaHCO3![]() Na2CO3+CO2↑+H2O↑,
Na2CO3+CO2↑+H2O↑,
所以m(NaHCO3):m(Na2O2)≥168:78(或84:39);
答案:大于或等于168:78(或84:39)。


科目:高中化学 来源: 题型:
【题目】500 多年前,一艘载着天然苏打晶体(Na2CO3·10H2O)的商船在航行中搁浅,船员们便在附近的沙滩上用几块苏打晶体支锅煮饭。之后他们惊奇地发现,在苏打与沙粒接触的地方出现了许多晶莹发亮的珠子。回答下列问题:
(1)沙滩上沙粒的主要成分为_______(填化学式)。
(2)上述晶莹发亮的珠子可能是______(填字母)。
A. 水晶颗粒 B.无水碳酸钠 C.晶体硅 D.玻璃珠
(3)生成该珠子时发生反应的化学方程式为_____________。
(4)氢氟酸常用作玻璃的蚀刻剂,原因是______________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意完成下列问题:
(1)做实验时皮肤上不小心粘了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸的稀溶液洗涤马上可以复原,其离子方程式为:MnO4- + C2O42- + H+ → CO2↑+ Mn2+ + ![]()
①该反应的氧化剂是_____右边方框内的产物是_____
②完成并配平该离子方程式 __________________电子转移总数是_____ e-
(2)如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。单质A能与某气态单质化合生成化合物B。
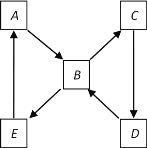
若化合物B是造成酸雨的主要污染物,化合物D是组成单质A元素的最高价氧化物对应水化物,则单质A是_________(物质名称),将化合物B通入溴水中观察到的现象是_________ ,该现象说明化合物B具有_______ 性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到1 mol/L酸中,待合金完全溶解后,再往溶液里加入1 mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液的体积变化的关系如下图所示,下列说法中错误的是( )

A. 盐酸的体积为80mlB. a的取值范围为0≤ a <50
C. n(Mg2+)<0.025molD. 当a值为30时,b值为0.01
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,化学键类型都相同的是( )
A. CaCl2和NaOH B. Na2O和Na2O2 C. CO2和CS2 D. HCl和NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀____________(填操作名称)、洗涤、烘干、称量、计算。洗涤沉淀的具体操作是_____________________________。
方案二:把一定量的样品与足量硫酸反应后,用下图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用_________________。下图装置中实验仪器a的名是_________________。

方案三:利用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如下:
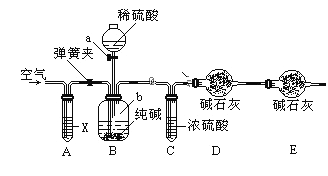
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为33.4g;
③准确称得6g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为35.6g。
(1)若④⑤两步的实验操作太快,则会导致测定结果__________(填“偏大”或“偏小”)。
(2)装置A中试剂X应选用________________________。
(3)E装置的作用是_______________________________。
(4)根据实验中测得的有关数据,计算纯碱样品Na2CO3的质量分数为___________(结果保留小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是
A. Mg在CO2中的燃烧是置换反应
B. 将Mg(OH)2沉淀转化为MgCl2,是镁原子失电子转化为Mg2+
C. 电解得到镁的过程可以写出离子反应方程式,但不是氧化还原反应
D. Mg在CO2中燃烧的反应中,CO2既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中既能与稀H2SO4反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤(NH4)2CO3
A.③④B.①②③④C.①③④D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的核外电子排布式为___________,3d能级上的未成对电子数为_______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是___________,与其为等电子体的分子是___________
②在[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的成键原子是______。
(3)单质铜及镍都是由____键形成的晶体;元素铜与镍的第二电离能分别为:ICu=1 958 kJ·mol–1、INi=1 753 kJ·mol–1,ICu> INi的原因是______________________。
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为____________。
②若合金的密度为d g·cm–3,晶胞参数a=__________nm。
(5)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+ 配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3和NH3键角不同,其中键角较大的是____________,其原因是_______________________。且NF3不易与Cu2+形成配离子,其原因是:_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com