
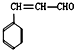
 和化合物Ⅱ
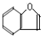
和化合物Ⅱ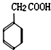 在一定条件下发生反应能生成化合物Ⅲ
在一定条件下发生反应能生成化合物Ⅲ ,请回答以下问题.
,请回答以下问题. 、
、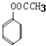 、
、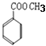 故答案为:
故答案为: 、
、 、
、 (任写2种);
(任写2种); ,
, ;
; ,故答案为:
,故答案为: .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、XY |
| B、X2Y |
| C、XY2 |
| D、XY3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
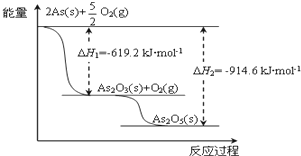 氮是一种非常重要的元素,它的单质和化合物应用广泛,在科学技术和生产中有重要的应用.砷(As)位于周期表中的第4周期,与氮元素属同一主族元素,其广泛分布于自然界.试回答下列问题:
氮是一种非常重要的元素,它的单质和化合物应用广泛,在科学技术和生产中有重要的应用.砷(As)位于周期表中的第4周期,与氮元素属同一主族元素,其广泛分布于自然界.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

 与丁醛缩合得到的含有六元环的高分子化合物,若已知反应:2CH3OH+HCHO→CH3OCH2OCH3+H2O可以发生.请写出制取聚乙烯醇缩丁醛粘合剂的化学方程式:
与丁醛缩合得到的含有六元环的高分子化合物,若已知反应:2CH3OH+HCHO→CH3OCH2OCH3+H2O可以发生.请写出制取聚乙烯醇缩丁醛粘合剂的化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:
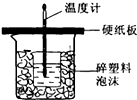 I.已知中和热是指酸跟碱发生中和反应生成lmol H2O时的反应热.
I.已知中和热是指酸跟碱发生中和反应生成lmol H2O时的反应热.| 实验起始温度(℃) | 实验中止温度(℃) | |
| 实验① | 25.00 | 28.64 |
| 实验② | 25.00 | 28.52 |
| 实验③ | 25.00 | 29.66 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4 |
| △ |
| CH3OH |
| 浓H2SO4△ |

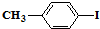 和
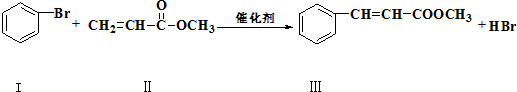
和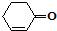 也可以发生类似如图的反应,有机产物的结构简式
也可以发生类似如图的反应,有机产物的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na、Fe分别与不足量的稀硫酸反应所得溶液均呈中性 |
| B、7.8gNa2O2与CO2完全反应,转移0.1 mol电子 |
| C、合金中至少含有两种金属元素 |
| D、NaHCO3、CaCO3、(NH4)2CO3三种固体受热后均能生成气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com