
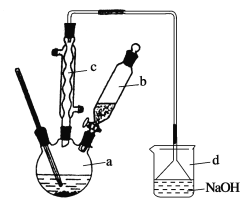
����Ŀ���屽��һ�ֻ���ԭ�ϣ�ʵ���Һϳ��屽��װ��ʾ��ͼ���й��������£�
�� | �� | �屽 | |
�ܶ�/g��cm��3 | 0.88 | 3.10 | 1.50 |
�е�/�� | 80 | 59 | 156 |
ˮ���ܽ�� | �� | �� | �� |
�����кϳɲ���ش����⣺
(1)��a�м���15 mL��ˮ����������м����b��С�ļ���4.0 mLҺ̬�塣��a�е��뼸���壬�а�ɫ��������������Ϊ������________���塣�����μ���Һ����ꡣװ��d��������______________��
(2)Һ�����������в�������ᴿ��
����a�м���10 mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����Һ������10 mLˮ��8 mL 10%��NaOH��Һ��10 mLˮϴ�ӡ�NaOH��Һϴ�ӵ�������____________��
����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����ˡ������Ȼ��Ƶ�Ŀ����________��
(3)�����Ϸ���������屽�л����е���Ҫ����Ϊ________��Ҫ��һ���ᴿ�����в����б������________(������ȷѡ��ǰ����ĸ)��
A���ؽᾧ B������
C������ D����ȡ
(4)�ڸ�ʵ���У�a���ݻ����ʺϵ���________(������ȷѡ��ǰ����ĸ)��
A��25 mL B��50 mL
C��250 mL D��500 mL
���𰸡�(1)HBr ����HBr��Br2(2)�ڳ�ȥHBr��δ��Ӧ��Br2 �۸��� (3)�� C (4)B
��������(1)��м��������a�з����ķ�ӦΪ![]() ��Br2
��Br2![]()
 ��HBr��HBr������ˮ���������������װ��d�������ǽ���β������������HBr�ͻӷ�������������(2)��δ��Ӧ��Br2�������屽�У���Ϊ���ʣ�Br2��ˮ�е��ܽ�Ƚ�С��������NaOH��Һ��Ӧ���ַ�Ӧ���ɵ�HBr��������ˮ���屽����ḽ���������ᣬ��NaOH��Һϴ�ӵ������dz�ȥHBr��δ��Ӧ��Br2���۷ֳ��Ĵ��屽�л���ˮ�֣����������Ȼ��ƿ��Գ�ȥˮ�֡�(3)�����屽���ܣ��������������û�г�ȥ�����Լ������Ծ��������������屽�е���Ҫ�����DZ������ݱ����屽�ķе��нϴ���죬������ķ������Խ����߷��롣(4)4.0 mLҺ��ȫ������a�����У���a������Һ������ԼΪ19 mL�����ǵ���ӦʱҺ����ܻ���ڣ�Һ��������ܳ���������
��HBr��HBr������ˮ���������������װ��d�������ǽ���β������������HBr�ͻӷ�������������(2)��δ��Ӧ��Br2�������屽�У���Ϊ���ʣ�Br2��ˮ�е��ܽ�Ƚ�С��������NaOH��Һ��Ӧ���ַ�Ӧ���ɵ�HBr��������ˮ���屽����ḽ���������ᣬ��NaOH��Һϴ�ӵ������dz�ȥHBr��δ��Ӧ��Br2���۷ֳ��Ĵ��屽�л���ˮ�֣����������Ȼ��ƿ��Գ�ȥˮ�֡�(3)�����屽���ܣ��������������û�г�ȥ�����Լ������Ծ��������������屽�е���Ҫ�����DZ������ݱ����屽�ķе��нϴ���죬������ķ������Խ����߷��롣(4)4.0 mLҺ��ȫ������a�����У���a������Һ������ԼΪ19 mL�����ǵ���ӦʱҺ����ܻ���ڣ�Һ��������ܳ���������![]() ����ѡ��50 mL����Ϊ�ˡ�
����ѡ��50 mL����Ϊ�ˡ�


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ҩ��ұصá�����Ҫ�ɷֵĽṹ��ʽ��ͼ��ʾ�� ![]()
���й��ڡ��ұصá�����������ȷ���ǣ� ��
A.���������ڲ�������
B.�����ʵķ���ʽΪC13H20O2
C.�������������������
D.���������ڷ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������Ļ�����A������Է�������Ϊ104��̼����������Ϊ92.3%��
(1)A�ķ���ʽΪ____________��
(2)A��������Ȼ�̼��Һ��Ӧ�Ļ�ѧ����ʽΪ____________����Ӧ������____________��
(3)��֪��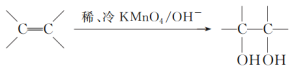 ����д��A��ϡ�����KMnO4��Һ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ___________��
����д��A��ϡ�����KMnO4��Һ�ڼ��������·�Ӧ�Ļ�ѧ����ʽ___________��
(4)һ�������£�A��������Ӧ���õ��Ļ�������̼����������Ϊ85.7%��д���˻�����Ľṹ��ʽ__________________��
(5)��һ�������£���A�ۺϵõ��ĸ߷��ӻ�����Ľṹ��ʽΪ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�д��������һ��������
A. Cu2+��SO42-��OH-��K+B. Na+��CO32-��H+��Cl-
C. H+��Cl-��NO3-��Ba2+D. Ba2+��H+��SO42-��NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д������������ˮ��Һ�еĵ��뷽��ʽ
�Ȼ�ͭ_______________________
Fe2(SO4)3__________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��úȼ�պ����Ҫ������CO��CO2 �� 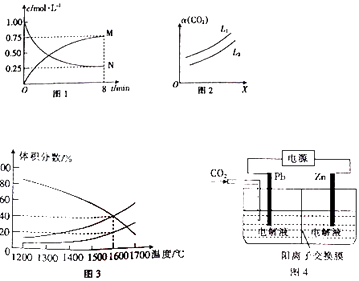
��1����֪����C��s��+H2O��g��CO��g��+H2��g����H1=+131.3KJ/mol
��C��s��+2H2O��g��CO2��g��+2H2��g����H2=+90.0kJ/mol
��CO2��g��+H2��g��CO��g��+H2O��g����H3
��H3=kJ/mol���ڷ�Ӧ�ٵ���ϵ�м����������H1���������С�����䡱����
��2����CO2Ϊԭ�Ͽ��Ʊ��״���CO2��g��+3H2��g��CH3OH��g��+H2O��g����H=��49.0kJ/mol����1L �ĺ����ܱ������г���1molCO2��g����3mol H2��g�������CO2��g����CH3OH��g��Ũ����ʱ��ı仯��ͼ1 ��ʾ��
��ͼ1��N��ʾ�������ѧʽ����0��8min�ڣ���������ʾ��ƽ����Ӧ����v��H2��=mol/��Lmin����
����һ�������£���ϵ��CO2��ƽ��ת���ʣ�������L��X�Ĺ�ϵ��ͼ2 ��ʾ��L��X�ֱ��ʾ�¶Ȼ�ѹǿ��X��ʾ��������������¶ȡ���ѹǿ������L1 ������������� L2 ��
��3����һ���Ϊ20L�ĺ����ܱ�������ͨ��1molCO2������Ӧ2CO2��g���T2CO��g��+O2��g�����ڲ�ͬ�¶��¸����ʵ���������仯��ͼ3��ʾ��1600��ʱ��Ӧ�ﵽƽ�⣬���ʱ��Ӧ��ƽ�ⳣ��K= ��
��4������п��Ӧ�����л��ϳɡ����ӹ�ҵ�ȣ���ҵ����ȡZnC2O4��ԭ����ͼ4��ʾ�����Һ���μӷ�Ӧ����Zn�缫�����������������������������������֪��Pb�缫���õ�ZnC2O4 �� ��Pb�缫�ϵĵ缫��ӦʽΪ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ�ı���������
A.����Ƿ��һ B.��ɢ�������Ĵ�С
C.���������ЧӦ D.��ɢ�������Ƿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϰ�Ŀμ䣬ͬѧ��վ����¥�ϣ����Կ�������Ŀ������ƶ��Ĺ�������������ܽ������Ķ����ЧӦ������˵������ȷ���� (����)
A. �������Һ���ǻ����������ڲ�ͬ�ķ�ɢϵ
B. �����ɢ�����ӵ�ֱ������1��100 nm֮��
C. ���ö����ЧӦ�ɼ��������Һ
D. ���徭��ʱ�侲�ú���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com