
| A. | H2+X2═2HX | B. | X2+H20═HX+HXO | ||
| C. | NaX+AgNO3═AgX↓+NaNO3 | D. | 2NaX+H2SO4(浓)═Na2SO4+2HX |
分析 A.卤素单质都能和氢气反应;
B.氟气和水反应生成氢氟酸和氧气;
C.氟化钠和硝酸银不反应;
D.碘化钠和浓硫酸反应,得不到碘化氢.
解答 解:A.卤素非金属性随着原子序数增大而减弱,元素的非金属性越强,其氢化物的稳定性越强,其单质的氧化性越强,卤素单质氧化性较强,所以卤素单质都能和H2反应,且气态氢化物的稳性随单质氧化性的增强而增强,故A正确;
B.氟气氧化性强,氟气和水反应2F2+2H2O=4HF+O2 ,其余卤素单质和水反应都能用X2+H20═HX+HXO表示,故B错误;
C.氟化银易溶于水,其余卤化银难溶于水,即能发生NaX+AgNO3═AgX↓+NaNO3,故C错误;
D.碘化氢具有较强的还原性,浓硫酸具有强氧化性,碘化钠和浓硫酸反应,得不到碘化氢,故D错误;
故选A.
点评 本题考查卤素通性,题目难度不大,注意卤族元素是典型的非金属元素,注意元素周期律的递变规律,注意把握卤素原子的结构及其单质的性质.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
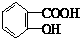 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备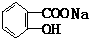
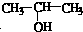 与NaOH的醇溶液共热制备CH3-CH=CH2.
与NaOH的醇溶液共热制备CH3-CH=CH2.| A. | ① | B. | ①② | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学方程式 | 平衡常数K | 化学方程式 | 平衡常数K |
| F2+H2?2HF | 6.5×1095 | Br2+H2?2HBr | 1.9×1019 |
| Cl2+H2?2HCl | 2.6×1033 | I2+H2?2HI | 8.7×102 |
| A. | X2与H2反应的反应速率依次减小 | B. | F2的转化率最大 | ||
| C. | X2与H2反应的剧烈程度逐渐减弱 | D. | 升高温度,平衡常数都增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
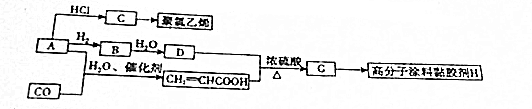
 ,A→C的反应类型:加成反应.
,A→C的反应类型:加成反应.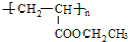 ,写出D的同分异构体的结构简式:CH3OCH3.
,写出D的同分异构体的结构简式:CH3OCH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
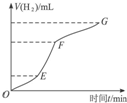 某化学课外小组的同学用Mg等与稀硫酸反应制H2,根据反应进行的情况,同学们得出了反应时间与产生H2的体积关系,并做出了如图.请回答:
某化学课外小组的同学用Mg等与稀硫酸反应制H2,根据反应进行的情况,同学们得出了反应时间与产生H2的体积关系,并做出了如图.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com