
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
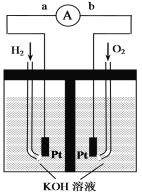
(1)氢氧燃料电池的能量转化主要形式是_______,在导线中电子流动方向为____(用a、b表示)。
(2)负极反应式为_________________________。
(3)电极表面镀铂粉的原因为______________________。
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2![]() 2LiH
2LiH
II.LiH+H2O =LiOH+H2↑
①反应Ⅰ中的还原剂是___,反应II中的氧化剂 是_____。
②已知LiH固体密度为0.82 g/cm3。用锂吸收224 L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为________。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为_________mol。
【答案】由化学能转变为电能 由a到b 2H2+4OH--4e- = 4H2O 或H2+2OH--2e- = 2H2O 增大电极单位面积吸附H2、O2分子数,加快电极反应速率,同时也增大了Pt的利用率以降低成本 Li H2O 1/1148或8.71×10-4 32
【解析】
(1)原电池的能量转化形式主要是将化学能转化为电能;
(2)负极发生的是氧化反应,对应通氢气的一极,注意所给介质为碱性;
(3)在氢氧燃料电池中,多孔的铂片可以直接作电极。本题中在电极表面镀上一层细小的铂粉,从题干强调的“细”、“粉”,“吸附气体的能力强”进行分析表述。
(4)通过价态变化进行氧化剂和还原剂的判断。通过所给的化学方程式进行求算。
(1)氢氧燃料电池作为原电池,其能量转化主要形式是化学能变为电能;通入H2的a电极为负极,通入O2的b电极为正极,电子从负极经外电路流向正极,所以导线中电子流动方向为由a到b;
(2)所给介质为强碱性介质,所以负极的电极反应式为: H2+2OH--2e-= 2H2O,如考虑与正极电极反应式从形式上即可看出得失电子数相等,该电极反应式也可以写成:2H2+4OH--4e-=4H2O;
(3)电极表面镀铂粉的原因为:镀上铂粉,可以增大该电极单位面积吸附H2、O2分子数,从而加快电极反应的速率。与直接使用多孔铂电极相比,降低了成本而提高了贵金属Pt的利用率;
(4)①从价态变化可以明显看出,反应Ⅰ中Li的化合价由0价升至+1价,还原剂是Li,反应II,LiH中H的化合价为-1价,水中H的化合价为+1价,产物H2既是氧化产物又是还原产物,氧化剂是H2O;
②标准状况下224 LH2的物质的量为10mol,用锂吸收生成的LiH的物质的量为20mol,其质量为20mol×8g/mol=160g,又知LiH的密度为0.82g/cm3,所以生成的LiH的体积为:![]() =195.12cm3,所以生成的LiH体积与被吸收的H2体积比为:
=195.12cm3,所以生成的LiH体积与被吸收的H2体积比为:![]() =
=![]() (或8.71×10-4);
(或8.71×10-4);
③由②生成的LiH为20mol,与H2O作用,放出的H2为20mol;这些氢气用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为:20mol×2×80%=32mol。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下

已知:①菱锰矿的主要成分是MnCO3,还含少量Fe、Al、Ca、Mg等元素。
②相关金属离子[c0(Mn+)=0.1mol/L形成氢氧化物沉淀的pH范围如下:

③常温下,CaF2、MgF2的溶度积分别为1.46×10-10、7.42×10-11。
回答下列问题:
(1)“焙烧”时发生的主要反应的化学方程式为__________________。
分析下列图1、图2、图3,氯化铵焙烧菱锰矿的最佳条件是:焙烧温度为_________、氯化铵与锰矿粉的质量之比为_________、焙烧时间为_________。

(2)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式为_________;再调节溶液的pH将Al3+、Fe3+变为沉淀除去,溶液pH的范围为_________;然后加入NH4F将Ca2+、Mg2+变为CaF2、MgF2沉淀除去,两种沉淀共存时溶液中c(Ca2+)/c(Mg2+)=_________。
(3)碳化结晶时,反应的离子方程式为__________________。
(4)将制得的高纯度碳酸锰溶于过量稀硫酸后用惰性电极电解,在某极得到重要的无机功能材料MnO2,该电极的电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学教材中元素周期表的一部分,其中标出A~R15种元素,试根据它们回答下列问题(填具体元素符号或化学式):
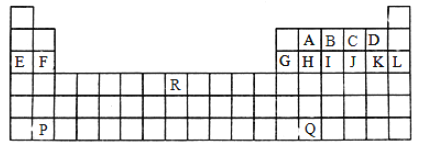
(1)最高价氧化物对应的水化物中酸性最强的是_____,单质中氧化性最强的是_____,第三周期元素形成的简单离子中半径最小的是______。
(2)C与E可形成一种具有漂白性的物质,它含有的化学键为_____。
(3)Q在元素周期表中的位置是____,B、C可形成化合物B2C,该化合物的核外电子总数为____。
(4)P的最高价氧化物对应的水化物与B的最高价氧化物对应的水化物的离子方程式:_____。
(5)元素E与元素F相比,金属性较强的是____(用元素符号表示),下列表述中能证明这一事实的是______(填序号)。
a.与酸反应时,每个F原子比每个E原子失电子数多
b.E的氢化物比F的氢化物稳定
c.E和F的单质与水反应E较剧烈
d.最高价氧化物对应水化物碱性E比F强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中铝制品比铁制品耐腐蚀的原因是( )
A.铝的金属活动性比铁弱
B.铝不与氧气发生化学反应
C.铝在空气中易与氧气反应形成一层致密的氧化膜
D.铝的密度比铁的密度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、D、E、W是中学常见的四种元素,原子序数依次增大。A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是__________________。
(2)下列事实能用元素周期律解释的是_____(填字母序号)。
a . D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是__________。
(4)①工业上用电解法制备D的单质,反应的化学方程式为____________________。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为____________________。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。
① 上述反应的离子方程式为__________。
② D的单质与X在高温下反应的化学方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某无色溶液中加入BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则有关溶液中含有的离子说法正确的是( )
A.一定有SO42-B.一定没有SO42-
C.一定有Ag+D.可能是SO42-,也可能是Ag+,但二者不能同时存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在做浓硫酸与铜反应的实验过程中,观察到铜片表面变黑,于是对黑色物质的组成进行实验探究。
(1)用如右图所示装置进行实验1。(加热和夹持仪器已略去)

实验1:铜片与浓硫酸反应
操作 | 现象 |
加热到120℃~250℃ | 铜片表面变黑,有大量气体产生,形成墨绿色浊液 |
继续加热至338℃ | 铜片上黑色消失,瓶中出现“白雾”,溶液略带蓝色,瓶底部有较多灰白色沉淀 |
①装置B的作用是________;装置C中盛放的试剂是_______。
②为证明A装置中灰白色沉淀的主要成分为硫酸铜,实验操作及现象是___________。
(2)探究实验1中120℃~250℃时所得黑色固体的成分。
【提出猜想】黑色固体中可能含有CuO、CuS、Cu2S中的一种或几种。
【查阅资料】
资料1:亚铁氰化钾[K4Fe(CN)6]是Cu2+的灵敏检测剂,向含有Cu2+的溶液中滴加亚铁氰化钾溶液,生成红棕色沉淀。
资料2:
CuS | Cu2S |
黑色结晶或粉末 | 灰黑色结晶或粉末 |
难溶于稀硫酸;可溶于硝酸;微溶于浓氨水或热的浓盐酸 | 难溶于稀硫酸和浓盐酸;可溶于硝酸;微溶于浓氨水 |
【设计并实施实验】
实验2.探究黑色固体中是否含CuO
操作 | 现象 |
i.取表面附着黑色固体的铜片5片,用清水洗干净,放入盛有10mL试剂A的小烧杯中,搅拌 | 黑色表层脱落,露出光亮的铜片 |
ii.取出铜片,待黑色沉淀沉降 | 上层溶液澄清、无色 |
①试剂A是_________。
②甲认为ii中溶液无色有可能是Cu2+浓度太小,于是补充实验确认了溶液中不含Cu2+,补充的实验操作及现象是______。
实验3.探究黑色固体中是否含CuS、Cu2S
操作 | 现象 |
i.取实验2中黑色固体少许,加入适量浓氨水,振荡后静置 | 有固体剩余,固液分界线附近的溶液呈浅蓝色 |
ii.另取实验2中黑色固体少许,加入适量浓盐酸,微热后静置 | 有固体剩余,溶液变成浅绿色 |
【获得结论】由实验2和实验3可得到的结论是:实验1中,120℃~250℃时所得黑色固体中_______。
【实验反思】
分析实验1中338℃时产生现象的原因,同学们认为是较低温度时产生的黑色固体与热的浓硫酸进一步反应造成。已知反应的含硫产物除无水硫酸铜外还有二氧化硫,则黑色固体消失时可能发生的所有反应的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由铁、铜和稀硫酸组成的原电池,所发生的总反应的离子方程式是
A. Fe-2e-=Fe2+ B. Cu2++2e-=Cu
C. 2H++2e-=H2↑ D. Fe+2H+=Fe2++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知SO2和O2反应生成2molSO3时,放出的热量为QkJ,在1L的密闭容器中进行反应2SO2(g)+O2(g)![]() 2SO3(g),SO2、O2、SO3的起始物质的量分别为0.2mol、0.1mol、0.2mol,下列叙述正确的是( )
2SO3(g),SO2、O2、SO3的起始物质的量分别为0.2mol、0.1mol、0.2mol,下列叙述正确的是( )
A. 某时刻,SO3的物质的量为0.28 mol,则SO2的转化率为40%
B. 反应达到平衡时放出的热量为0.1QkJ
C. 某时刻,SO2、O2、SO3的物质的量分别为0.3mol、0.15mol、0.15mol
D. 某时刻,SO3的浓度可能为0.4mol-1·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com